Clear Sky Science · sv
Anti-TLR2-immunterapi påverkar neuron-till-oligodendrocyt-överföring av α-synuklein i mus- och människomodeller
Varför denna forskning är viktig
Multipel systematrofi (MSA) är en sällsynt men snabbt framskridande hjärnsjukdom som kombinerar Parkinson-liknande rörelsestörningar med balans- och autonoma svikt, till exempel blodtrycksfall. Läkare kan lindra symtom, men de kan i nuläget inte bromsa sjukdomens förlopp. Denna studie avslöjar hur ett felveckat protein sprids mellan hjärnceller och skadar hjärnans "isolering" och visar att en riktad antikroppsbehandling kan avbryta denna process i djur- och cellmodeller. Arbetet pekar på en konkret, läkemedelsliknande strategi som en dag skulle kunna förändra MSA:s förlopp i stället för att bara behandla symtomen.
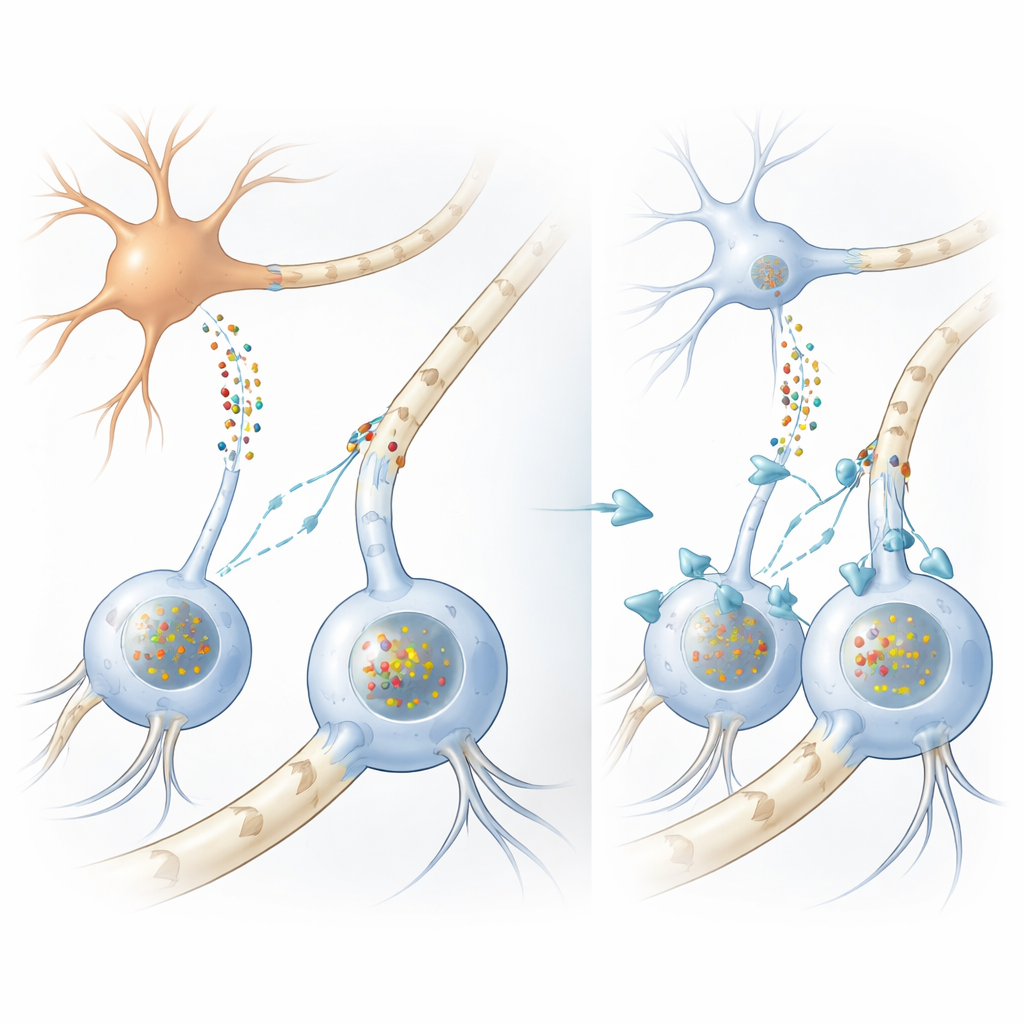
Hur hjärnans ledningsnät går fel
I många rörelsestörningar, inklusive Parkinsons sjukdom, samlas klumpar av ett protein kallat alfa-synuklein inuti nervceller. Hos MSA bildas däremot de mest iögonfallande ansamlingarna inne i stödjeceller som kallas oligodendrocyter, vilka normalt sveper nervfibrer med fettiga myelinskidor som snabbar upp elektriska signaler. Underligt nog producerar oligodendrocyter själva väldigt lite alfa-synuklein, vilket lämnat en länge liggande gåta: varifrån kommer de omfattande proteinavlagringarna i dessa celler? Författarna bekräftade först, med mänskliga hjärnprover och storskaliga RNA-analyser, att oligodendrocyter verkligen producerar avsevärt mindre alfa-synuklein än neuroner, vilket stärker idén att det skadliga proteinet måste komma utifrån.
Protein överförs från neuron till stödjecell
För att testa detta byggde teamet flera kompletterande modeller. I rätter odlade de mänskliga oligodendrocytliknande celler från neurala stamceller och exponerade dem för vätska insamlad från neuronliknande celler som var konstruerade för att frisätta stora mängder alfa-synuklein. Stödjecellerna tog upp proteinet och utvecklade klumpar som starkt liknade de gliala inklusionerna som ses i MSA-hjärnor, inklusive samma kemiska markörer och hjälpproteiner. När forskarna undersökte en musstam som producerar mänskligt muterat alfa-synuklein endast i neuroner, fann de åter mänskliga proteinkluster inne i oligodendrocyter i vit substans, trots att dessa celler inte uttryckte den mänskliga genen. Tillsammans visar dessa experiment att alfa-synuklein kan förflytta sig från neuroner till oligodendrocyter och bilda sjukdomsliknande inklusioner där.
Porten på cellytan
Nästa fråga var hur proteinet tar sig in i oligodendrocyterna. Tidigare arbete hade identifierat immunsensoren Toll-lik receptor 2 (TLR2) på cellytor som en dockningsplats för alfa-synuklein i neuroner och mikroglia. Genom att gräva i genuttrycksdatamängder från MSA-hjärnor fann teamet att oligodendrocyter hos patienter bar ovanligt höga nivåer av TLR2 jämfört med kontroller, och att högre TLR2 kopplades till lägre nivåer av myelinrelaterade gener såsom myelin basic protein. Denna relation framträdde inte i flera oberoende Parkinson-datamängder, vilket antyder att oligodendrocyters känslighet för alfa-synuklein via TLR2 är ett utmärkande drag för MSA snarare än ett generellt kännetecken för alla synukleinopatier.
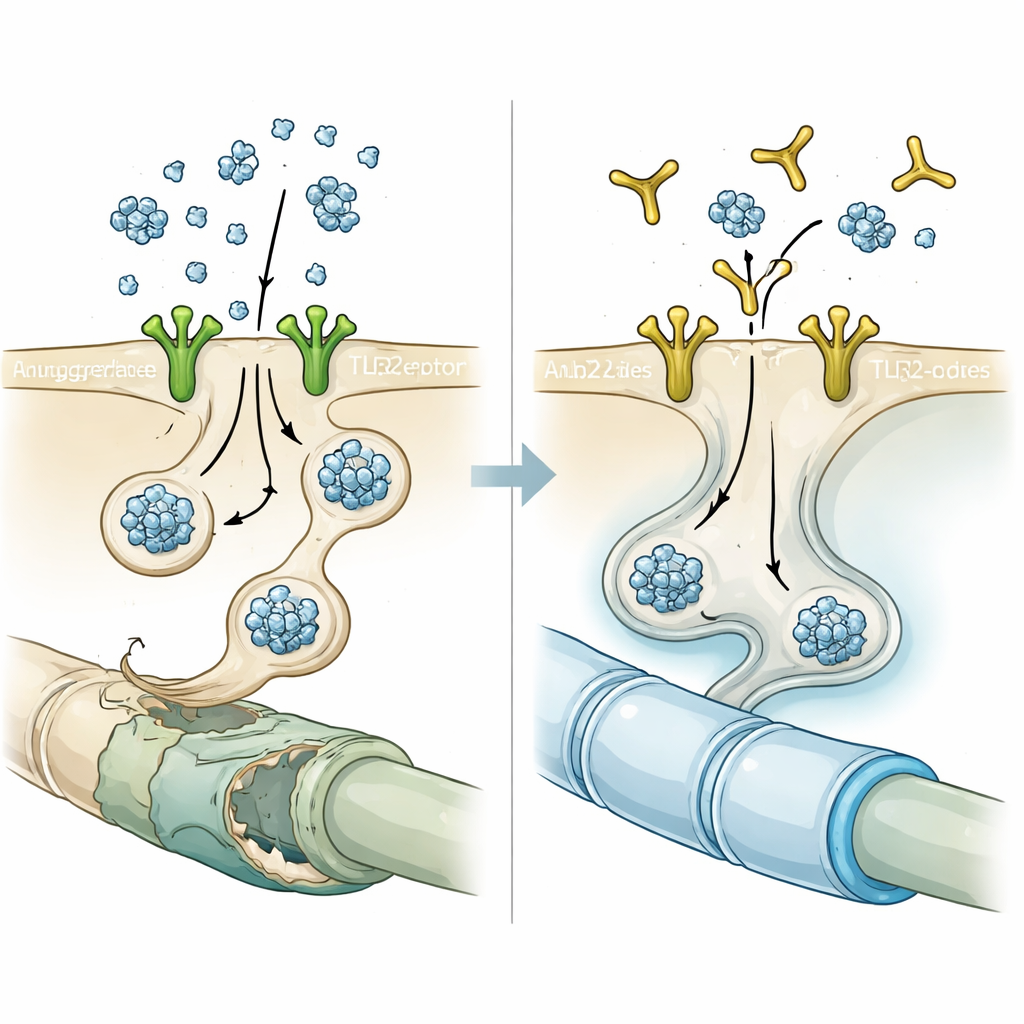
Blockera porten med en antikropp
Med denna ledtråd testade forskarna NM-101, en antikropp utformad för att binda TLR2 och förhindra dess aktivering. I cellkulturer minskade kort förbehandling av oligodendrocyter med NM-101 innan tillsats av neuronellt härlett alfa-synuklein kraftigt antalet och intensiteten av inklusionsliknande klumpar. I möss som antingen överproducerade neuronalt alfa-synuklein eller fick injektioner av färdiga alfa-synukleinfibriller sänkte veckovisa infusioner av NM-101 aggregerat protein i vit substans, dämpade inflammatoriska responser från mikroglia och astrocyter och minskade aktiveringen av ett inflammatoriskt enzym kallat kaspas-1 inne i oligodendrocyterna. Behandlade djur levde längre och presterade bättre i motoriska tester, vilket tyder på att antikroppens skyddande effekter var funktionellt meningsfulla, inte bara mikroskopiska fynd.
Återställa skadad isolering
Eftersom oligodendrocyter är hjärnans myelltillverkare undersökte teamet om alfa-synukleinöverföring skadade myelinet och om blockering av TLR2 kunde hjälpa. Enkelcells-RNA-sekvensering av mänskligt härledda oligodendrocyter exponerade för neuronconditionerat alfa-synuklein visade breda skift bort från ett moget, myeltillverkande tillstånd mot en mer omogen, progenitorlik profil, med många centrala myelengener nedreglerade. Parallella genuttrycksstudier av laserfångade oligodendrocyter från MSA-patienter och från musmodellen visade en delad signatur: minskat uttryck av gener inblandade i bildandet och underhållet av myelin. I elektronmikroskop visade vit substans hos alfa-synukleinmössen tunnare, oorganiserade myelinskidor. NM-101-behandling vände många av dessa förändringar, förtjockade myelinet, återställde nivåer av myelinproteiner och normaliserade uttrycket av gener nödvändiga för oligodendrocytmognad.
Vad detta betyder för framtida behandlingar
Studien stöder en tydlig berättelse: vid MSA kan alfa-synuklein som produceras av neuroner spridas in i oligodendrocyter via TLR2 på deras yta, där det byggs upp, utlöser inflammation, ställer till det för cellernas utvecklingsprogram och urholkar myelinskiktet på hjärnans ledningar. Genom att blockera TLR2 med en riktad antikropp kunde forskarna avbryta denna händelsekedja i möss och mänskliga cellmodeller, minska giftiga inklusioner, dämpa inflammation, reparera myelin och förbättra överlevnad och rörelseförmåga. Medan NM-101 i sig fortfarande behöver rigorösa prövningar på människor, etablerar arbetet TLR2-beroende proteinöverföring som en central drivkraft i MSA-liknande patologi och framhäver anti-TLR2-immunterapi som en lovande strategi för att bromsa eller förebygga denna förödande sjukdom.
Citering: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Nyckelord: multipel systematrofi, alfa-synuklein, oligodendrocyter, myelinskada, immunterapi