Clear Sky Science · sv
Ökad NKG2D-känslighet gör tumörer mer mottagliga för kombinerad anti-PD1- och anti-VEGF-behandling och förhindrar hörselförlust
Varför denna forskning är viktig för personer med hörselnedsättning
Vissa människor ärver ett tillstånd som kallas NF2-relaterad schwannomatos, vilket orsakar godartade tumörer på nerverna i innerörat och ofta leder till gradvis, permanent hörselnedsättning. Nuvarande behandlingar kan krympa tumörerna men kan skada hörseln eller sluta fungera över tid. Denna studie undersöker en ny läkemedelskombination som inte bara bromsar tumörtillväxt i laboratoriemodeller utan också hjälper till att skydda hörseln, vilket pekar mot skonsammare och potentiellt mer långvariga alternativ för patienter.
Att förstå tumörerna bakom tystnaden
I NF2-relaterad schwannomatos bildas tumörer som kallas vestibulära schwannom på balans- och hörselnerven inne i skallen. När dessa tumörer växer kan de skada de känsliga nervfibrerna som för ljudsignaler till hjärnan och i svåra fall trycka på hjärnstammen. Kirurgi och strålning kan rädda liv och ta bort eller kontrollera tumörer, men båda innebär verkliga risker: försämrad hörsel, yrsel och svaghet i ansiktsnerven. Ett läkemedel som heter bevacizumab, som blockerar en tillväxtsignal för blodkärl (VEGF), används ibland för att krympa dessa tumörer och förbättra hörseln, men bara ungefär en tredjedel av patienterna får nytta och effekten avtar ofta. Detta har drivit sökandet efter behandlingar som är både säkrare och mer långvariga.
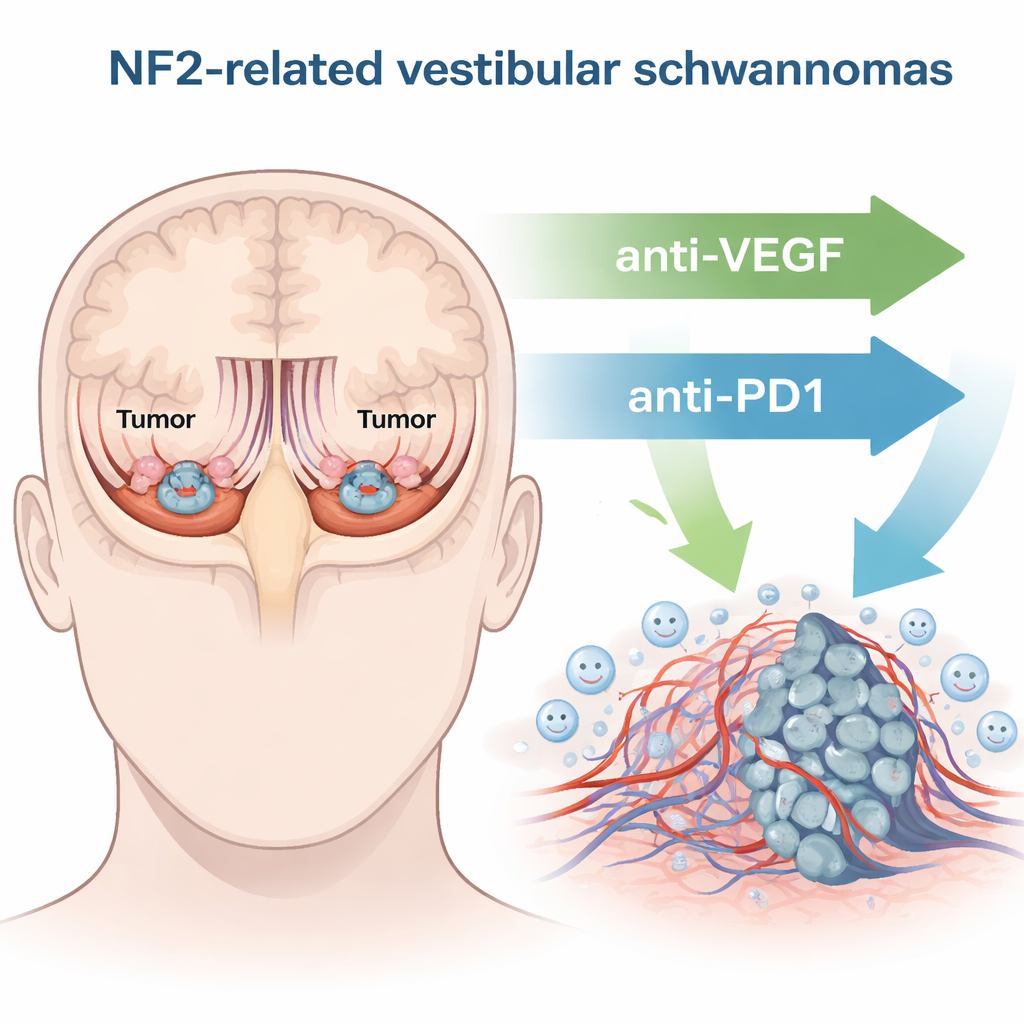
Rekrytera immunförsvaret som allierad
Under det senaste decenniet har cancerterapi omvandlats av immunkontrollpunktshämmare—läkemedel som släpper på immuncellernas ”bromsar” så att de bättre kan angripa tumörer. En sådan broms, PD-1, sitter på ytan av immunceller och kan stänga av dem när den aktiveras. Författarna undersökte om blockering av PD-1 (med en anti-PD1-antikropp) kunde hjälpa immunförsvaret att kontrollera vestibulära schwannom, och om kombination med VEGF-blockerande terapi skulle fungera ännu bättre. Med hjälp av musemodeller som nära efterliknar mänskliga innerörs- och periferala nervtumörer behandlade de djur med antingen anti-VEGF, anti-PD1 eller kombinationen, och följde därefter tumörtillväxt, överlevnad och hörsel.
Få tumörernas blodkärl att fungera bättre, inte försvinna
Teamet fann att anti-VEGF gjorde mer än att bara svälta tumörer. Det omformade deras onormala, läckande blodkärl till mer stabila, bättre fungerande kanaler. Under mikroskop hade behandlade tumörer fler kärl täckta av stödjeceller och en större andel kärl som faktiskt bar blod. Denna ”normalisering” förbättrade leveransen av anti-PD1-antikroppen in i tumören och tillät fler cancerbekämpande immunceller—särskilt CD8 T‑celler och naturliga mördarceller (NK‑celler)—att komma in. Hos möss som gavs kombinationsbehandling växte tumörerna långsammare, hade färre delande celler och fler celler som genomgick programmerad celldöd, och djuren levde längre än vid någon av läkemedlen ensamma.
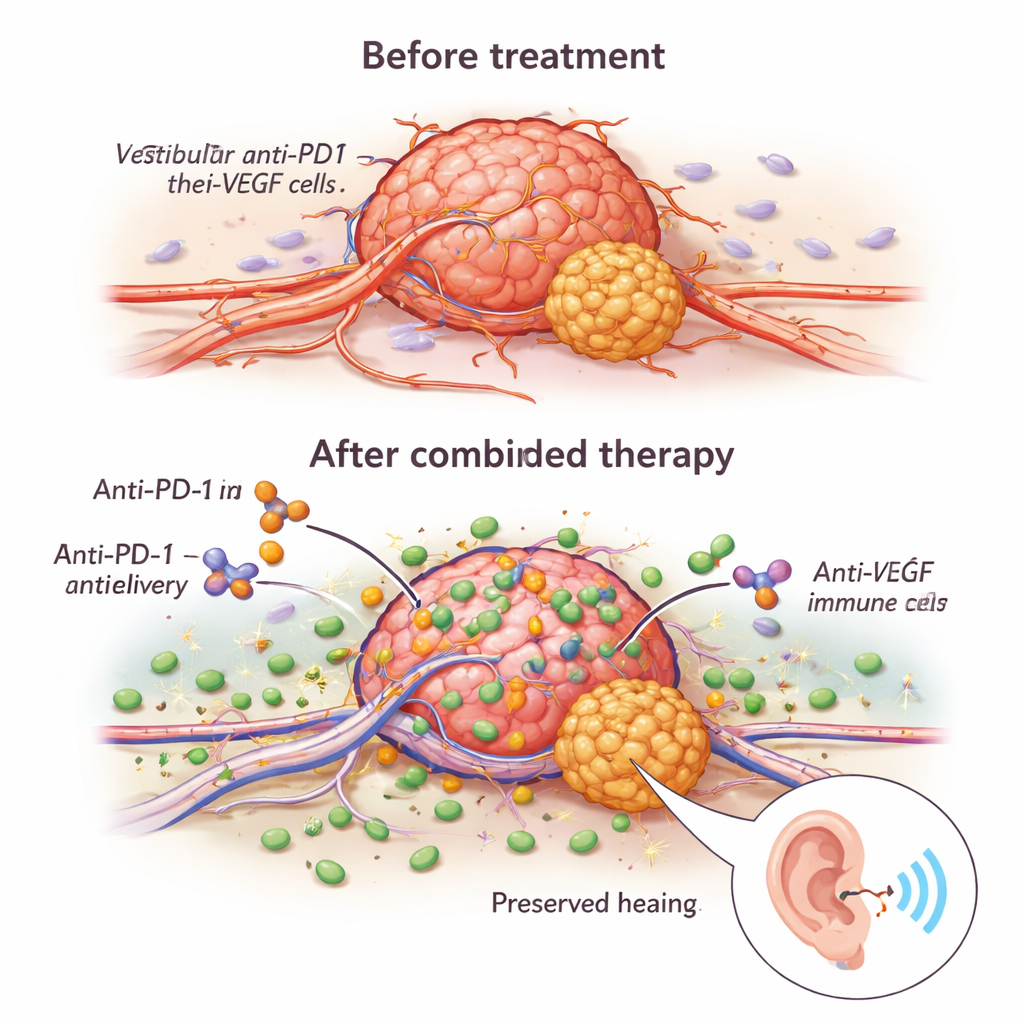
Öka immuncellernas dödskraft
Fördelarna med kombinationen handlade inte bara om att få fler immunceller in i tumören; dessa celler var också mer aggressiva när de väl anlände. Anti-VEGF-behandling ökade förekomsten av molekyler som granzyme B och perforin, immunsystemets molekylära ”kulor” för att skapa hål i tumörceller. En nyckelregulator i detta var en receptor kallad NKG2D, som finns på både T‑celler och NK‑celler. Anti-VEGF ökade NKG2D och dess partnermolekyler på tumörceller, vilket gjorde immuncellerna till effektivare mördare i laboratorietester. När forskarna blockerade NKG2D minskade de anti-tumöreffekter som terapierna gav markant, vilket visar att denna väg är central för läkemedelssynergins effekt. Viktigt är att små prov från mänskliga tumörer som fått långvarig behandling med bevacizumab visade genaktivitetsmönster förenliga med mer aktiverade och mindre ”utmattade” T‑celler och NK‑celler, vilket tyder på att liknande immunförstärkning kan ske hos patienter.
Skydda hörseln samtidigt som tumörer kontrolleras
En avgörande fråga var om dessa immunbaserade behandlingar skulle skada eller hjälpa hörseln. När friska möss fick anti-PD1 ensamt förblev deras hörseltrösklar normala, vilket tyder på att läkemedlet inte orsakar kortsiktig skada på hörselsystemet. I tumörbärande möss förbättrade anti-VEGF ensamt hörseln jämfört med ingen behandling, vilket speglar klinisk erfarenhet. Anti-PD1 ensamt och kombinationen av anti-PD1 med anti-VEGF återställde båda hörseltrösklarna till nästan normala nivåer. När forskarna efterliknade ett verkligt scenario—först behandla tumörer med anti-VEGF och sedan antingen fortsätta, avbryta eller lägga till anti-PD1—fann de att övergång till anti-PD1 fortfarande kunde bromsa tumörtillväxt, men att avbrott av anti-VEGF tog bort dess hörselfördel. Att fortsätta anti-VEGF och lägga till anti-PD1 gav de bästa resultaten för både överlevnad och bevarande av hörseln.
Vad detta kan innebära för patienter
För personer som lever med NF2-relaterad schwannomatos tyder detta arbete på en framtid där behandling gör mer än att bara hålla tumörer i schack—den kan också bevara hörseln. I omsorgsfullt utformade musemodeller skapade kombinationen av en VEGF‑hämmare och en PD‑1‑hämmare en vänligare miljö för immunceller, förstärkte deras tumördödande kraft via NKG2D och skyddade hörseln bättre än någon av metoderna ensamma. Medan kliniska prövningar fortfarande behövs för att bekräfta säkerhet och nytta hos människor lägger studien upp en tydlig färdplan för att testa denna läkemedelsparet som en ny, potentiellt mer hållbar strategi för att hantera vestibulära schwannom och förhindra hörselförlust.
Citering: Lu, S., Yin, Z., Wu, L. et al. NKG2D upregulation sensitizes tumors to combined anti-PD1 and anti-VEGF therapy and prevents hearing loss. Nat Commun 17, 1148 (2026). https://doi.org/10.1038/s41467-026-68865-8
Nyckelord: vestibulärt schwannom, NF2, immunterapi, bevacizumab, hörselbevarande