Clear Sky Science · sv
Antiparallell stapling av Csu-pili driver Acinetobacter baumannii:s tredimensionella biofilmsammansättning
Hur sjukhusbakterier bygger skyddade städer
Vissa av de svåraste sjukhusbakterierna överlever antibiotika genom att gömma sig i slemmiga, tredimensionella gemenskaper kallade biofilmer. Denna studie ställer en enkel men avgörande fråga: hur flätar enskilda bakterier ihop sig till sådana robusta, lager-på-lager-strukturer? Genom att zooma in med avancerade elektronmikroskop avslöjade forskarna en mikroskopisk ”velcro” av hårlika filament som låter den farliga patogenen Acinetobacter baumannii väva sig till skyddande 3D-klumpar. Att förstå detta dolda skelett kan öppna nya vägar för att riva isär biofilmer och få befintliga läkemedel att fungera bättre.
Små hår som håller bakterier ihop
A. baumannii, en huvudorsak till svårbehandlade sjukhusinfektioner, är täckt av tunna ythår kallade Csu-pili. Tidigare arbete visade att dessa pili är avgörande för att bilda robusta, kupolliknande biofilmer, men ingen visste hur de faktiskt sammanflätar celler till en 3D-struktur. Med flera former av elektronmikroskopi bekräftade författarna först att i flytande odling sticker pili för det mesta ut enskilt från varje bakterie, som taggar på en kardborre. I täta, yttillväxta kolonier förändras bilden dock dramatiskt: många pili packas tätt tillsammans och bildar breda, platta band som löper mellan närliggande celler och skapar ett ömtådigt men omfattande nätverk i tre dimensioner. 
Platta stegar byggda av parade filament
För att lista ut hur dessa band bildas renade teamet Csu-pili och observerade vad de gjorde av sig själva. Över dagar till veckor började enskilda filament para sig och sedan smälta samman till mångfilamentiga ”superstackar”, som så småningom bildade ett gel-liknande nätverk som starkt efterliknade strukturerna som sågs i verkliga biofilmer. Högupplöst kryoelektronmikroskopi avslöjade den underliggande konstruktionen. Varje pilus är inte ett jämnt rör utan en zickzackande stav. När två stavar ligger sida vid sida i motsatta riktningar möts de vid upprepade hörnpunkter och bildar stabila laterala korsningar. Många sådana antiparallella par kan sedan rada upp sig till en mycket tunn, skivliknande stapel—i princip en mikroskopisk stege eller band som är endast ett filament tjockt men många filament brett.
En inbyggd ritning för 3D-tillväxt
De detaljerade strukturerna visar att denna staplingsförmåga är inbyggd i piliernas egen geometri. Zickzackmönstret upprepas över mycket korta avstånd och skapar många potentiella kontaktpunkter längs varje filament. Som en följd, när två pili möts i rätt orientering, kan en kedja av korsningar bildas likt en dragkedja och snabbt förlänga skivan. Viktigt är att sättet stavarna vänder sig på säkerställer att kontakter oftast bildas mellan pili från olika celler, inte samma cell, vilket naturligt främjar cell–cell-länkning. Staplarna förblir flexibla och töjbara, så den växande biofilmen kan absorbera fysisk påfrestning utan att brytas sönder. Forskarna såg att under celldelning hamnar nya dotterceller ofta med sina pili placerade ansikte mot ansikte, vilket uppmuntrar stapelbildning precis där det behövs för att knyta celler till en 3D-kluster. 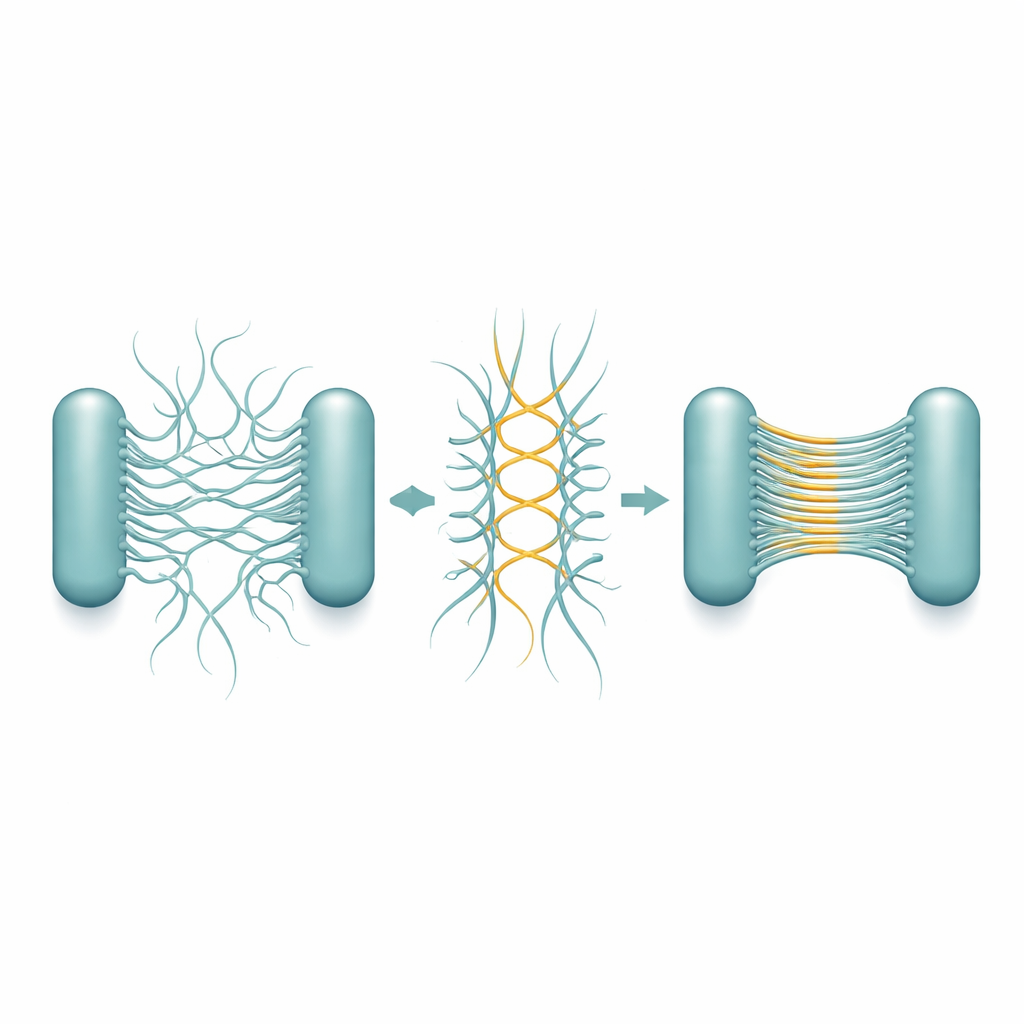
Lim, fyllnad och tidigt skelett
Studien undersökte också hur andra komponenter i biofilmen bidrar. Ett sockermolekylärt polymer kallat PNAG och löst DNA från sönderslagna celler är känt för att ansamlas i mogna biofilmer. Mikroskopi visade dessa substanser fylla de smala gliporna mellan bakterier och omsluta pilusstaplarna, ungefär som betong som hälls runt armeringsjärn. Men när teamet avlägsnade PNAG och DNA bildade bakterierna fortfarande organiserade flottar hållna samman av Csu-pilusstaplarna ensamma. Detta visar att pili bygger det primära skelettet, medan det omgivande materialet senare cementerar och stabiliserar strukturen.
Nya svaga punkter i bakteriella fästningar
Förenklat förklarar detta arbete hur A. baumannii använder sina ythår för att snöra sig till tuffa, flerskiktade klumpar som läkemedel och immunceller har svårt att tränga igenom. Pili fungerar först som krokar för att greppa ytor och sedan som flexibla remmar som staplas till platta skivor och binder samman närliggande celler i alla riktningar. Sockerpolymerer och DNA fyller sedan i mellanrummen och förvandlar detta remnät till en solid fästning. Genom att precisera hur pili fäster vid varandra framhäver studien ett nytt mål: läkemedel eller molekyler som blockerar pilus–pilus-kontakter skulle kunna försvaga biofilmskelettet inifrån och göra långvariga bakteriella infektioner lättare att rensa ut.
Citering: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Nyckelord: biofilmer, Acinetobacter baumannii, pili, antibiotikaresistens, kryoelektronmikroskopi