Clear Sky Science · sv
cGAS-IFN-I‑svar genom att extrahera nukleärt DNA från döende celler via nukleocytos
Hur vårt immunsystem läser DNA från de döda
När våra celler dör vid infektioner, cancer eller genom vardagligt slitage måste deras rester städas upp utan att väcka för mycket inflammation. Denna artikel avslöjar ett överraskande sätt som immunceller faktiskt kan borra sig in i kärnorna hos döende celler, dra ut deras DNA och använda det som en fara-signal. Att förstå detta dolda system för städning och alarm kan förändra hur vi tänker kring antivirala läkemedel, autoimmunitet, cancerbehandling och läkemedelsbiverkningar.
En dold DNA‑alarm inuti immunceller
Våra celler innehåller en sensor kallad cGAS som upptäcker DNA på fel plats — flytande i cytosolen istället för säkert packat i kärnan eller mitokondrierna. När cGAS möter sådant DNA slår den på ett kraftfullt larmprogram som producerar typ I interferoner, nyckelproteiner för antiviral och immunsreglering. Forskare har vetat att virus kan leverera sitt genetiska material in i celler för att trigga denna väg, och att bitar av vårt eget DNA ibland kan läcka ut och orsaka autoimmuna sjukdomar. Men en grundläggande gåta kvarstod: hur når stora mängder av vårt eget DNA, särskilt från döda celler, cGAS utan att först brytas ner i cellens ”magar” kallade lysosomer?
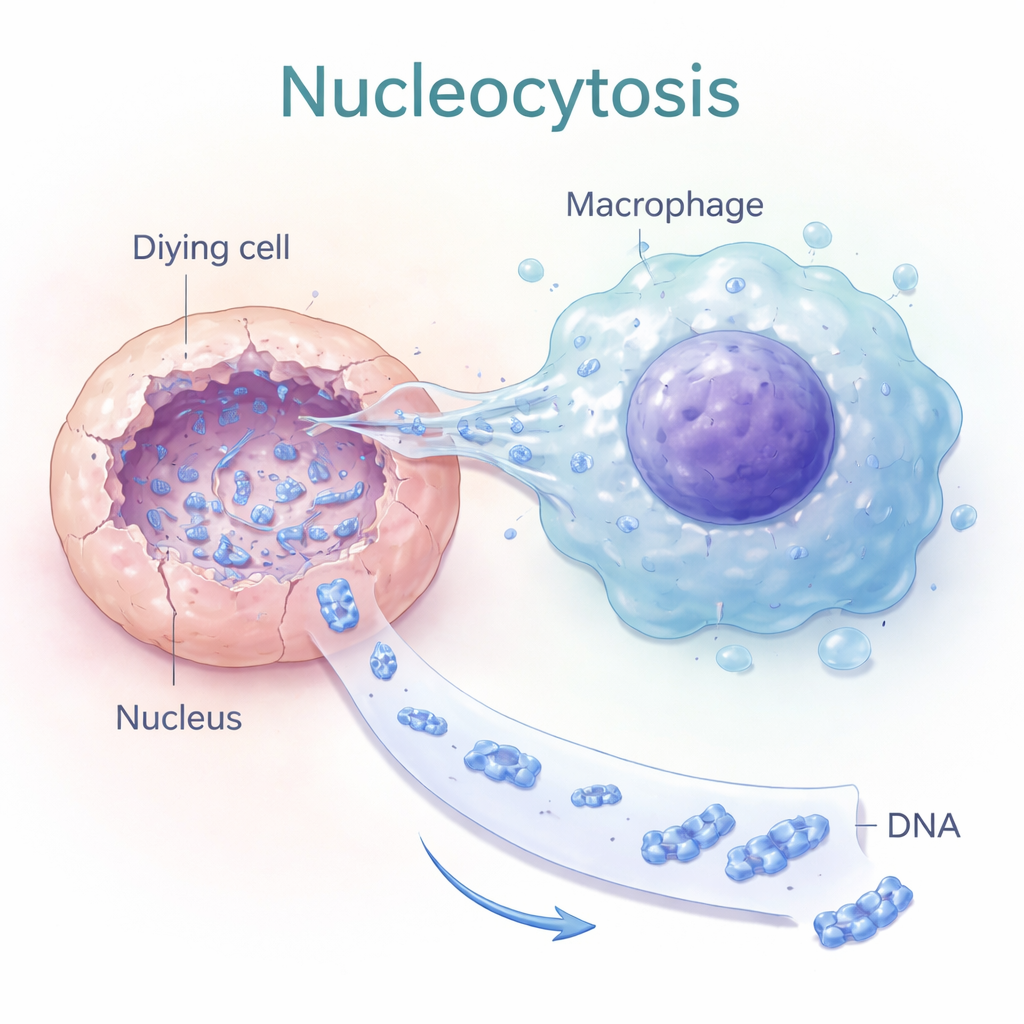
Nukleocytos: att borra in i döda cellkärnor
Författarna upptäckte en process som de kallar ”nukleocytos”, där vissa makrofager — immunceller som normalt tar upp skräp — gör något mycket mer riktat. Istället för att svälja en hel död cell sträcker de ut tunna, fingerlika utlöpare direkt in i den döende cellens kärna. Live‑cell‑avbildning visade att DNA‑intensiteten sjönk inne i den döda cellens kärna samtidigt som den ökade inne i den anslutna makrofagen, vilket tyder på aktiv extraktion av nukleärt DNA. Denna överföring var beroende av cellens inre skelett (aktin) och av signalmolekyler som styr cellens form, vilket tyder på att nukleocytos är ett avsiktligt mekaniskt beteende, inte ett passivt läckage.
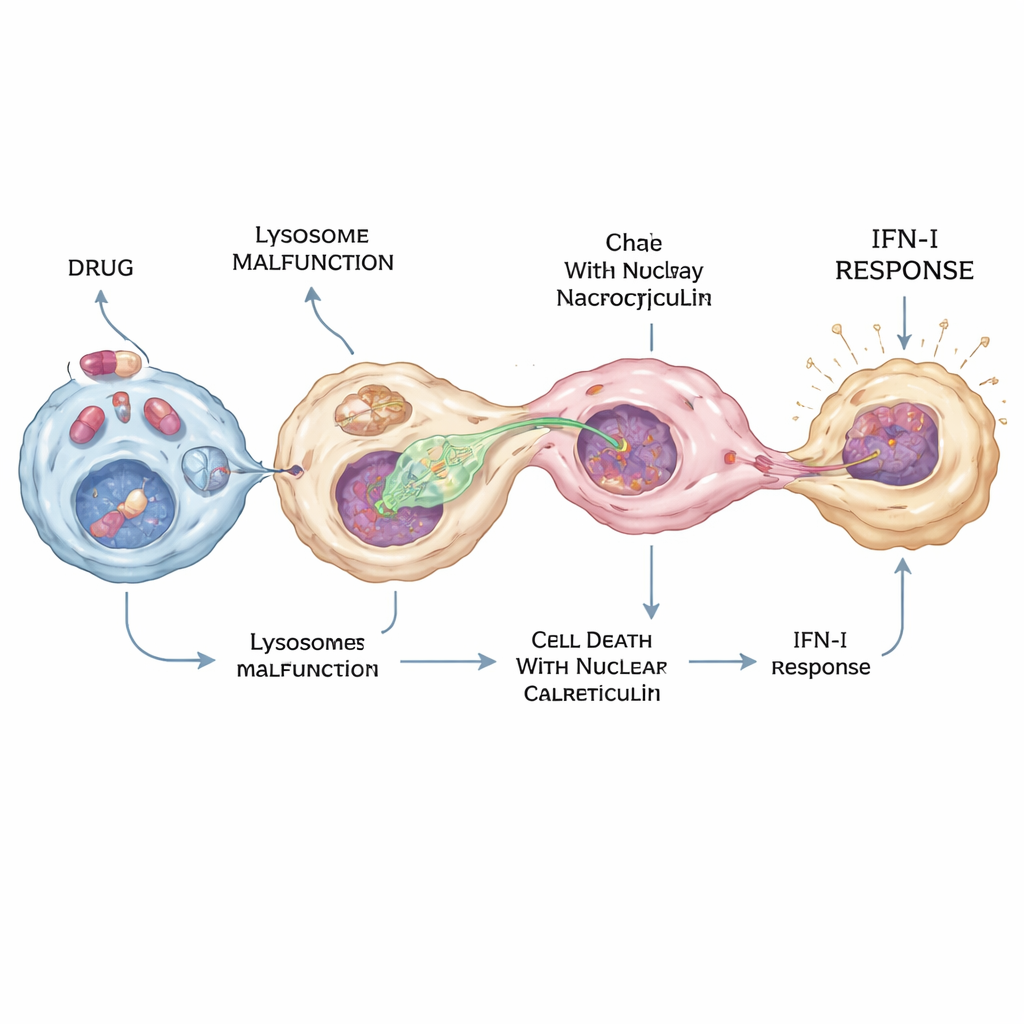
När antivirala läkemedel slår på DNA‑alarmet
Under COVID‑19‑pandemin testades läkemedel som hydroxyklorokin i stor utsträckning som antivirala, men deras exakta verkan i kroppen förblev oklara. Forskarna fann att hydroxyklorokin och flera närbesläktade ”kationiska amphifila” läkemedel starkt kan aktivera cGAS–STING–interferon‑vägen — men endast i en delmängd av makrofager. Dessa läkemedel stör lysosomer genom att höja deras pH och genom att blockera ett enzym kallat PPT1, som hjälper till att bryta ner fettsyror på proteiner. Den kombinerade effekten driver vissa celler in i en speciell form av celldöd där ett protein kallat kalretikulin ansamlas i kärnan. Makrofager sträcker då i första hand ut utlöpare mot dessa kalretikulin‑rika kärnor, extraherar DNA via nukleocytos och utlöser intensiv interferonproduktion i bara ett fåtal celler — tillräckligt för att skapa en stark lokal antiviral signal utan att översvämma hela kroppen.
Från lokal försvar till sjukdom och biverkningar
Genom att studera både cellkulturer och muslungor visade teamet att läkemedelsbehandlade makrofager kan utlösa ett STING‑beroende interferonsvar som förblir i stort sett lokalt — till exempel i lungan — snarare än blir systemiskt. Detta hjälper till att förklara varför läkemedel som hydroxyklorokin kan ge antivirala eller antitumöreffekter i vissa vävnader, men också varför de kan orsaka organspecifika biverkningar såsom ögon‑ eller hjärttoxicitet vid långvarig användning. Samma nukleocytosprocess skulle rimligen kunna bidra till autoimmuna eller inflammatoriska sjukdomar när döda celler och lysosomstress sammanfaller, eftersom den erbjuder en direkt väg för själv‑DNA att slå på cGAS‑larmet.
Varför detta spelar roll för framtida behandlingar
För en icke‑specialist är huvudbudskapet att immunceller inte bara passivt äter döda celler; de kan aktivt bryta in i deras kärnor för att hämta DNA och använda det som en signal för att ropa på hjälp. Denna nukleocytosväg förklarar hur vårt eget DNA säkert kan aktivera kraftfulla antivirala försvar på ett fokuserat, lokalt sätt, samtidigt som den belyser hur läkemedel som stör lysosomer eller PPT1 oavsiktligt kan slå på denna brytare. Genom att lära sig reglera nukleocytos upp eller ner — antingen genom att designa smartare antivirala och cancerbehandlingar eller genom att undvika oönskade själv‑DNA‑signaler vid autoimmuna sjukdomar — hoppas forskare kunna utnyttja denna nyupptäckta mekanism för säkrare och mer precisa terapier.
Citering: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Nyckelord: nukleocytos, cGAS-STING, hydroxyklorokin, typ I interferon, makrofager