Clear Sky Science · sv
Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice
Att förvandla strålning till en immunallierad
Onkologer försöker i allt högre grad engagera immunsystemet för att bekämpa tumörer, men många cancerformer ignorerar eller motstår fortfarande dessa läkemedel. Den här studien ställer en aktuell fråga: kan olika typer av riktad strålning användas inte bara för att krympa tumörer direkt utan också för att coacha immunsystemet att göra ett bättre jobb — och förändrar valet av radioaktivt läkemedel hur den coachningen fungerar?
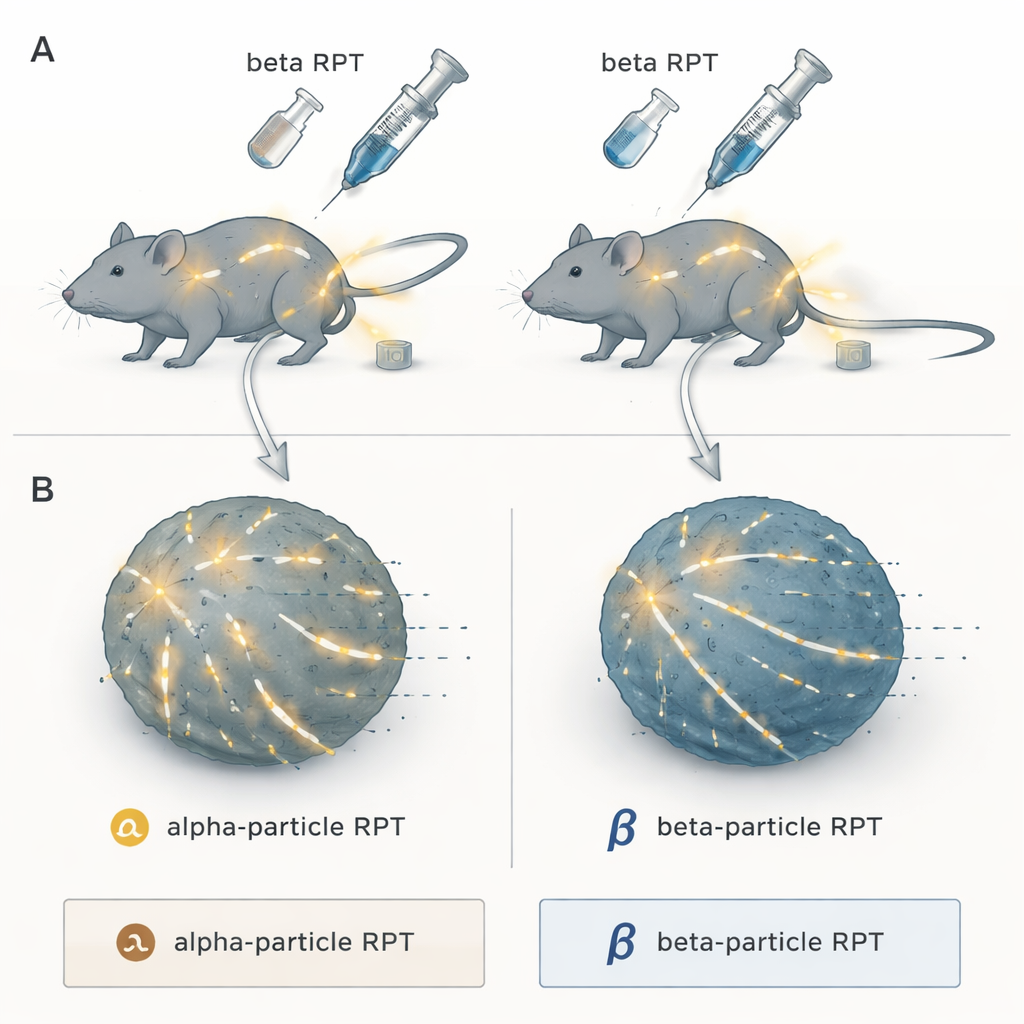
Två varianter av precisionsstrålning
Forskarna fokuserade på radiofarmakoterapi, en "sök‑och‑förstör"‑metod där en radioaktiv last kopplas till en molekyl som naturligt söker sig till tumörer. När den injiceras cirkulerar den i kroppen och levererar strålning till cancertumörer varhelst de gömmer sig — något vanlig extern strålbehandling har svårt att göra vid spridd sjukdom. Teamet jämförde två huvudkategorier: alfastrålande ämnen, som frigör extremt täta energiburstar över mycket korta avstånd, och betastrålande ämnen, som sänder ut lägre täthet av strålning som färdas längre genom vävnad. Alla var bundna till samma tumörsökande förening, NM600, så att endast strålningstypen — inte målinriktningen — skilde dem åt.
Att kombinera strålning med hämmare av immunkontrollpunkter
På egen hand kan checkpointhämmare som anti‑PD‑L1 och anti‑CTLA4 lyfta bromsarna för immunceller, men de fungerar bäst när tumören redan är synlig för immunsystemet. I musmodeller för melanom, prostatacancer och kolorektalcancer gav forskarna en noga vald låg dos strålning från antingen alfarelaterat eller betabaserat NM600, med eller utan en kombination av checkpointhämmare. De varierade också när immundrogerna gavs — före, strax efter eller långt efter den radioaktiva behandlingen — för att se hur tidpunkten påverkade utfall som tumörtillväxt, överlevnad och långsiktigt immunminne.
När betastrålning glänser: förstärka en befintlig respons
I en "immunkall"? nej, i en "immune‑hot" kolorektalcancermodell som redan svarar på immunterapi kom de bästa resultaten från betastrålande NM600, särskilt när immundrogerna startades tidigt eller vid en mellanliggande tidpunkt. Tumörer krympte mer, mössen levde längre, och botade djur avvisade ofta samma cancer när den återintroducerades månader senare. Detaljerad immunprofilering visade att betabaserad behandling plus checkpointblockad inte så mycket skapade en ny respons som förstärkte en som redan fanns: befintliga tumörspecifika mördande T‑celler expanderade, blev mer aktiverade och producerade fler angreppssignaler. Kort sagt var betaemittrar utmärkta på att propagera en pågående immunrespons.
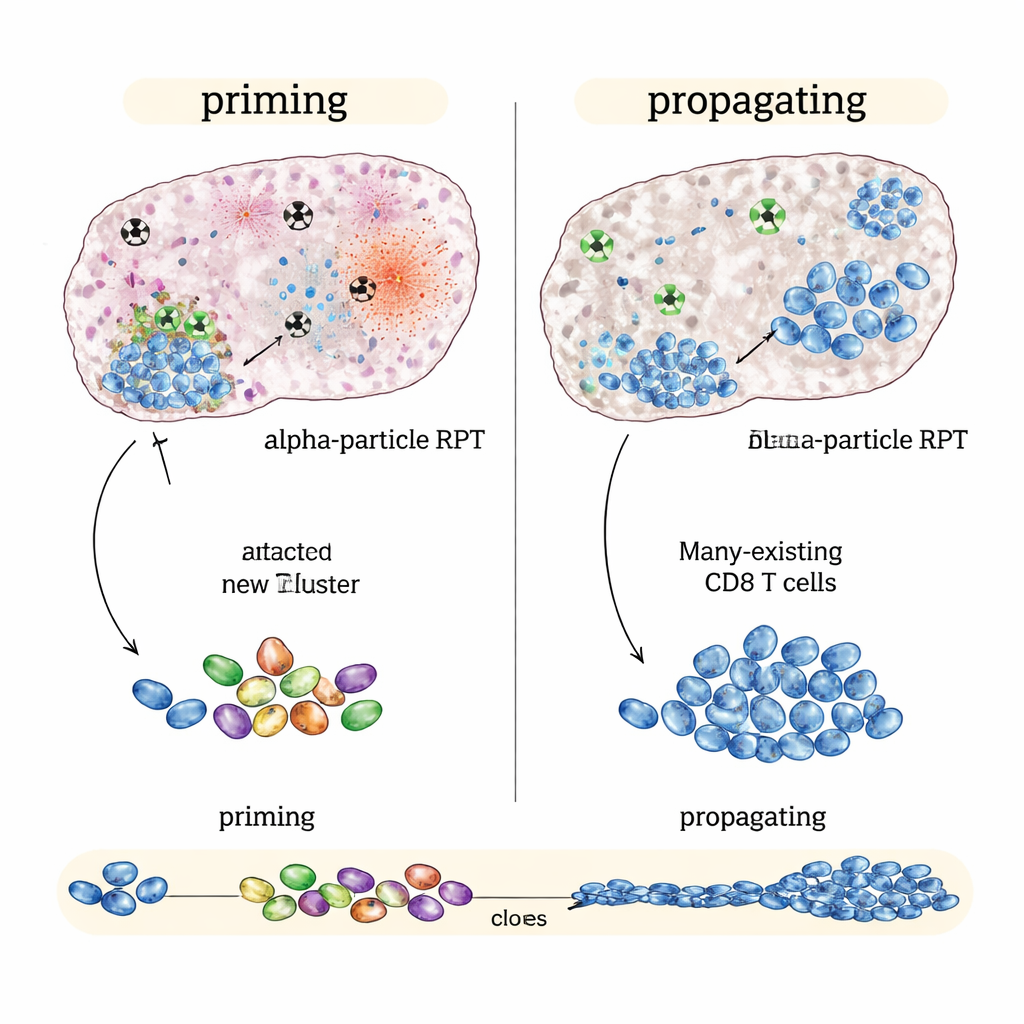
När alfastrålning glänser: tända en ny immunattack
Tvärtemot detta, i "immune‑cold" tumörer som en melanommodell och en prostatacancermodell som knappt svarar på checkpointläkemedel ensamma, presterade den alfastrålande varianten bättre än betaemittrar vid samma genomsnittliga tumördoss. Alfa‑baserad terapi plus immundroger bromsade tumörtillväxten mer och förlängde överlevnaden ytterligare. Enkelcellsgenetiska analyser antydde varför: alfastrålning orsakade intensiv, lokaliserad skada som verkade generera starka alarmsignaler inne i tumören samtidigt som närliggande immunstrukturer skonsades. Detta mönster kopplades till bredare, mer diversifierade T‑cellsvar och tecken på att nya tumörigenkännande mördande T‑celler bildades och kopplades till långlivade minnesceller — bevis för immunpriming snarare än blott förstärkning.
Varför typ och timing av strålning spelar roll
I de olika modellerna presterade tidig eller mellanliggande tidsplacering av checkpointhämmare — ungefär i takt med när strålningsinducerade dangersignaler når sin topp — konsekvent bättre än fördröjd behandling. Arbetet antyder en praktisk tumregel: i cancerformer som redan är synliga för immunsystemet kan lågdos beta‑baserade radiofarmaka vara idealiska partner till checkpointhämmare eftersom de propagerar och stärker befintlig immunitet. I mer immunresistenta tumörer kan högpåverkande alfaemittrar vara bättre lämpade för att priming av nya T‑cellsvar och förvandla en "cold" tumör till "hot". För patienter innebär detta att inte alla radioaktiva läkemedel är utbytbara; att matcha isotop och schema med tumörens immunpersonlighet kan göra kombinations radio‑immunterapi både mer effektiv och mer varaktig.
Citering: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Nyckelord: radiopharmaceutical therapy, alpha vs beta radiation, immune checkpoint inhibitors, cancer immunotherapy, tumor microenvironment