Clear Sky Science · sv
Säkerhet och biologisk aktivitet hos en bispecifik T‑cellreceptor riktad mot HIV Gag hos män som lever med HIV: en förstai‑människa‑studie
Varför denna nya HIV‑studie är viktig
Människor som lever med HIV kan i dag förvänta sig nästan normala livslängder tack vare moderna läkemedelskombinationer. Men dessa läkemedel, så kallad antiretroviral behandling (ART), tar inte bort viruset; de håller det bara under kontroll. Dolda fickor av HIV finns kvar i kroppen och kan starta om infektionen om behandlingen upphör. Denna studie testar en ny typ av precisions‑immunkur—byggd kring en laboratorieframställd T‑cellreceptor—som syftar till att träna immunsystemet att säkert jaga upp dessa gömställen hos personer som redan har välkontrollerad infektion på ART.
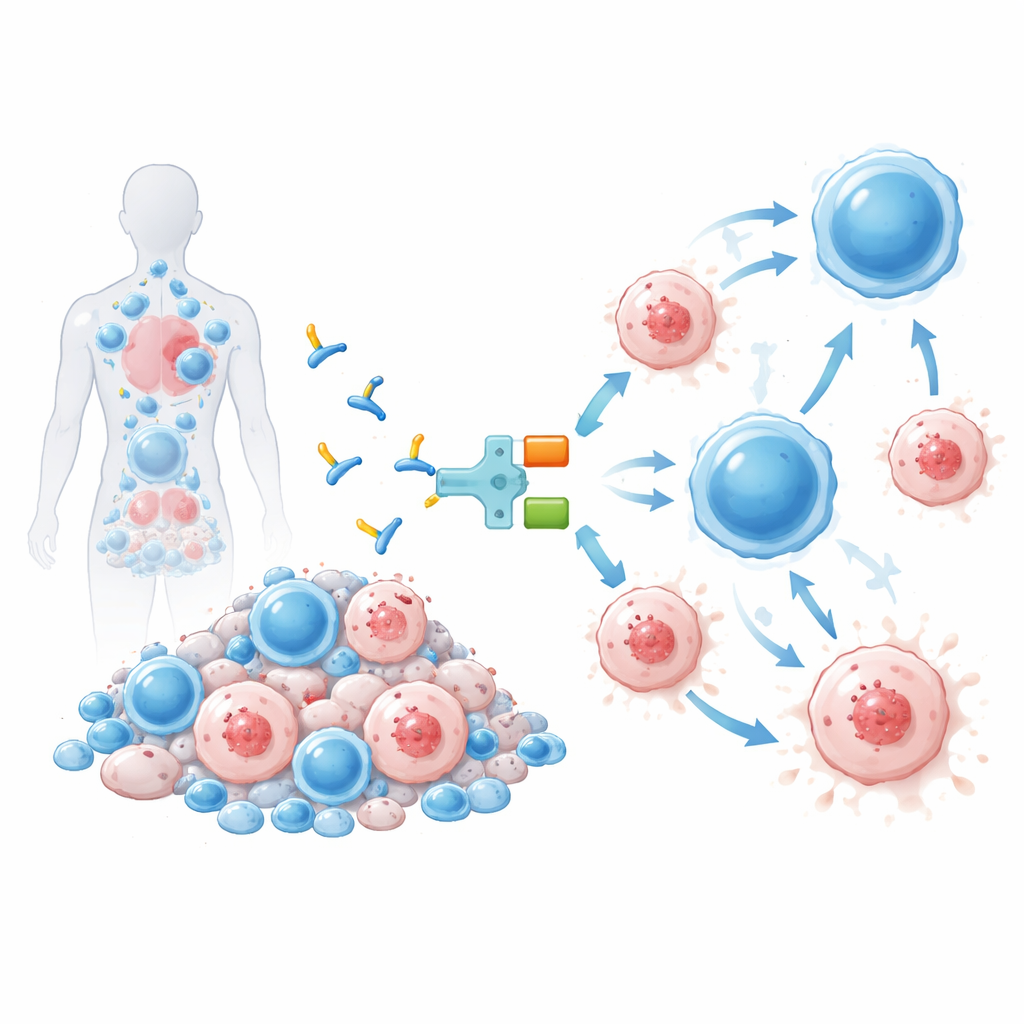
Det dolda viruset som inte försvinner
Även när blodprover visar “otiddetekterbart” virus, kvarstår HIV som genetiskt material inneslutet i långtlevande celler, främst en typ av vita blodkroppar som kallas CD4‑T‑celler. Dessa reservoirceller bär tyst men intakt virus som kan vakna till liv igen, vilket tvingar personer att ta dagliga piller livet ut. Att helt utplåna varje infekterad cell är extremt svårt och har bara uppnåtts hos ett fåtal personer som genomgick riskfyllda benmärgstransplantationer för cancer. Många forskare siktar istället på en ”funktionell bot”: att krympa reservoaren tillräckligt så att kroppens egna försvar kan hålla HIV i schack utan konstant medicinering.
En designad molekyl som omdirigerar T‑celler
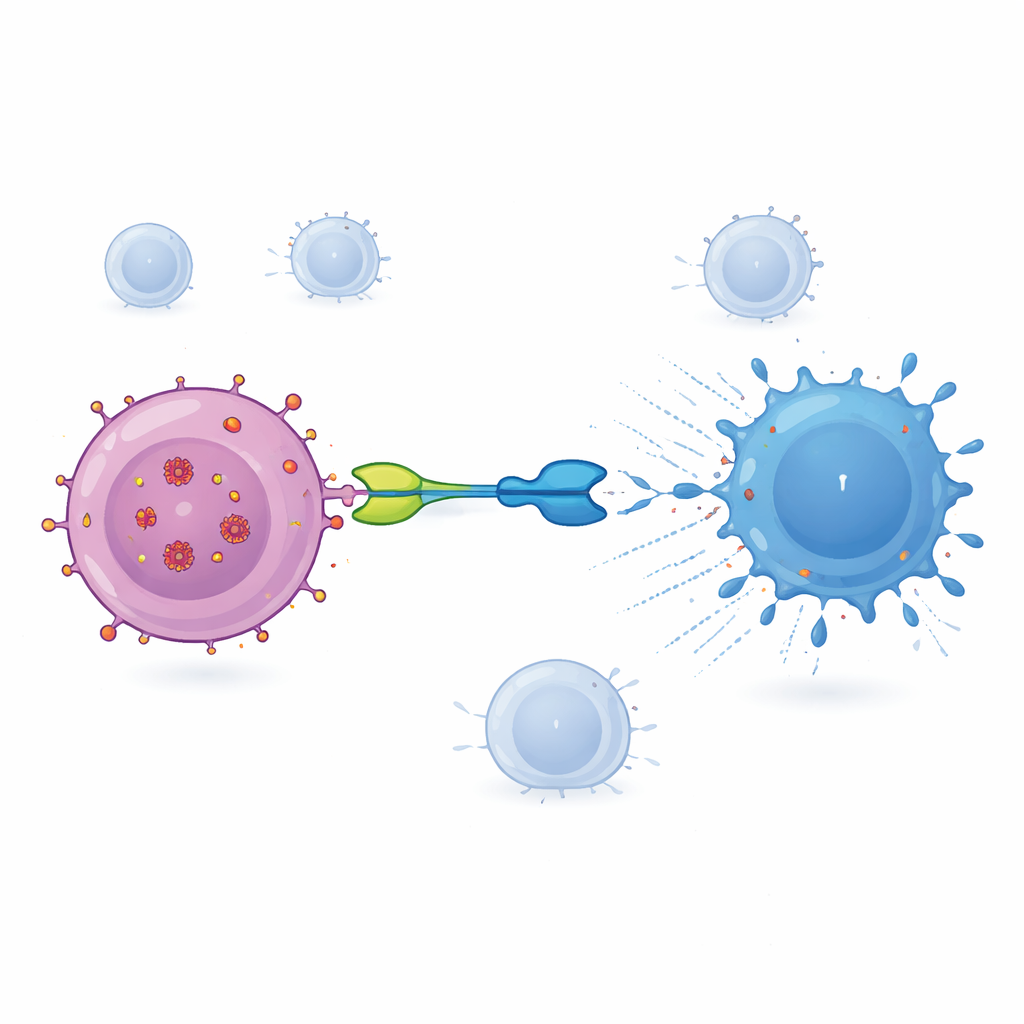
Den terapi som testas här, kallad IMC‑M113V, är ett litet protein som fungerar som en molekylär adapter mellan infekterade celler och immunsystemet. Ena änden av IMC‑M113V är en konstruerad T‑cellreceptor som känner igen ett litet HIV‑fragment från Gag‑proteinet som visas på ytan av infekterade celler i samband med en vanlig immunsignal (HLA‑A*02:01). Den andra änden fäster vid CD3, en struktur som finns på alla T‑celler. När IMC‑M113V binder båda sidor samtidigt för den vanliga T‑celler i nära kontakt med en HIV‑infekterad cell och utlöser att de dödar den. I laboratorietester var denna molekyl mycket känslig, den upptäckte endast några få kopior av virusfragmentet på en cells yta och eliminerade effektivt celler infekterade med flera vanliga HIV‑varianter, samtidigt som den inte visade någon meningsfull aktivering mot ett urval friska humana celler.
Första testet i människor som lever med HIV
För att se om detta tillvägagångssätt är säkert hos människor genomförde forskarna en tidig fas‑prövning i tolv vuxna män som lever med HIV i Storbritannien, Belgien och Spanien. Alla deltagare hade välkontrollerad infektion på ART, höga CD4‑värden och bar det krävs HLA‑typen. Varje person fick en engångsinjektion av IMC‑M113V intravenöst på en av tre låga dosnivåer och övervakades noggrant under en månad. Huvudfokus i detta skede var säkerhet: att leta efter biverkningar såsom feber, svår inflammation eller neurologiska problem, som kan förekomma med andra potenta T‑cells‑aktiverande läkemedel som används vid cancerbehandling.
Vad forskarna observerade i kliniken
Över alla doser var IMC‑M113V generellt väl tolererad. Hälften av deltagarna rapporterade vissa biverkningar, mestadels milda problem som trötthet eller hudirritation, och ingen utvecklade allvarliga komplikationer som cytokinfrisättningssyndrom eller neurotoxicitet. Blodprover visade att nivåerna av läkemedlet steg och föll inom ungefär en dag, med en halveringstid på cirka 15–22 timmar. Vid den högsta dosen (15 mikrogram) uppvisade flera deltagare tillfälliga ökningar i inflammatoriska molekyler, särskilt interleukin‑6, och tecken på att deras T‑celler hade blivit aktiverade och mer kapabla att producera celldödande proteiner. Dessa immunsvar var starkast hos volontärer vars virus bar Gag‑varianter som IMC‑M113V kan binda särskilt starkt, vilket tyder på att läkemedlet engagerade sina avsedda mål i kroppen. Efter en enda dos sågs emellertid ingen mätbar minskning av storleken på HIV‑reservoaren i blodet, bedömt utifrån virus‑RNA och intakt virus‑DNA i CD4‑celler.
Vad detta betyder för framtida HIV‑behandling
För en icke‑specialist är huvudbudskapet att denna studie levererar ett viktigt första bevis för konceptet: en högt riktad immunkopplande molekyl kan ges säkert till personer med välkontrollerad HIV och kan väcka deras T‑celler till att känna igen celler som rymmer viruset. Den botade inte HIV eller gjorde det möjligt för deltagare att sluta med ART, men det var inte målet för denna förstai‑människa‑prövning. Resultaten stödjer att testa högre och upprepade doser, eventuellt i kombination med läkemedel som får fler infekterade celler att blotta sig, och att utvidga tillvägagångssättet för att omfatta andra immuntyper utöver HLA‑A*02:01. Om framtida studier bekräftar att denna strategi på ett pålitligt sätt kan krympa virala reservoarer utan farliga biverkningar, kan den bli en nyckelkomponent i kombinationsbehandlingar inriktade på långsiktig, läkemedelsfri kontroll av HIV.
Citering: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Nyckelord: HIV‑bot, T‑cellsterapi, viralt reservoar, bispecifik receptor, klinisk prövning