Clear Sky Science · sv
Mekanistiska insikter i PCBP1-styrd veckning upp av utvalda i-motiv-DNA vid G1/S-kontrollpunkten
DNA-veck som fungerar som trafikljus
Inuti våra celler är den genetiska koden mer än en enkel rak stege av DNA. Delar av den kan vika sig till ovanliga former som fungerar som små brytare och hjälper till att styra när celler kopierar sitt DNA och delar sig. Denna studie fokuserar på en sådan form, kallad i-motiv, och på ett protein som heter PCBP1 som kan känna igen och veckla upp dessa strukturer just när en cell förbereder sig för att replikera sitt DNA. Att förstå denna interaktion ger insikt i hur celler bevarar sin genoms stabilitet och vad som kan gå fel vid cancer.
Underliga DNA-knutar i regioner kopplade till cancer
De flesta lär sig att DNA bildar den välkända dubbelspiralen, men vissa sekvenser rika på bokstaven C (cytosin) kan vika sig till en fyrsträngad knut känd som ett i-motiv. Dessa strukturer tenderar att uppträda i reglerande regioner av gener som driver celltillväxt, såsom cMYC och BCL2. Under åratal har forskare diskuterat om i-motiv verkligen bildas i levande celler, eftersom de är lättare att påvisa i sura provrörsförhållanden än vid de nära neutrala förhållanden som råder i kroppen. Med specialiserade antikroppar som känner igen i-motiv har nyare arbete, inklusive denna studie, bekräftat att de förekommer i cellkärnor—och ofta klustrar nära viktiga tillväxt- och cancerassocierade gener.
Ett protein som plockar ut speciella DNA-veck
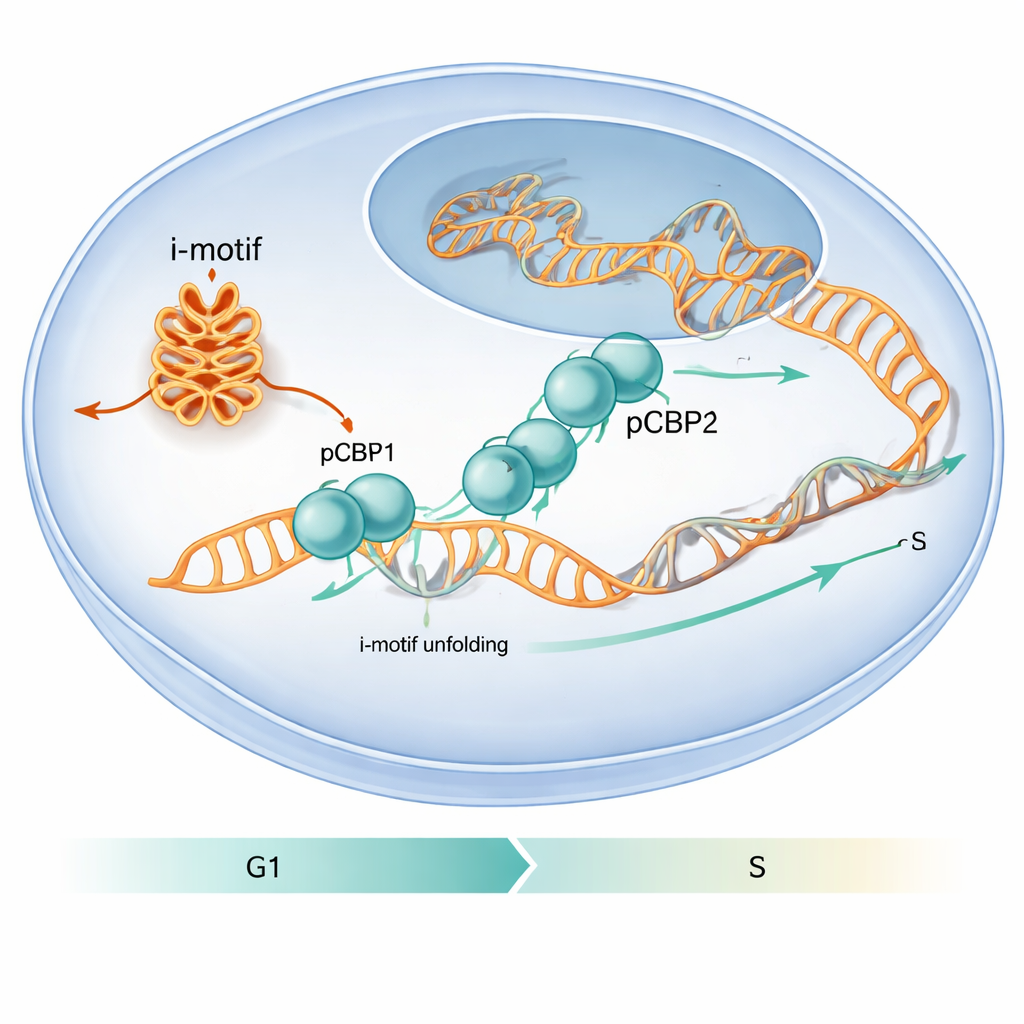
Författarna ville ta reda på hur proteiner i cellen hanterar dessa ovanliga DNA-veck. De fokuserade på PCBP1, ett protein som redan är känt för att binda C-rika DNA- och RNA-sträckor och påverka cellcykeln. Genom att analysera befintliga genomomfattande bindningskartor och utföra riktade experiment fann de att PCBP1 ofta sitter på C-rika regioner som kan bilda i-motiv, särskilt runt geners startsidor. I cellexperiment med humana cancercellinjer visade regioner från promotrarna för cMYC, BCL2 och den insulinrelaterade ILPR-sekvensen både starka i-motiv-signaler och stark PCBP1-ockupation, vilket tyder på att PCBP1 fungerar som en dedikerad väktare av dessa strukturer.
Hur PCBP1 griper tag i och vecklar upp knuten
I provrörsbaserade tester jämförde forskarna hur väl PCBP1 binder veckade i-motiv jämfört med samma DNA i en veckad upp lös form. De justerade surheten så att DNA antingen förblev veckat eller slappnade av, samtidigt som proteinet var stabilt. PCBP1 föredrog alltid det veckade i-motivet och band det ungefär dubbelt så starkt som samma sekvens i uppveckat tillstånd, och svarade endast svagt på orelaterade DNA-strukturer. När det väl bundit kunde PCBP1 aktivt främja uppveckning, vilket tillät i-motivsträngen att para sig med sin komplementära partner. Dock uppträdde inte alla i-motiv likadant: vissa, såsom strukturen i cMYC-promotorn, vecklades upp snabbt, medan andra, som de i BCL2, var motståndskraftiga och vecklades upp först långsamt. Ytterligare egenskaper såsom hårnålsloopar i DNA och graden av protonering av cytosiner (dvs. extra positiv laddning) kunde antingen underlätta eller hindra PCBP1:s uppveckningsaktivitet.
Ett lagarbete inom ett enda protein
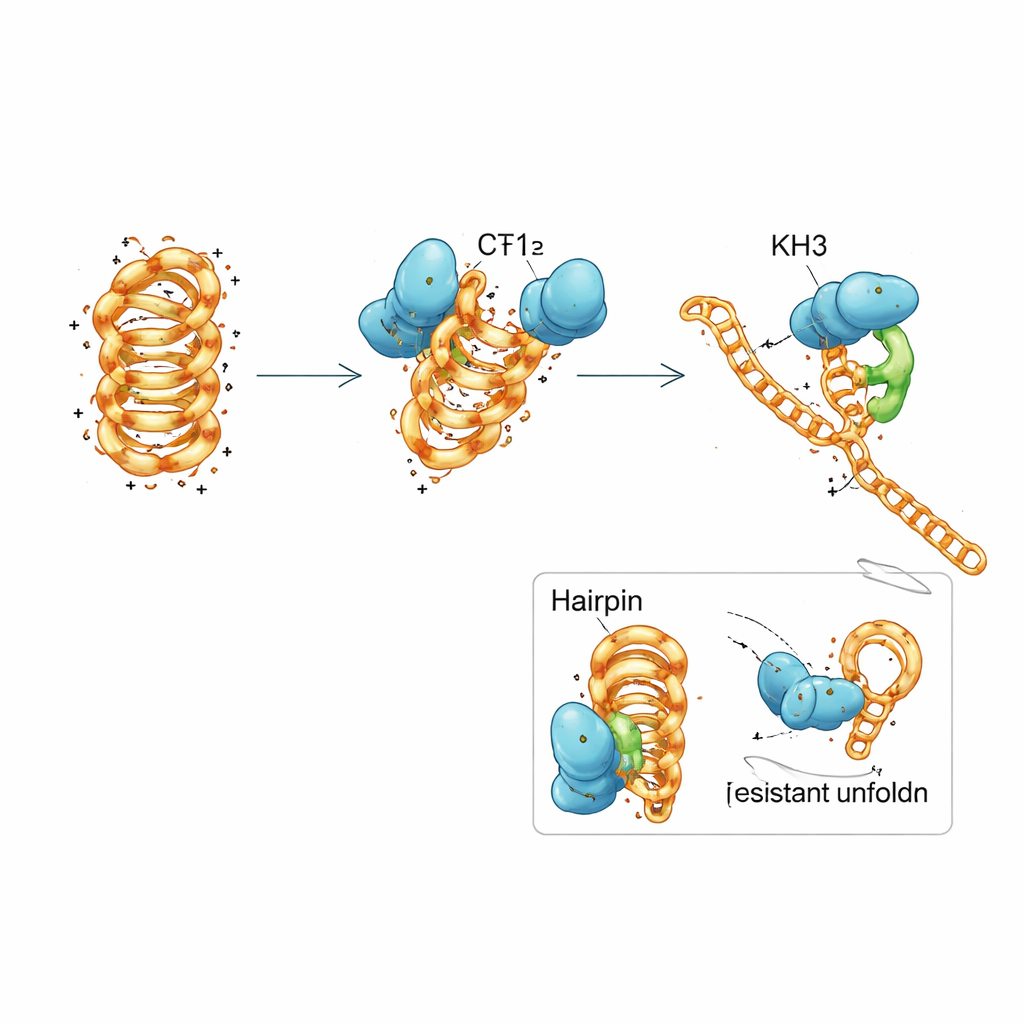
PCBP1 är uppbyggt av tre upprepade moduler kallade KH-domäner, vanliga motiv som fångar korta nukleinsyrasekvenser. Teamet dissekerade PCBP1 i delar och upptäckte att ingen enskild KH-domän fullt ut kunde efterlikna hela proteinets beteende. De två första domänerna tillsammans kunde fästa både vid veckat och uppveckat DNA och knuffa i-motivet mot en mindre stabil form, men de främjade bara långsamt en fullständig uppveckning. Den tredje domänen ensam band knappt alls. När alla tre domäner var närvarande och fick samverka återtog proteinet sin starka preferens för veckade i-motiv och sin effektiva förmåga att veckla upp dem. Detaljerade biofysiska mätningar och datorsimuleringar föreslog en stegvis mekanism: KH1 och KH2 först dockar på flexibla loopregioner av i-motivet och stör delvis ut utvalda baspar, vilket sedan tillåter KH3 att engagera sig och driva strukturen till ett öppet, replikationsredo tillstånd.
Håller cellcykeln i fas
Studien visar också att denna molekylära koreografi har betydelse för cellbeteende. När forskarna minskade PCBP1-nivåerna i humana celler uppträdde fler i-motivstrukturer vid specifika genpromotorer, markörer för DNAskada ökade och celler stannade vid den kritiska G1/S-kontrollpunkten—ögonblicket precis före att DNA-replikation börjar. Under normala förhållanden når PCBP1:s närvaro vid i-motivbildande regioner sin topp kring denna kontrollpunkt, för att sedan minska när S-fasen startar och i-motiven löses upp. Denna tidpunkt tyder på att PCBP1 fungerar som en vårdare: det binder och vecklar upp specifika i-motiv vid precis rätt tidpunkt så att DNA-replikationen kan fortgå smidigt och genomet förbli intakt. För en lekmannaläsare är budskapet att ovanliga DNA-veck kan fungera som tillfälliga vägspärrar, och PCBP1 är ett av de specialiserade verktyg cellen använder för att avlägsna dem och därigenom hjälpa till att förebygga fel som annars skulle kunna bidra till cancer.
Citering: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Nyckelord: i-motiv-DNA, PCBP1-protein, cellcykelns kontrollpunkt, genomstabilitet, DNA sekundärstruktur