Clear Sky Science · sv
Kemiskt vägledd enkelcells-transkriptomik avslöjar sulfotransferasmedierad ombyggnad av scaffold i securinine-biosyntes
Varför en buskes kemi spelar roll
Securinega-alkaloider är potenta molekyler som finns i en liten prydnadsbuske, Flueggea suffruticosa, länge studerad för sin potential vid behandling av cancer och neurologiska sjukdomar. Men fram till nu har ingen riktigt förstått hur växten faktiskt bygger dessa intrikata föreningar. Denna studie kombinerar modern enkelcells-gengläsning med väl avvägda kemiska experiment för att steg för steg avslöja hur växten sätter samman och omformar dessa molekyler — och upptäcker på vägen en överraskande ny roll för en vanlig enzymtyp. 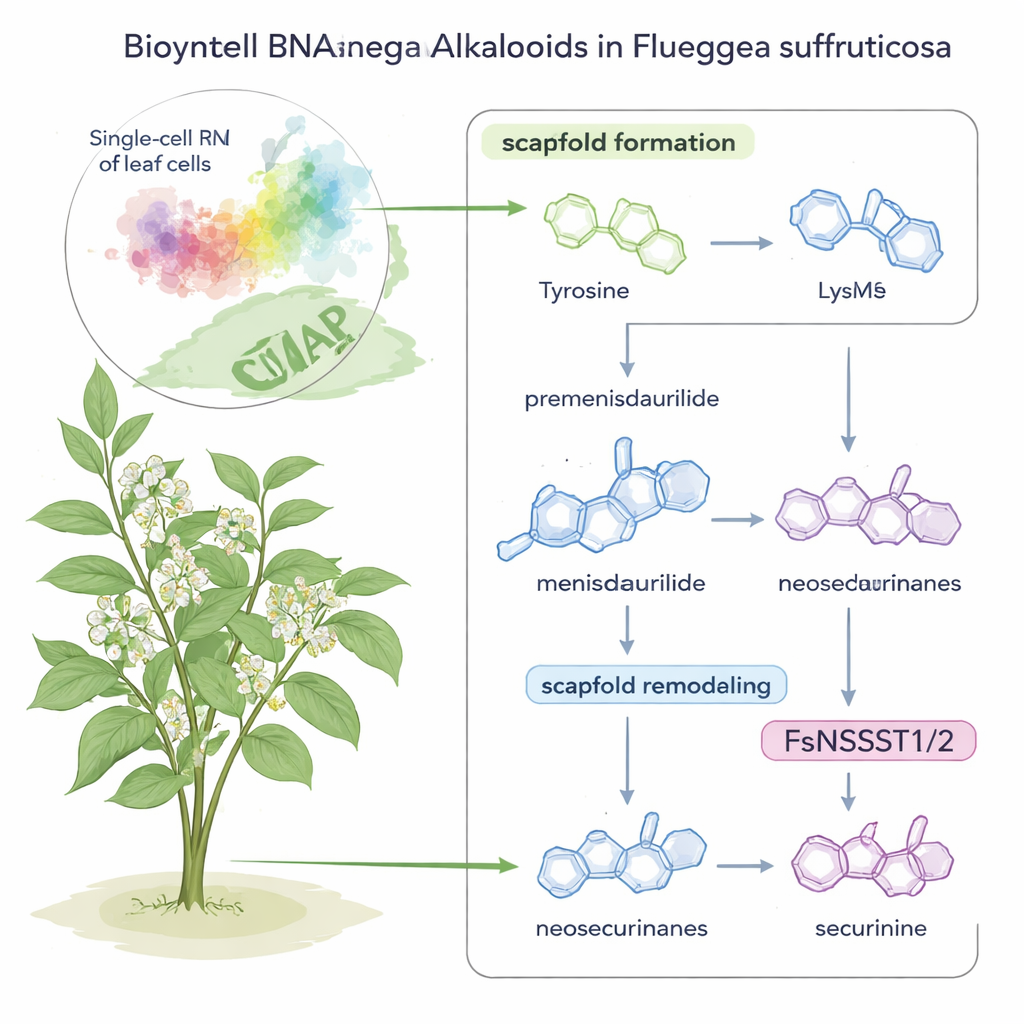
Byggstenar från vanliga aminosyror
Berättelsen börjar med två välkända näringsämnen: aminosyrorna tyrosin och lysin. I F. suffruticosa omvandlas tyrosin till en ovanlig ringformad molekyl kallad premenisdaurilid, som sedan reduceras till menisdaurilid av ett nyupptäckt enzym som författarna namnger FsMS (för “menisdaurilide synthase”). Parallellt omvandlas lysin till en liten kvävehaltig ring, 1-piperidein, av ett annat enzym, FsPS, som upptäcktes i tidigare arbete. När menisdaurilid och 1-piperidein möts i svagt basiska, vattenliknande förhållanden förenas de spontant för att bilda “neosecurinane”-alkaloider — intermediära strukturer på vägen mot de slutliga medicinskt intressanta föreningarna.
Att se kemin ske i realtid
För att bekräfta att dessa föreslagna steg inte bara är teoretiska syntetiserade teamet versioner av de misstänkta intermediärerna märkta med tunga kolatomer. Genom att mata dessa märkta molekyler till växtextrakt kunde forskarna spåra exakt var atomerna hamnade. De såg att märkt menisdaurilid omvandlades till märkta neosecurinaner, och dessa vidare till de kända alkaloiderna allosecurinine och securinine, vilket bekräftar att dessa intermediär verkligen ingår i den naturliga vägen. Viktigt är att några av de nyckelreaktioner som bildar ringarna också skedde i kokta extrakt, vilket visar att delar av rutten kan fortgå utan enzymer, drivna enbart av molekylernas kemi.
Zooma in på rätt celler
Att veta vilka molekyler som dyker upp var är bara halva pusslet; att identifiera generna som styr varje steg kräver att man vet vilka celler som utför arbetet. Forskarna sekvenserade RNA från tusentals individuella celler från F. suffruticosa-blad och klustrade dem i distinkta celltyper baserat på genaktivitetsmönster. Ett kluster, kopplat till bladsystemets vener, stack ut: det uttryckte starkt de kända väggenesgenerna och många enzymer kopplade till tyrosin-, lysin- och svavelmetabolism. Genom att undersöka vilka gener som varierade i takt med väggenzymerna inom detta kluster fokuserade teamet in på FsMS och två sulfotransferaser, FsNSST1 och FsNSST2, som starka kandidater för de saknade stegen. 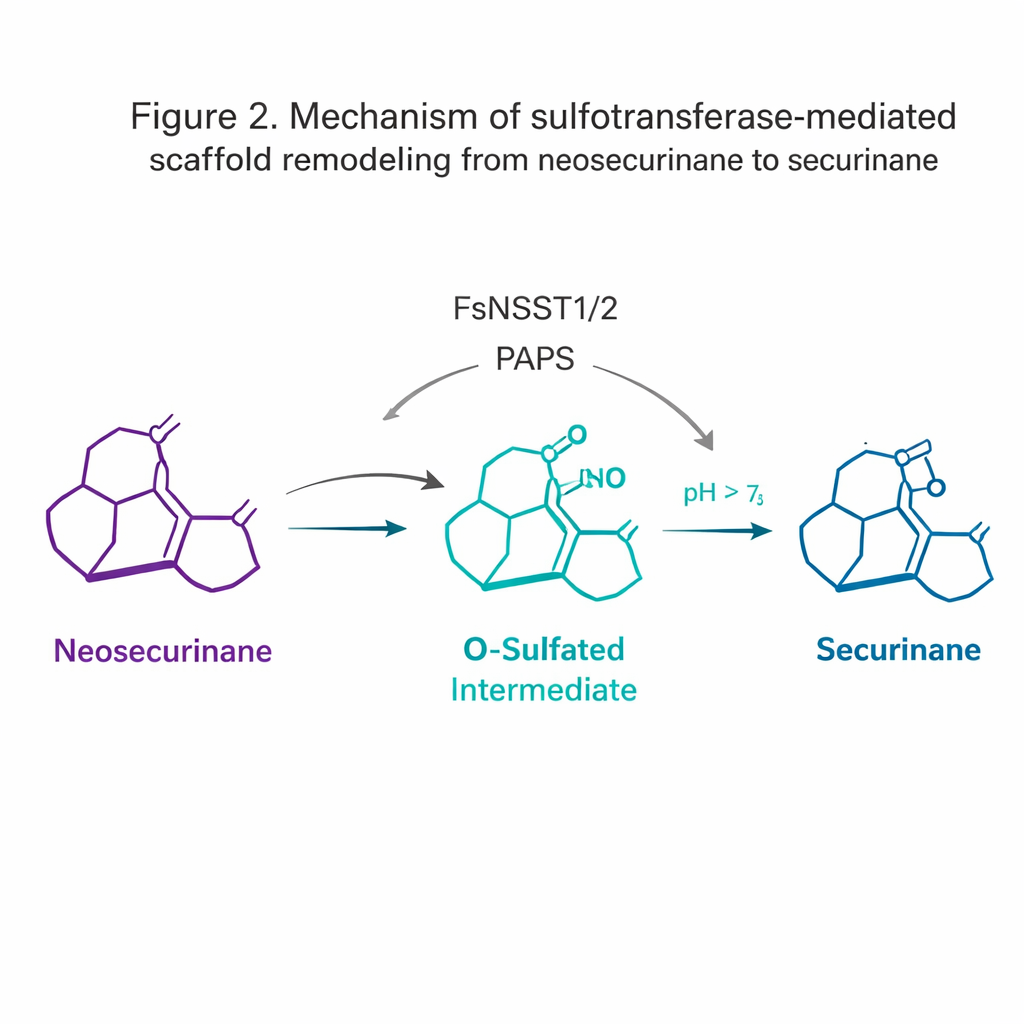
Ett enzym som bygger om det molekylära skelettet
Den mest överraskande upptäckten kom från sulfotransferaserna. Sulfotransferaser fäster vanligtvis en sulfatgrupp på molekyler för att öka deras löslighet eller markera dem för nedbrytning. Här agerar FsNSST1 och FsNSST2 istället som omkopplare: de fäster sulfat på neosecurinane‑scaffolden, och förvandlar den tillfälligt till en högenergetisk ”O‑sulfaterad” intermediär. Denna aktiverade form genomgår sedan en spontan 1,2-amine‑förskjutning — en liten omarrangemang där en kväveatom migrerar — och omvandlar det [2.2.2] bicykliska ”neosecurinane”-ramverket till det [3.2.1] ”securinane”-ramverket. Detta subtila omformningssteg ger upphov till den karakteristiska tetracykliska kärnan hos de biologiskt aktiva alkaloiderna.
Varför denna väg är viktig
För en icke‑specialist är huvudbudskapet att växten bygger securinega-alkaloider i två huvudfaser: först bygger den ett preliminärt ringsystem från vanliga aminosyror; sedan kemiskt omformar den detta scaffold till en mer komplex form med hjälp av en sulfat‑"trigger." Genom att kombinera cell-för-cell genprofilering med isotopmärkta kemiexperiment kartlägger författarna denna väg i detalj och visar att sulfotransferaser — enzymer som återfinns i alla livsformer — kan mer än bara dekorera molekyler; de kan initiera omfattande omarrangemang av deras form. Att förstå denna väg klargör inte bara hur en lovande klass läkemedelsliknande molekyler skapas i naturen, utan öppnar också möjligheter att konstruera grödor eller mikrober för att producera nya securinega‑inspirerade läkemedel.
Citering: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Nyckelord: växtalkaloider, biosyntes, enkelcells‑transkriptomik, sulfotransferas, naturproduktkemi