Clear Sky Science · sv
Den funktionella landskapen för alternativ splitsning vid hematopoetisk linjeåtagande
Hur små genredigeringar formar vårt blod
Varje sekund bildar din kropp miljontals nya blodceller. Bakom detta tysta under ligger ett molekylärt redigeringssystem som kan klippa och klistra delar av genetiska budskap på olika sätt och därigenom skapa något olika versioner av samma protein. Denna studie undersöker hur den redigeringsprocessen, kallad alternativ splitsning, hjälper omogna stamceller att utvecklas till röda blodkroppar, vita blodkroppar eller andra blodcellstyper — och vad som händer när en enskild redigerad del saknas.
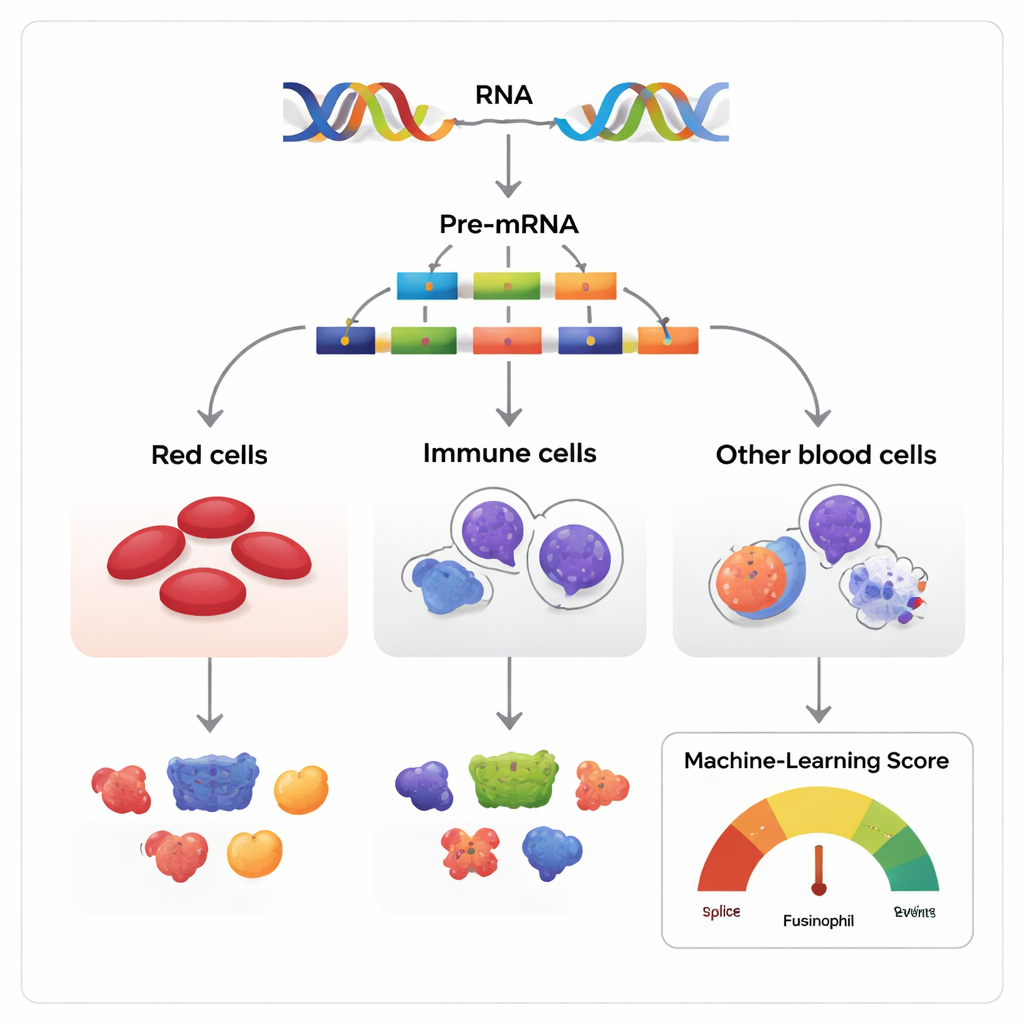
Många versioner från samma genetiska manus
Gener beskrivs ofta som ritningar, men i verkligheten är de mer som manus som kan omarrangeras. När en gen avläses innehåller den initiala RNA-kopian segment som kallas exoner som antingen kan behållas eller hoppas över innan det slutliga budskapet blir ett protein. Författarna studerade denna process, känd som exon skipping, i blodbildande vävnader hos människor, möss och flera andra ryggradsdjur. De sammanställde mer än 270 RNA-dataset som tillsammans följer blodstam- och progenitorceller när de mognar till tre huvudfamiljer: erytroida celler som producerar röda blodkroppar, myeloida celler som bekämpar infektioner, och lymfoida celler som producerar antikroppar.
Prioritering av vilka splitsningsförändringar som verkligen spelar roll
Eftersom de flesta gener med flera exoner kan splitsas på många sätt är den centrala utmaningen att skilja ofarliga variationer från dem som faktiskt påverkar cellens öde. Forskarna byggde en maskininlärningsmodell, kallad Functional AS Score (FAScore), för att angripa detta problem. För varje exon-skipping-händelse beaktar modellen 19 informationsdelar, såsom hur starkt dess användning ändras under celldifferentiering, hur väl den omgivande DNAn är bevarad över arter, om den förändrar kända proteindomäner, och om den innehåller platser för kemiska modifieringar av proteinet. Algoritmen, tränad med en positiv–oetiketterad strategi och en random forest-klassificerare, ger ett poängvärde mellan 0 och 1 som indikerar hur sannolikt det är att en given splitsningshändelse har en funktionell påverkan.
Att hitta konserverade, linjespecifika strömbrytare
Genom att tillämpa FAScore på tiotusentals exon-skipping-händelser klassificerade teamet dem som sannolikt funktionella, icke-funktionella eller osäkra. Händelser som förutsågs vara funktionella återfanns oftare i proteinregioner viktiga för interaktioner, i evolutionärt bevarade sekvenser och i segment som bär kemiska etiketter som fosforylering eller SUMOylering. Många av dessa händelser var också aktiva endast i specifika blodlinjer eller under fostrets blodbildning, vilket tyder på att de fungerar som finjusterade strömbrytare i särskilda utvecklingsfönster. Studien visade vidare att några av de äldsta splitsningshändelserna — de som delas över ryggradsdjur i hundratals miljoner år — särskilt sannolikt är funktionella, vilket speglar hur äldre gener tenderar att bära centrala biologiska roller.
Experimentellt bevis: att ställa om blodcellernas utfall
För att pröva modellens förutsägelser valde författarna flera högt rankade exoner i gener aktiva i olika blodlinjer och tog bort dessa exoner i mössens blodstam- och progenitorceller med CRISPR. Resultaten stämde överens med modellens förväntningar: borttagning av vissa exoner i generna KLF6 och SSBP3 försämrade bildningen av myeloida kolonier utan att skada produktionen av röda blodkroppar, medan borttagning av exoner i EPB41L1 och TBC1D23 ändrade erytroid koloniutveckling. Särskilt reducerade hopp över exon 15 i TBC1D23 produktionen av förstadier till röda blodkroppar hos möss och zebrafisk, vilket ledde till färre cirkulerande röda celler och lägre hemoglobinnivåer, medan vita blodkroppar i stort sett var opåverkade.
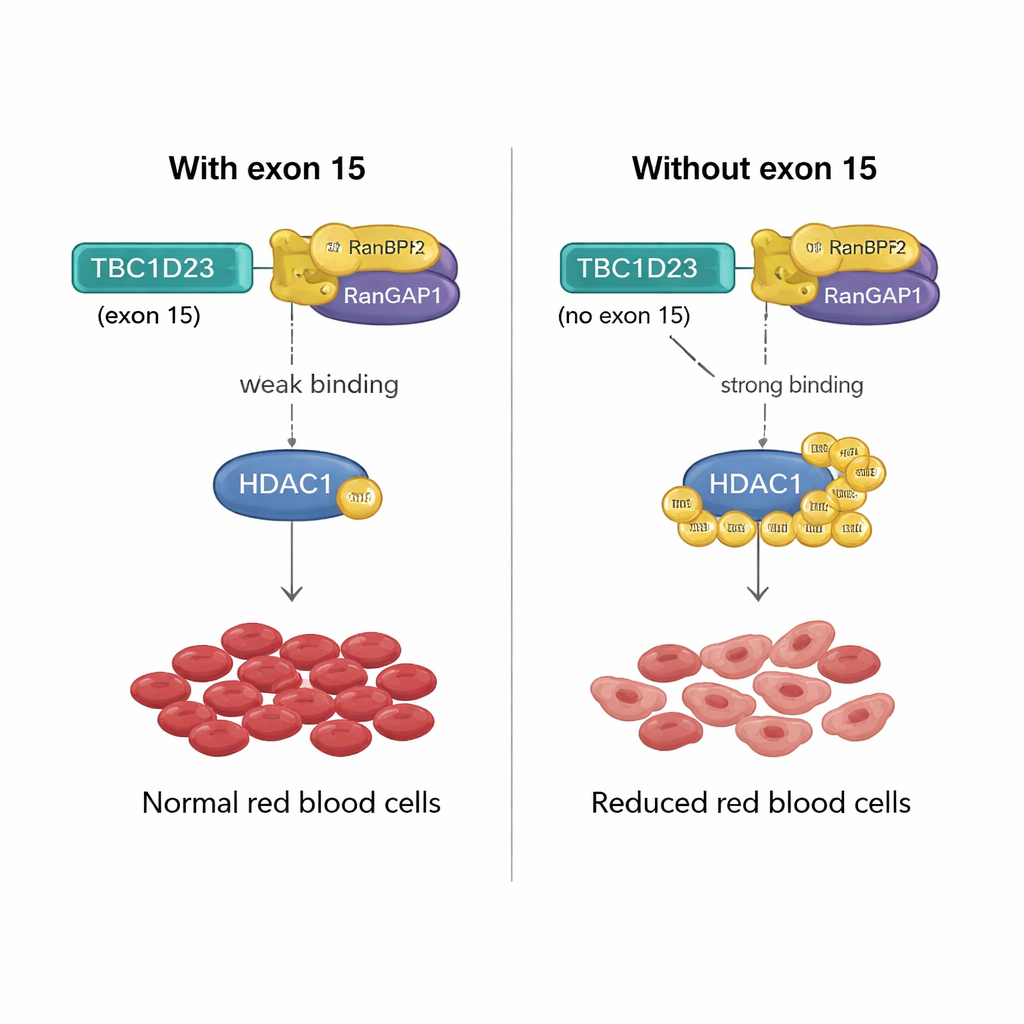
En molekylär spak för produktion av röda blodkroppar
Hur kan en 15 aminosyra lång sträcka kodad av exon 15 i TBC1D23 ha en sådan effekt? Teamet fann att inkludering av detta exon försvagar TBC1D23:s bindning till ett proteinpar kallat RANBP2/RANGAP1, som samarbetar för att fästa SUMO-taggar på andra proteiner. Utan exon 15 binder TBC1D23 detta par starkare, vilket ökar SUMOyleringen av ett nyckelenzym, HDAC1. Denna ökade märkning ändrar aktiviteten hos många transkriptionsfaktorer — huvudregulatorer av genuttryck — och rubbar de genprogram som behövs för korrekt mognad av röda blodkroppar. När forskarna konstruerade en version av HDAC1 som inte kan SUMO- märkas på två avgörande positioner återställdes bildningen av röda celler i celler som saknade TBC1D23 exon 15, vilket bekräftar att denna kemiska märkning är det kritiska steget.
Varför detta betyder något för hälsa och framtida behandlingar
För en icke-specialist är budskapet i detta arbete att inte alla genetiska förändringar är likadana: ibland ligger skillnaden mellan friskt blod och anemi i om ett litet segment av en gen behålls eller hoppas över i det slutliga budskapet. Genom att kombinera storskaliga RNA-data med ett sofistikerat poängsystem ger studien en färdplan för att upptäcka vilka splice-varianter som mest sannolikt påverkar hur stamceller väljer sina öden. Detta tillvägagångssätt fördjupar inte bara vår förståelse av hur blodceller bildas vid hälsa och sjukdom, utan erbjuder också en generell strategi för att identifiera viktiga splitsningshändelser i andra organ, vilket potentiellt kan vägleda framtida genbaserade terapier och precisionsbehandlingar.
Citering: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
Nyckelord: alternativ splitsning, hematopoes, maskininlärning, röda blodkroppar, genreglering