Clear Sky Science · sv
Strukturell grund för transkriptionsreglering av celldelningsregulatorn MraZ i Mycoplasma genitalium
Hur en pytteliten bakterie styr när den delar sig
Varje levande cell måste bestämma när den ska dela sig i två, och det beslutet kan vara skillnaden mellan hälsosam tillväxt och okontrollerad infektion. Denna studie granskar en av de enklaste kända bakterierna, Mycoplasma genitalium, för att visa i atomär detalj hur ett enda protein, kallat MraZ, hakar fast vid DNA och slår av eller på viktiga celldelningsgener. Genom att förstå detta minimalistiska styrsystem hoppas forskare kunna avslöja generella regler för bakteriell tillväxt som en dag kan inspirera nya typer av antibiotika eller syntetiska ”minimiceller”.
En avskalad cell med stora lärdomar
Mycoplasma genitalium är känd för sitt pyttelilla genom: bara en bråkdel av DNA:t som finns i vanliga bakterier som E. coli. Denna lilla storlek gör den till en kraftfull modell för att klargöra vilka gener och kontrollsystem som verkligen är nödvändiga för liv. Många bakterier håller sina gener för celldelning och cellvägg tillsammans i ett block som kallas dcw-klustret. I vägglösa mykoplasmor är de flesta av dessa gener borta, men ett fåtal finns kvar, inklusive mraZ längst fram i klustret. MraZ fungerar som en trafikpolis som kontrollerar aktiviteten hos sina närbelägna gener, vilka i sin tur påverkar hur och när cellen delar sig.
Ett upprepat DNA-mönster som en kontrollväxel
Strax uppströms om mraZ-genen fann forskarna ett starkt bevarat DNA-segment som fungerar som en dockningsstation för MraZ-proteinet. Denna region innehåller fyra korta upprepade segment, eller ”boxar”, som har nästan identisk sekvens över många bakteriearter. Genom att noggrant mutera en, två eller flera av dessa boxar och sedan mäta hur hårt MraZ fortfarande kunde binda DNA visade teamet att proteinet binder kooperativt: varje box bidrar till att stärka det övergripande greppet. Reporterexperiment med en fluorescerande markör bekräftade att ju mer dessa boxar stördes, desto mindre effektivt kunde MraZ repressa genaktiviteten, vilket understryker deras betydelse som en fint avvägd kontrollpanel. 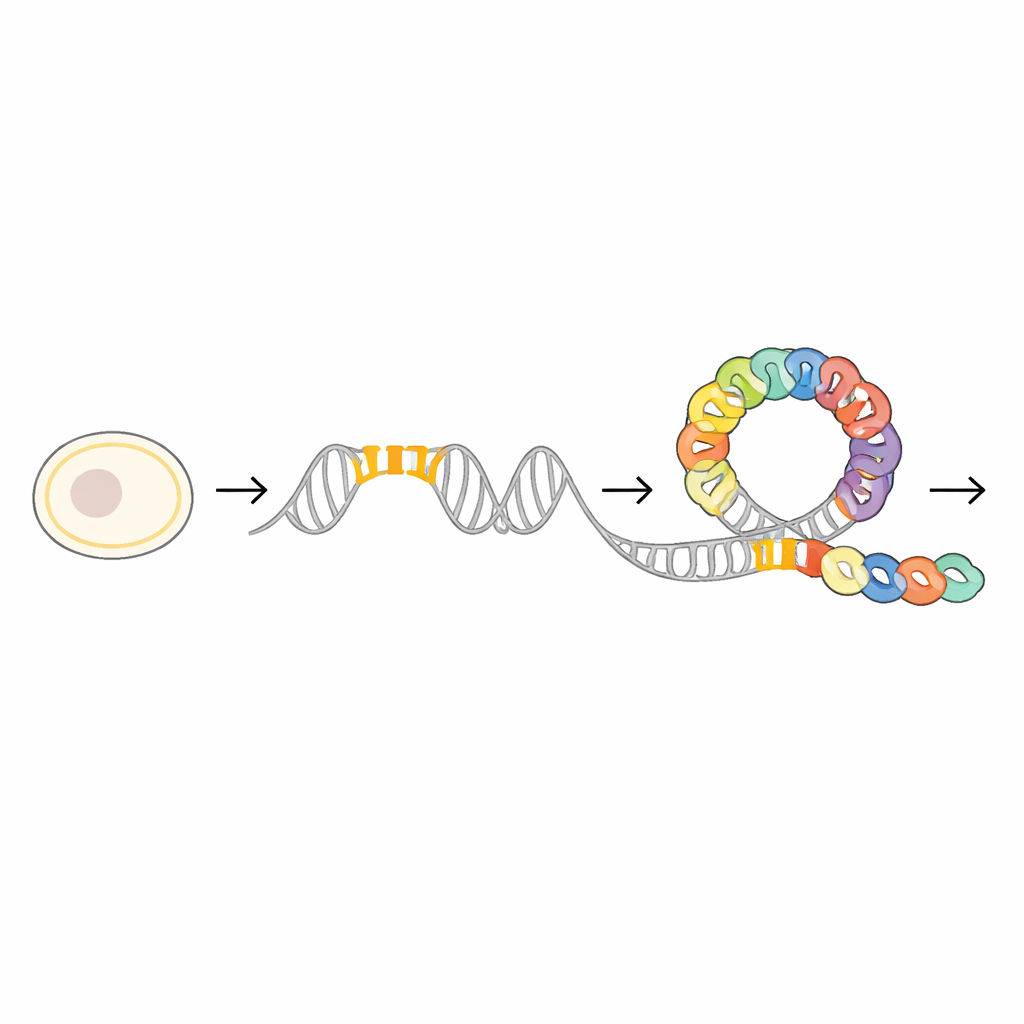
En ringformad proteinstruktur som öppnar sig för att omfamna DNA
För att se hur denna kontrollpanel fungerar på atomär nivå använde forskarna kryo-elektronmikroskopi och röntgenkristallografi för att lösa flera tredimensionella strukturer av MraZ både ensam och bunden till DNA. Isolerade MraZ-molekyler sluter sig till ringlika assemblage bestående av åtta eller nio identiska subenheter. Dessa ringar har en distinkt ”vagga-lik” yta formad av ett litet beta-skikt, olikt de spiralformade helixar som ofta ses i DNA-bindande proteiner. När MraZ möter sitt fyraboxiga DNA-segment sätter sig ringen inte bara ovanpå helixen; istället flexar den upp och omarrangerar sig så att fyra av dess subenheter radar upp längs DNA:t, var och en omsluter en box i major groove.
Nyckelkontaktpunkter som läser DNA-koden
De högupplösta strukturerna visade att varje DNA-kontakterande subenhet använder tre positivt laddade sidokedjor—specifika punkter på proteinytan—för att läsa DNA-sekvensen. Dessa kemiska ”fingrar” sträcker sig in i dubbelhelixens fåra och bildar precisa vätebindningar med särskilda baspar i de bevarade boxarna. När forskarna ändrade någon av dessa tre restpositioner förlorade MraZ till stor del förmågan att binda DNA och att slå av testreportergenen. Ytterligare kontakter med DNA-ryggraden hjälper till att stabilisera komplexet men är mindre sekvensspecifika. Tillsammans visar dessa fynd hur MraZ kombinerar ett högspecialiserat läshuvud med en flexibel multienhetskropp för att känna igen sitt målområde. 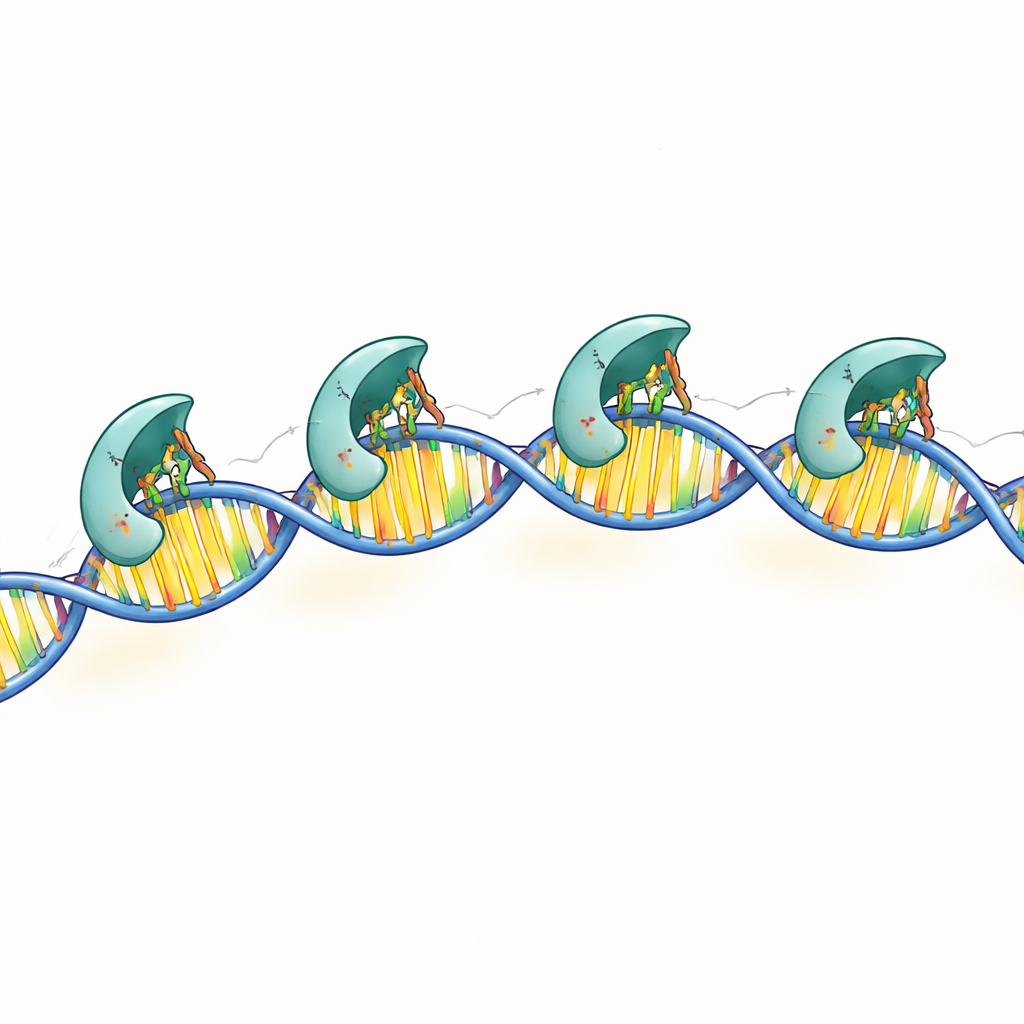
Oligomerer som ställer in kontrollens styrka
Eftersom MraZ bildar ringar och andra multienhetsformer frågade teamet om denna klustring är nödvändig för DNA-bindning eller bara finjusterar den. Genom att konstruera en version av MraZ som inte längre kunde montera sig till ringar fann de att proteinet fortfarande band till fyraboxsekvensen, men med svagare affinitet. Denna monomera form hade särskilt svårt när avståndet mellan boxarna ändrades, vilket tyder på att det fullständiga oligomeret hjälper till att bädda över och justera avlägsna boxar, och höjer den lokala koncentrationen av bindningsmotif längs DNA:t. Författarna föreslår en dynamisk modell där MraZ växlar mellan en sluten ring och en öppen, DNA-engagerad form och använder sitt monteringsläge som en ratt för att reglera hur hårt det klämmer ner på promotorn.
Vad detta betyder för bakterier och vidare
Enkelt uttryckt förklarar detta arbete hur ett litet protein i en minimal bakterie fångar ett upprepat mönster på DNA och använder det som en huvudbrytare för celldelningsgener. Kombinationen av ett vagga-likt läshuvud och en flexibel ringkropp gör att MraZ kan känna igen sitt mål med hög precision samtidigt som det förblir anpassningsbart till olika DNA-arrangemang. Eftersom liknande proteiner och DNA-motiv förekommer i många bakterier är mekanismen som beskrivs här troligen en gemensam strategi för att samordna tillväxt och delning. Insikter från detta avskalade system kan hjälpa forskare att designa strömlinjeformade genetiska kretsar i syntetiska celler och, på längre sikt, kunna bidra till nya sätt att störa bakteriell tillväxt i sjukdomssammanhang.
Citering: Sánchez-Alba, L., Varejão, N., Durand, A. et al. Structural basis for transcriptional regulation by the cell division regulator MraZ in Mycoplasma genitalium. Nat Commun 17, 2132 (2026). https://doi.org/10.1038/s41467-026-68809-2
Nyckelord: bakteriell celldelning, DNA–proteinteraction, transkriptionell reglering, kryo-elektronmikroskopi, Mycoplasma genitalium