Clear Sky Science · sv
YL1004 är en hämmare av SARS‑CoV‑2:s papain‑liknande proteas med immunmodulerande och antivirala effekter hos möss
Varför en ny COVID‑19‑tablett fortfarande spelar roll
Världen har vacciner och flera antivirala tabletter mot COVID‑19, men coronaviruset fortsätter att utvecklas, undviker immunitet och kan bli resistent mot befintliga läkemedel. Denna studie presenterar YL1004, ett experimentellt oralt läkemedel som riktar sig mot en annan sårbar punkt i SARS‑CoV‑2 och samtidigt hjälper kroppens egna försvar att återhämta sig. I möss minskade det inte bara virusnivåerna från flera varianter, inklusive en läkemedelsresistent stam, utan förhindrade också död vid annars dödliga infektioner.
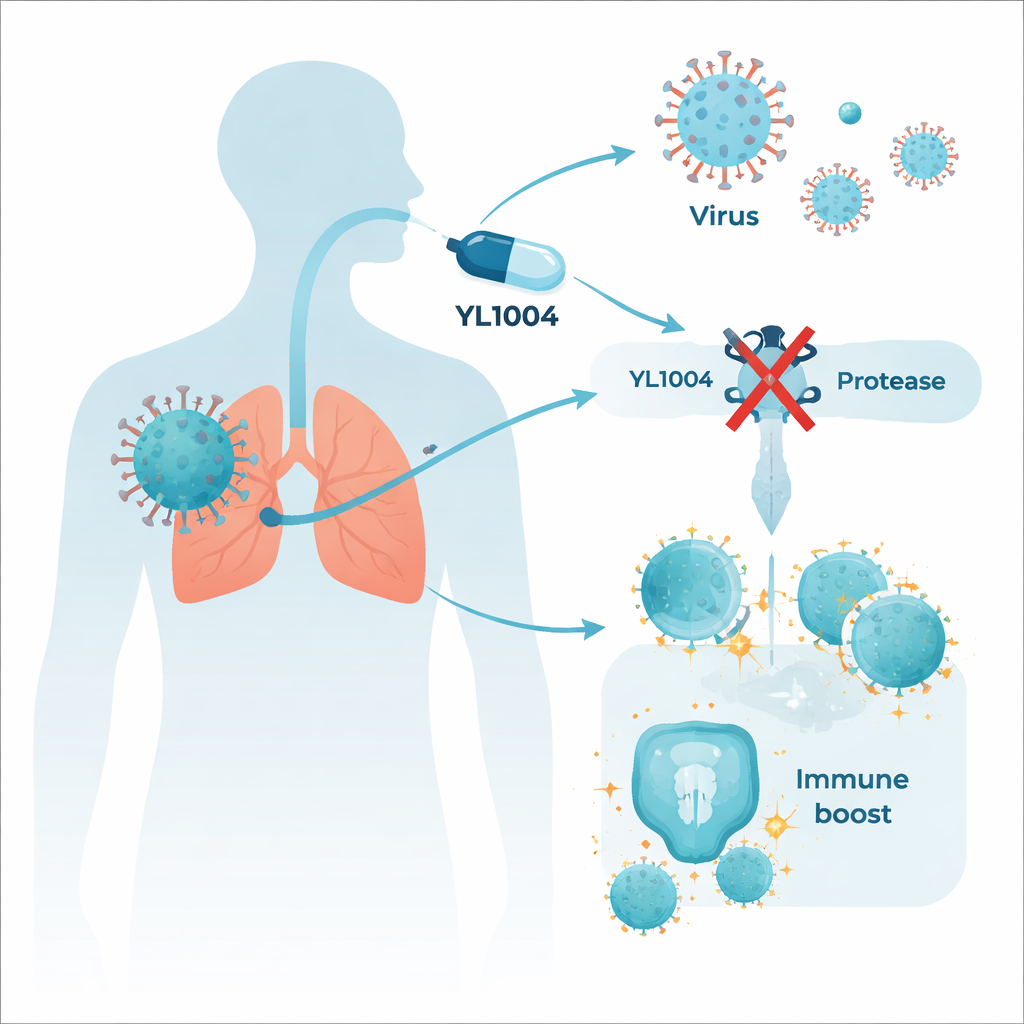
Ett viralt verktyg med dubbel funktion
YL1004 är utformat för att blockera ett viralt enzym kallat papain‑liknande proteas, eller PLpro. Detta enzym fungerar som molekylära saxar: det klyver långa virala proteiner till arbetande delar som viruset behöver för att kopiera sig. Men PLpro har en andra, mer slug roll. Det avlägsnar små kemiska märken från våra egna immunproteiner, vilket effektivt dämpar alarmsignaler som normalt skulle kalla på immunceller. På grund av denna dubbla funktion kan hämning av PLpro både bromsa virusreplikation och återställa tidiga antivirala försvar.
Att konstruera ett precist molekylärt lås
Forskarna började med att screena cirka 35 000 föreningar för deras förmåga att störa PLpro i ett provrörs‑test. De fann en lovande "tricyklisk" kemisk form och förfinade den systematiskt, med vägledning från jämförelser med äldre PLpro-hämmare. Dussintals varianter togs fram, finjusterades och testades för potens, säkerhet i celler och hur de uppträdde i djur. YL1004 framträdde som den bästa kandidaten: den hämmade PLpro kraftigt vid mycket låga koncentrationer, visade låg toxicitet i flera mänskliga och apcellinjer, och hade gynnsamma ”läkemedelslika” egenskaper såsom god stabilitet i levertester, acceptabel löslighet och förmåga att effektivt passera celllager.
Att se hur läkemedlet greppar viruset
För att förstå varför YL1004 fungerar så väl löste teamet en tredimensionell kristallstruktur av läkemedlet bundet till PLpro. Bilderna visade att YL1004 placerar sig i en ficka nära en flexibel slinga på enzymets yta och bildar flera täta kontakter. Delar av molekylen bildar vätebindningar—specifika riktade attraktioner—med flera aminosyror, medan andra ringformade regioner skapar ett brett hydrofobt, det vill säga vattenavvisande, gränssnitt som låser läkemedlet på plats. Jämfört med en klassisk PLpro-hämmare gör YL1004 fler och starkare kontakter, vilket förklarar dess förbättrade grepp. Strukturella jämförelser med liknande mänskliga enzymer visade också varför YL1004 skonar dem, vilket minskar risken för oönskade biverkningar utanför målet.
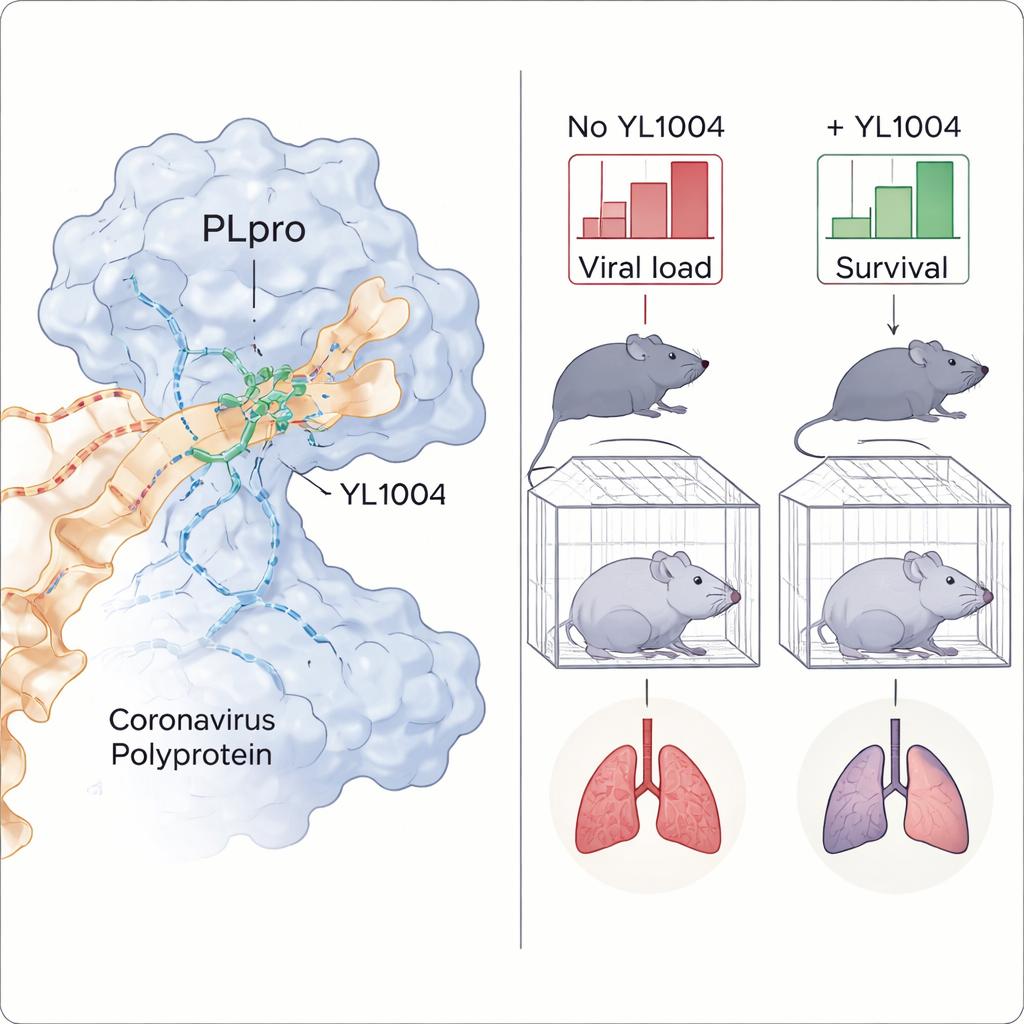
Stärker antivirala försvar och slår tillbaka varianter
I celler återställde YL1004 enzymets avlägsnande av reglerande märken från immunsignalerande proteiner, och återaktiverade därmed viktiga varningsvägar såsom interferon‑signalering och NF‑κB, vilka är centrala för tidigt antiviralt försvar. Genom genomeomfattande RNA‑analyser bekräftades att uttryck av PLpro normalt undertrycker många immunsystem‑relaterade och stress‑responsgener, medan tillsats av YL1004 slog på dessa vägar igen. När läkemedlet testades mot levande virus i människoliknande lungceller minskade det kraftigt både viral genetisk material och infektiva partiklar från den ursprungliga SARS‑CoV‑2‑stammen och flera större varianter, inklusive Delta och Omicron‑sublinjerna JN.1 och KP.3. Anmärkningsvärt är att det förblev aktivt mot ett virus som konstruerats för att vara resistent mot nirmatrelvir, huvudkomponenten i den antivirala tabletten Paxlovid.
Skyddade infekterade möss från dödlig sjukdom
De mest påtagliga resultaten kom från experiment i genetiskt modifierade möss som är mycket känsliga för SARS‑CoV‑2. Efter oral dosering nådde YL1004 blodnivåer som var tillräckligt höga, och varade tillräckligt länge, för att motsvara eller överstiga de nivåer som krävs för att blockera viruset i cellkultur. När möss infekterades med en Omicron JN.1‑stam sänkte behandlingen avsevärt virusmängder i näsa och lungor och minskade vävnadsskador och färgning för virala proteiner i lungsektioner. I ett tuffare test, där möss utmanades med en dödlig dos av Delta‑varianten, behandlades de med antingen YL1004 eller en jämförande PLpro-hämmare. Alla djur som fick YL1004 överlevde med mildare viktnedgång, medan de flesta obehandlade mössen dog, och den äldre föreningen presterade sämre.
Vad detta kan innebära för framtida COVID‑19‑vård
För icke‑specialister är slutsatsen att YL1004 är en nästa generations experimentell COVID‑19‑tablett som angriper viruset från två håll samtidigt: den blockerar ett nyckelenzym som viruset behöver för att föröka sig och lyfter bromsen som viruset sätter på vårt medfödda immunsystem. I laboratorie‑ och mössstudier fungerade den mot flera varianter, inklusive en som kringgår ett befintligt oralt läkemedel, och visade lovande säkerhets‑ och doseringsegenskaper. Även om mänskliga prövningar fortfarande krävs kan YL1004 och liknande PLpro-hämmare bli värdefulla tillskott i vår verktygslåda—särskilt för hög‑riskpatienter och inför framtida varianter som urholkar effekten av nuvarande behandlingar.
Citering: Nan, J., Shuai, H., Qiao, J. et al. YL1004 is a SARS-CoV-2 papain-like protease inhibitor with immunomodulatory and antiviral activity in mice. Nat Commun 17, 2035 (2026). https://doi.org/10.1038/s41467-026-68795-5
Nyckelord: SARS‑CoV‑2, COVID‑19 antivirala, papain‑liknande proteas, immunmodulation, läkemedelsresistens