Clear Sky Science · sv
Leverans av peptidkoacervat för att skapa stabila interaktionsnav i celler
Bygga nya ”arbetsstationer” inuti celler
Våra celler är fyllda med små arbetsplatser där viktiga uppgifter—som energiproduktion eller stressreaktioner—sker. Med tiden, eller vid sjukdom, kan dessa naturliga arbetsstationer svikta. Denna studie undersöker ett sätt att tillsätta helt nya ”interaktionsnav” i levande celler med hjälp av enkla, laboratorietillverkade droppar byggda av korta peptider. Dessa syntetiska nav kan fånga specifika proteiner, koncentrera dem och till och med bidra till att förstöra dem, vilket pekar på nya strategier för framtida behandlingar och cellteknik.
Varför celler behöver skräddarsydda arbetsytor
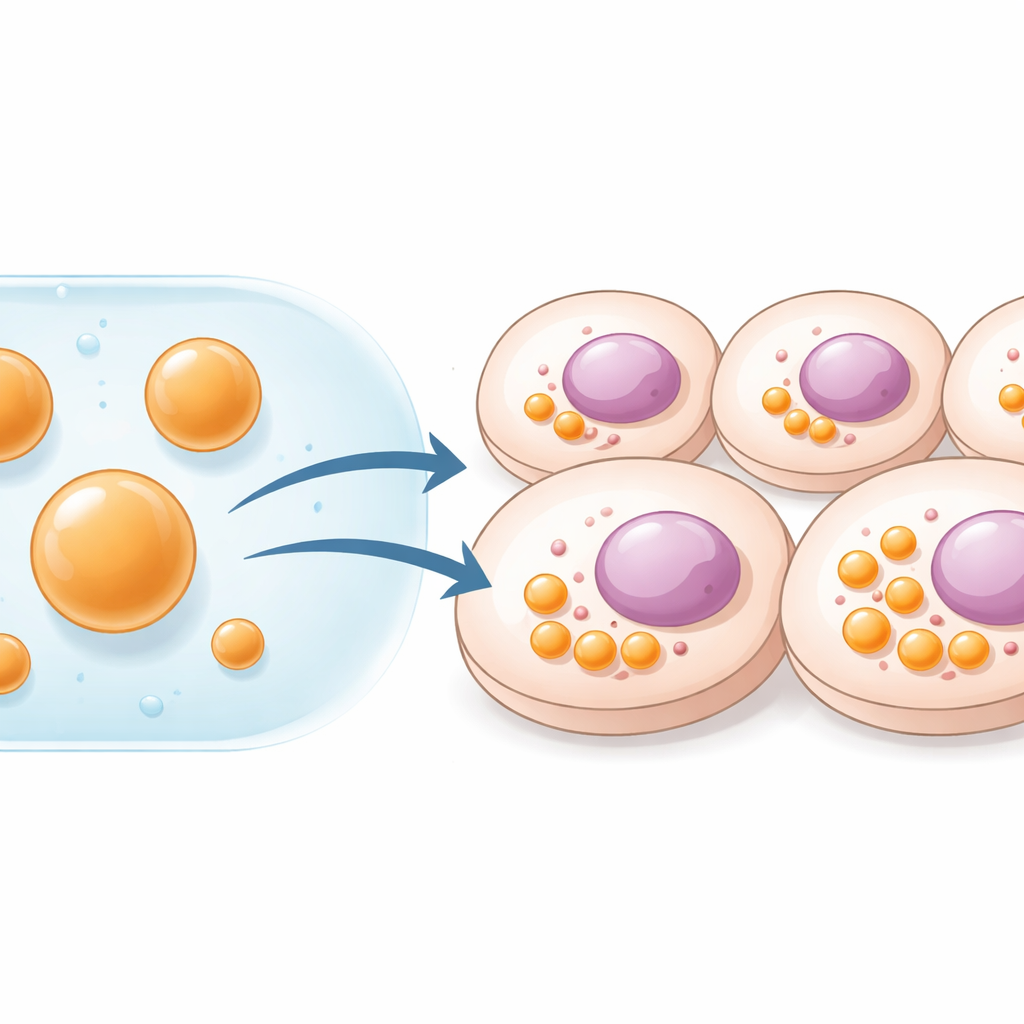
Celler håller ordning genom att separera olika uppgifter i distinkta fack. Vissa är omslutna av membraner, som mitokondrier; andra är mjukare, droppliknande strukturer som bildas när vissa proteiner och RNA klustrar ihop sig. Dessa flytande droppar, eller kondensat, fungerar som reaktionscentra som påskyndar eller stänger av specifika biokemiska vägar. Forskare har tidigare konstruerat sådana kompartment genom att tvinga celler att producera speciella scaffold-proteiner från införda gener. Även om det är kraftfullt kräver den metoden genleverans och begränsar hur mycket material cellen kan producera. Författarna till denna studie ville kringgå DNA helt och istället bygga färdiga kompartment utanför cellen, för att sedan leverera dem direkt som stabila, mikrometerstora droppar.
Peptiddroppar som bildar stabila nav
Gruppen arbetade med korta, oredigerade peptider kända som HBpep och en redox‑känslig variant, HBpep‑SA. Under svagt sura förhållanden förblir dessa peptider lösta, men när pH skiftas till nära‑fysiologiska nivåer—eller när temperatur sänks—separerar de i en fas och bildar mjuka, gel‑liknande droppar på cirka 1–5 mikrometer i diameter. Genom att justera peptidkoncentrationen kunde forskarna kontrollera både droppstorlek och antal. Med fluorescensteknik visade de att peptidmolekylerna inuti dropparna rör sig långsamt, vilket indikerar ett gellikt tillstånd som är tillräckligt robust för att klara utspädning och hantering. När dropparna tillsattes till odlingar av mänskliga cancerceller, musmelanomceller och primära mänskliga immunceller togs de effektivt upp och ackumulerades i cytoplasman. Större droppar, i synnerhet, förblev intakta i minst fem dagar och fungerade i praktiken som långlivade syntetiska organeller inuti levande celler.
Ladda och rikta navet
För att dessa nav ska vara användbara måste de hålla och organisera lastproteiner. Forskarna förbättrade först lastningen genom att fästa en kort HBpep‑härledd tagg på ett modellprotein, GFP. Denna tagg fick GFP att starkt partitionera in i dropparna och—intressant nog—koncentreras nära deras ytor, vilket skapade en kärna‑skalkonstruktion. Därefter inbäddade de nanobodies—kompakta, antikropps‑lika proteiner som binder tätt till utvalda mål—inne i dropparna. En GFP‑bindande nanobody gjorde att naven selektivt kunde fånga GFP både i provrör och inne i celler. Eftersom peptidgelen är relativt tät ackumulerades initialt det mesta av det fångade GFP vid droppens yta. Men när den interna strukturen delvis luckrades upp, antingen genom att ändra redoxförhållanden eller genom att underlätta dropparnas undflykt från omgivande endosomala membran, började GFP även tränga in i droppens inre. I celler ökade kemiska hjälpmedel som främjar endosomal flykt avsevärt andelen nav som framgångsrikt rekryterade sina mål.
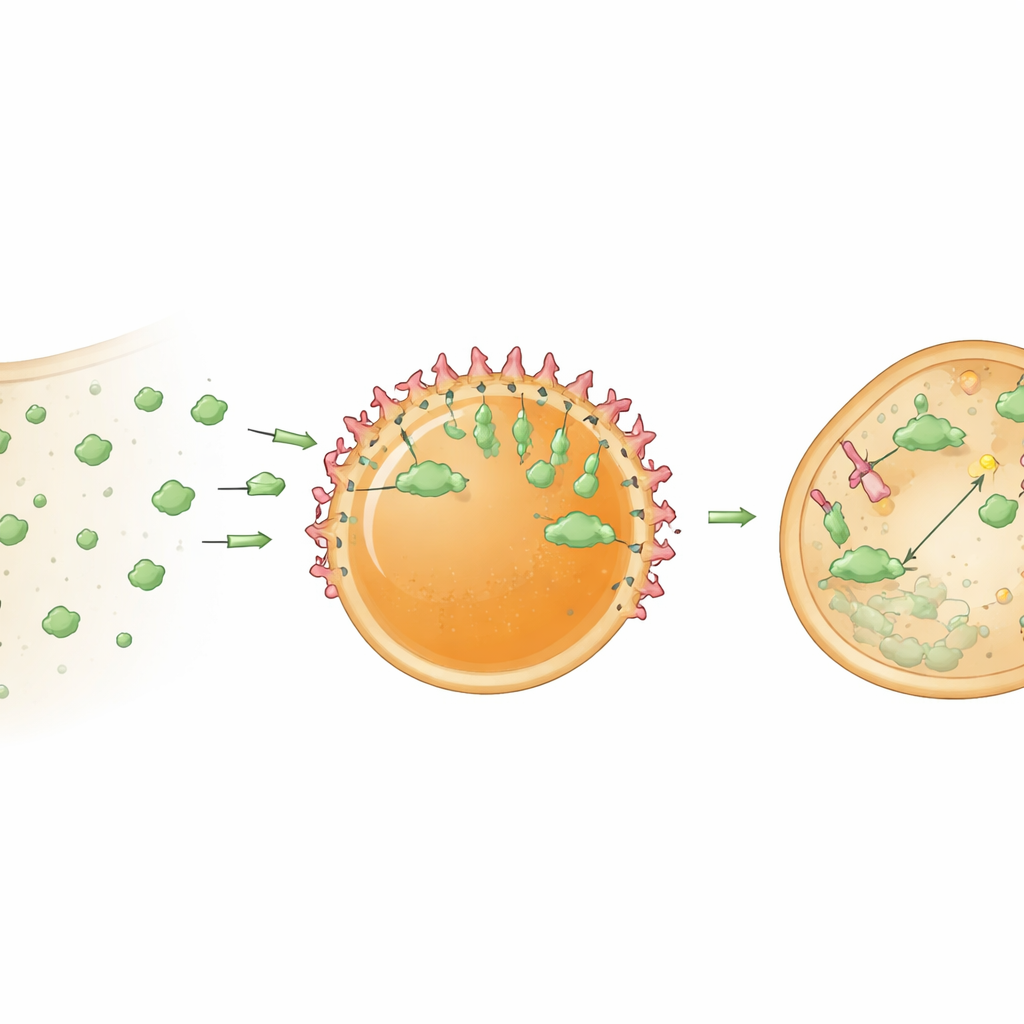
Förvandla nav till proteinförstörande maskiner
Författarna uppgraderade sedan dessa nav från passiva fällor till aktiva bearbetningscenter. De laddade dropparna med en bioPROTAC—ett fusionsprotein som kombinerar en målbindande nanobody med en del av en enzymadapter som flaggar proteiner för nedbrytning av cellens sopmaskineri. När dessa ”degradosom”‑droppar levererades in i celler som stabilt uttryckte GFP sjönk cytosoliskt GFP‑innehåll med cirka 78 procent inom ett dygn. Kontrollnav som endast innehöll nanobody sequestrerade GFP men sänkte inte dess totala nivå i någon större grad, vilket bekräftar att den starka minskningen berodde på riktad nedbrytning snarare än enkel fångst. Resultaten tyder på att klustring av bioPROTACs i ett koncentrerat mikro‑miljö gör dem mycket mer potenta än när de är fritt dispergerade i cytoplasman.
Vad detta kan innebära för framtida terapi
Enkelt uttryckt visar detta arbete att forskare kan framställa peptidbaserade droppar i ett provrör, packa dem med skräddarsydda proteininstrument och sedan leverera dem in i levande celler där de beter sig som nya, långvariga organeller. Dessa syntetiska nav kan selektivt dra till sig naturliga proteiner och, när de utrustas med nedbrytningsmaskineri, aktivt avlägsna utvalda mål från cellen. Eftersom plattformen undviker att förändra cellens gener och är modulär i vad den kan bära, öppnar den en väg mot terapier som återställer eller skriver om cellulärt beteende—såsom att rensa skadliga proteiner eller omkoppla felaktig signalering—genom att helt enkelt installera nya, programmerbara ”arbetsstationer” i våra celler.
Citering: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Nyckelord: syntetiska organeller, peptidkoacervat, intracellulär leverans, proteinnedbrytning, cellteknik