Clear Sky Science · sv
CRISPR-Cas9 trans-klyvning hämmas av ett flankerat R-loop, en förlängd spacer och en inaktiv HNH-domän
Varför små DNA-snitt spelar roll
CRISPR-Cas9 är välkänt som ett molekylärt skalpell som kan klippa DNA på valda platser, men verktyget har ett andra, mindre uppmärksammat beteende: när det väl aktiverats kan det också småäta andra DNA-bitar i närheten. Att förstå när denna ”kollaterala” klyvning slås på eller av är avgörande för att utveckla säkrare genredigeringsterapier och känsligare diagnostiska tester. Denna studie dissekerar de fysiska egenskaperna hos Cas9–DNA–RNA-komplexet som avgör om Cas9 tyst gör sitt avsedda snitt eller också börjar tugga igenom lösa enkelsträngade DNA.
Hur CRISPR-saxarna sätts igång
För att verka binder Cas9 en kort bit guide-RNA som styr den till en matchande DNA-sekvens i ett genom. När Cas9 hittar sitt mål parar guide-RNA ihop sig med ena DNA-strängen, tvingar de två strängarna isär och skapar en DNA–RNA-hybridregion kallad ett R-loop. I sin klassiska roll klipper Cas9 därefter båda DNA-strängarna vid den platsen. Men nyare arbete visade att när Cas9 aktiverats på detta sätt kan dess RuvC-klyvdomän också skära i orelaterade enkelsträngade DNA, såsom poly(T)-sträckor, på andra platser i lösningen. Författarna undersökte därför vilka exakt geometriska och strukturella egenskaper hos mål-DNA och guide-RNA som gör denna kollaterala aktivitet stark, svag eller frånvarande.
Korta kontra långa mål: ge Cas9 utrymme att röra sig
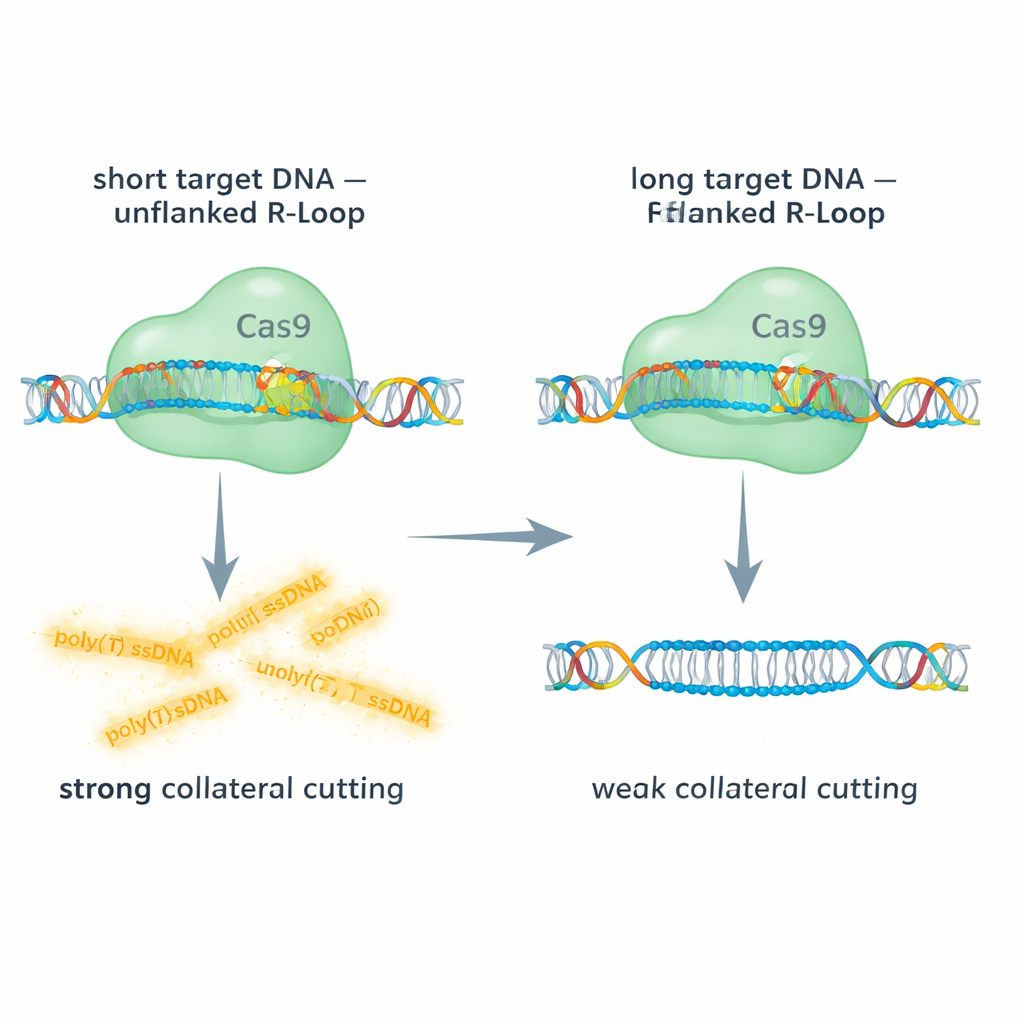
Teamet jämförde Cas9s verkan på korta och långa dubbelsträngade DNA-mål och använde fluorescerande avläsningar för att följa både det påmålsriktade snittet och kollateral klyvning av en enkelsträngad DNA-prob. Med korta DNA-mål är R-loopen vid guide-RNA:ets 5′-ände ”oflankerad” – det finns inget extra dubbelsträngat DNA som fortsätter bortom hybridregionen. Under dessa förhållanden visade Cas9 robust kollateral aktivitet på enkelsträngat DNA. I kontrast, när de använde längre DNA-segment som lämnade extra dubbelsträngat DNA som flankerade R-loopen, sjönk den kollaterala klyvningen dramatiskt, ibland med cirka 90 %, även om huvudsnittet på målet fortfarande inträffade. Att rikta in sig på långa enkelsträngade DNA, vilket helt tar bort R-loopen, återställde i stor utsträckning den kollaterala aktiviteten. Dessa jämförelser visar att en dubbelsträngad ”kappa” intill R-loopen styvar komplexet och fysiskt hindrar åtkomst eller flexibilitet som RuvC-domänen behöver för att skära andra strängar.
Finjustering med guidelängd och mismatchar
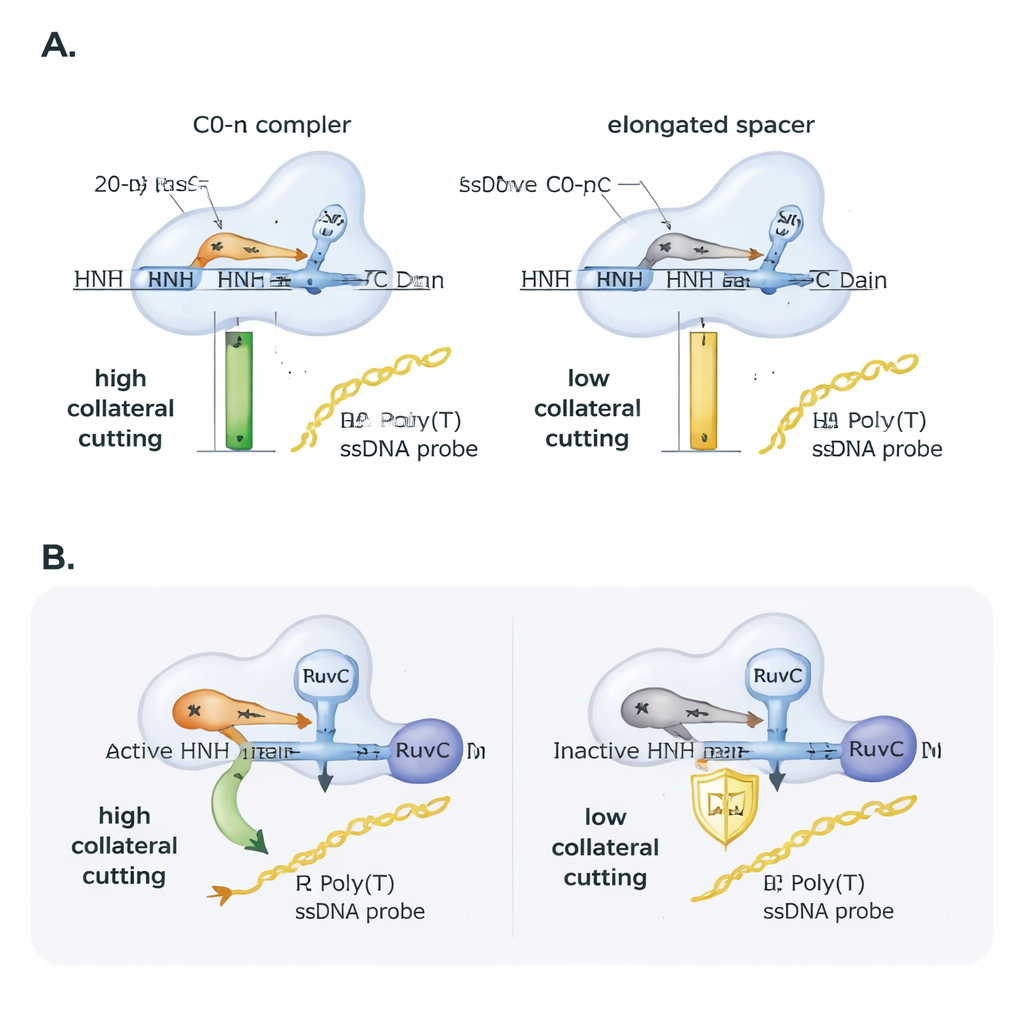
Forskarna undersökte sedan hur själva guide-RNA:t finställer detta beteende. De introducerade små mismatcher mellan guiden och mål-DNA:t och följde hur väl Cas9 fortfarande klippte. Huvudsakliga påmålsnittet tolererade många enkelbas-mismatchar, men den kollaterala klyvningen var mer bräcklig och berodde starkt på exakt var mismatchen var placerad, vilket understryker dess känslighet. Därefter förlängde de systematiskt guide-RNA-spacern utöver de vanliga 20 nukleotiderna. Även om Cas9 fortfarande kunde binda och klippa mål-DNA, föll den kollaterala aktiviteten nästan linjärt när spacer-längden ökade: att lägga till bara två extra baser halverade ungefär den kollaterala aktiviteten, och fyra extra baser minskade den ännu mer. I praktiska tester med SARS-CoV-2-genetiskt material gav endast DNA-ampliconer som var utformade för att producera en oflankerad R-loop med en guide av standardlängd en stark kollateral signal, vilket visar hur primer- och guide-design kan avgöra framgången för CRISPR-baserade detektionsassays.
En viktig hjälpardomän bakom kulisserna
Cas9 har två klyvdomäner, RuvC och HNH. Tidigare arbete kopplade kollateral klyvning direkt till RuvC, men denna studie visar att HNH fortfarande spelar roll. När författarna använde en Cas9-variant med en inaktiv HNH-domän sjönk den kollaterala aktiviteten kraftigt, även om bindningen till målet och nickningsbeteendet kvarstod. Intressant nog återfick den inaktiva-HNH-varianten kollateral klyvning liknande den normala enzymet om de gav Cas9 ett DNA-mål som redan var nickat i en sträng. Detta tyder på att HNH:s roll delvis är mekanisk: genom att klippa eller lossa den riktade strängen hjälper den proteinet att inta en form som exponerar RuvC för närliggande enkelsträngat DNA. Strukturella analyser av befintliga 3D-modeller stödjer denna bild och visar att oflankerade R-loopar och guider av standardlängd låter RNA:ets 5′-ände ”kapa” mot Cas9 och positionera de katalytiska regionerna gynnsamt, medan flankade R-loopar och förlängda guider packar proteinet mer tätt och sannolikt skärmar av RuvC-platsen från lösa strängar.
Vad detta betyder för framtida verktyg
För icke-specialister är huvudbudskapet att Cas9:s beteende inte är allt-eller-inget: små geometriska detaljer—hur långt DNA sträcker sig, hur lång guiden är och om en hjälpardomän kan fullfölja sitt snitt—avgör om enzymet håller sig till sitt huvuduppdrag eller också slaktar närliggande enkelsträngar. Korta mål som lämnar R-loopen oflankerad, standardguider på 20 baser och en aktiv HNH-domän främjar stark kollateral klyvning; långt flankerande DNA, utdragna guider eller en inaktiv HNH-domän undertrycker den. Dessa insikter ger forskare en mer exakt ratt att ställa in Cas9 med, vilket hjälper dem att designa säkrare genredigeringssystem som undviker oönskad kollateral skada, eller kraftfullare diagnostiska tester som avsiktligt utnyttjar denna kollaterala aktivitet för att upptäcka mycket små mängder virus- eller genetiskt material.
Citering: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Nyckelord: CRISPR-Cas9, kollateral klyvning, R-loop, guide RNA-spacer, nukleinsyra-diagnostik