Clear Sky Science · sv
NatA engagerar sig i multifaktor komplex vid ribosomens polypeptid-tunnelutgång
Hur celler finjusterar nya proteiner när de föds
Varje sekund tillverkar dina celler tusentals nya proteiner på små maskiner som kallas ribosomer. När varje proteinkedja framträder måste den trimmas, märkas och vikas korrekt, annars kan den bete sig fel och bidra till sjukdom. Denna studie granskar ett av de centrala märkningssystemen, en modifiering kallad N-terminal acetylering, och visar hur ett centralt enzymkomplex, NatA, samarbetar med flera partner direkt där nya proteiner lämnar ribosomen. Att förstå denna koreografi hjälper oss att förklara hur celler håller sina proteinfabriker i gott skick.
Den lilla kemiska etiketten som betyder något
De flesta proteiner börjar livet med samma första byggsten, aminosyran metionin. Ofta avlägsnas denna initiala metionin och ersätts med en liten kemisk etikett kallad en acetylgrupp. Denna etikett, som sätts på proteinets allra spets (dess N-terminus), kan påverka hur länge proteinet överlever, vart det tar vägen i cellen och hur det fungerar. Två huvudtyper av enzymer sitter vid ribosomens tunnelutgång för att hantera denna första förvandling: metionin-aminopeptidaser (MAPs), som klipper bort den inledande metioninen, och N-terminala acetyltransferaser (NATs), som lägger till acetyltaggen. Bland NAT:erna är NatA arbetsmyran i humana celler och kan potentiellt modifiera nästan 40 % av alla proteiner. Eftersom många proteiner tillverkas samtidigt måste cellen organisera dessa enzymer så att trimning och märkning sker snabbt och i rätt ordning.
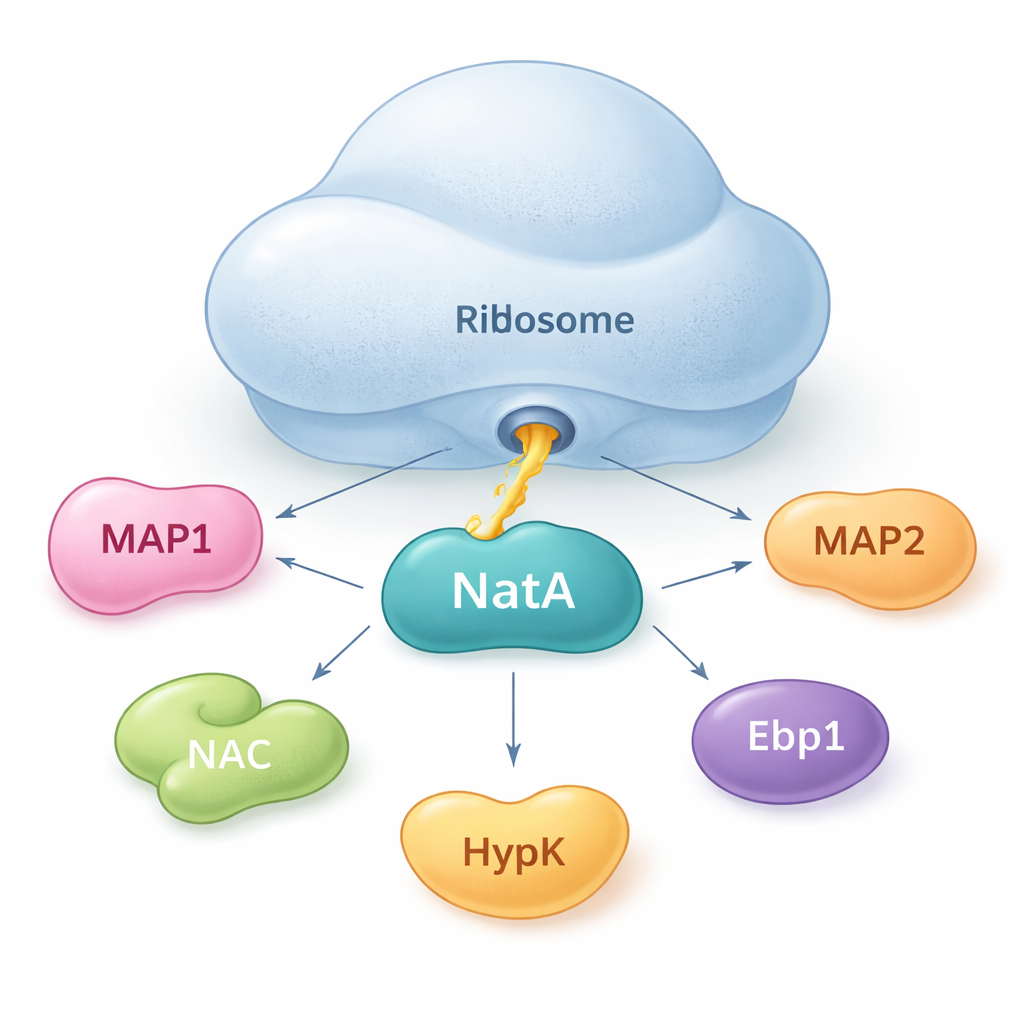
NatA som en mötespunkt för proteinhjälpare
Författarna visar att NatA inte agerar ensam. Istället fungerar det som en nav som samlar flera hjälpproteiner, både på och utanför ribosomen. Genom känsliga bindningsmätningar i lösning fann de att NatA kan bilda täta komplex med MAP1, det nysyntespolypeptid-associerade komplexet (NAC), regulatorproteinet HypK och ett annat enzym, Naa50, även utan ribosomen närvarande. NAC kan länka NatA till MAP1, vilket gör att både klipp- och märkningsstegen kan kopplas i en och samma assemblé. HypK, som normalt dämpar NatA:s aktivitet, kan dock blockera NAC:s bindning. Detta tyder på att celler kan växla NatA mellan ett mer aktivt, NAC-länkat tillstånd och ett begränsat, HypK-bundet tillstånd beroende på behov.
En andra dockningsplats precis vid tunnelutgången
Genom att använda kryo-elektronmikroskopi, en teknik som avbildar stora molekyler i nästan atomär detalj, upptäckte forskarna att NatA kan binda ribosomen i två distinkta positioner. En plats, tidigare känd, sitter något bort från tunnelutgången. Den nyligen upptäckta "proximal" platsen placerar NatA:s katalytiska kärna mycket nära där den växande proteinkedjan framträder, vilket förkortar avståndet kedjan måste färdas för att modifieras. Intressant nog kan båda positionerna vara ockuperade samtidigt, vilket innebär att två NatA-komplex kan sitta på samma ribosom. Den mer avlägsna kopian fungerar som ett skelett och ankare, medan den proximala kopian är optimalt placerad för att märka nya proteiner. De två NatA-molekylerna rör också vid varandra, vilket indikerar att NatA kan koordinera sina egna duplicat till multi-enzymteam.
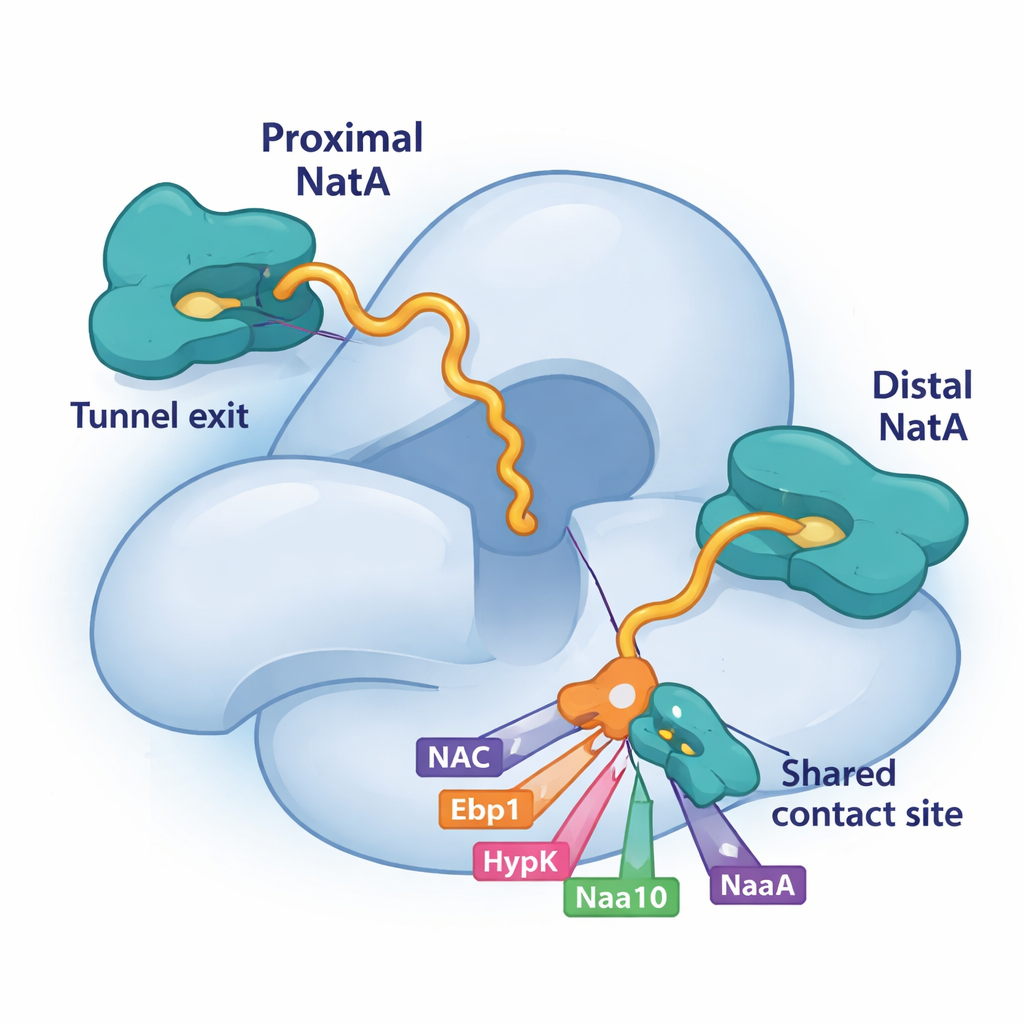
Konkurrens om en delad landningsplats på NatA
En nyckelbit i detta pussel är en liten fåra på den stora NatA-underenheten, Naa15. Studien visar att fyra olika ribosomassocierade faktorer—NAC, HypK, Ebp1 och till och med en svanssektion av NatA:s egen katalytiska undereenhet, Naa10—använder korta helixar för att fästa vid exakt samma yta på Naa15. Eftersom de alla förlitar sig på denna delade landningsplats måste de konkurrera om tillgång. När HypK ockuperar platsen tystar det inte bara NatA:s aktivitet utan förhindrar också att NatA parar ihop sig med NAC eller bildar NatA–NatA-dimerer. När NAC, pseudoenzymet Ebp1 eller proximal Naa10 binder där istället kan de omforma NatA:s position eller kopplingar vid ribosomen. Denna konkurrensutsatta bindning ger cellen ett flexibelt sätt att välja vilka partner som monteras runt NatA vid varje givet ögonblick.
Ett pseudoenzym som trafikledare
Proteinet Ebp1 är särskilt fascinerande. Det liknar ett av de metioninborttagande enzymerna men saknar katalytisk aktivitet; det är ett "pseudoenzym." Tidigare arbete visade att Ebp1 kan sitta på ribosomen nära tunnelutgången och klämma fast en lång RNA-segment. I denna studie finner författarna att när NatA ansluter till ribosomen, flyttar Ebp1 på sig, släpper RNA:t och använder i stället sin egen helix för att ta den samma bindningsplatsen på Naa15 som NAC och HypK använder. Denna omplacering tyder på att Ebp1 kan fungera som en platsinnehavare eller organisatör: det kan forma den lokala RNA-miljön och sedan lämna över kontrollen till aktiva enzymer som MAPs och NatA, utan att själv utföra kemi.
Varför denna molekylära trängselkontroll är viktig
För en icke-specialist kan detaljer om helixar och bindningsytor låta abstrakta, men budskapet är enkelt: celler kör ett högt koreograferat, flerstegs kvalitetskontrollsystem precis där proteiner föds. NatA sitter i centrum för detta system och kan rekrytera eller släppa olika partner beroende på vilka faktorer som vinner tillgång till en avgörande dockningsficka och vilken ribosomal plats NatA ockuperar. Detta flexibla nätverk hjälper till att säkerställa att trimning och acetylering sker med rätt timing och ordning för tusentals olika proteiner. Eftersom fel i N-terminal bearbetning kopplas till utvecklingsstörningar, neurodegeneration och cancer, ger kartläggningen av hur NatA och dess partner monterar ihop sig forskare en tydligare plan för hur tidig proteinbearbetning styrs — och hur den kan riktas när den går fel.
Citering: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Nyckelord: proteinkvalitetskontroll, N-terminal acetylering, ribosomens tunnelutgång, NatA-komplexet, ko-translationell modifiering