Clear Sky Science · sv
Växtfukosyltransferaset FUT11 förvränger sockermottagaren för att katalysera via en tillfällig oxokarbonyum‑liknande mellanprodukt
Hur växter finslipar sockren på sina proteiner
Proteiner i våra celler, och i växter, är ofta dekorerade med komplexa kedjor av sockerarter som fungerar som streckkoder och styr hur dessa proteiner veckas, hur länge de finns kvar och vilka partners de kan binda. Denna studie fokuserar på ett växtenzym kallat FUT11 som tillsätter en liten sockerart, fukos, till dessa kedjor. Genom att avslöja exakt hur FUT11 verkar på atomnivå visar författarna ett överraskande knep: enzymet böjer kortvarigt sitt sockermolekylära partner ur form för att driva ett svårt kemiskt steg. Att förstå denna process är viktigt inte bara för grundläggande biologi utan också för att utforma säkrare läkemedel framställda i växter som undviker att väcka oönskade immunsvar hos människor.
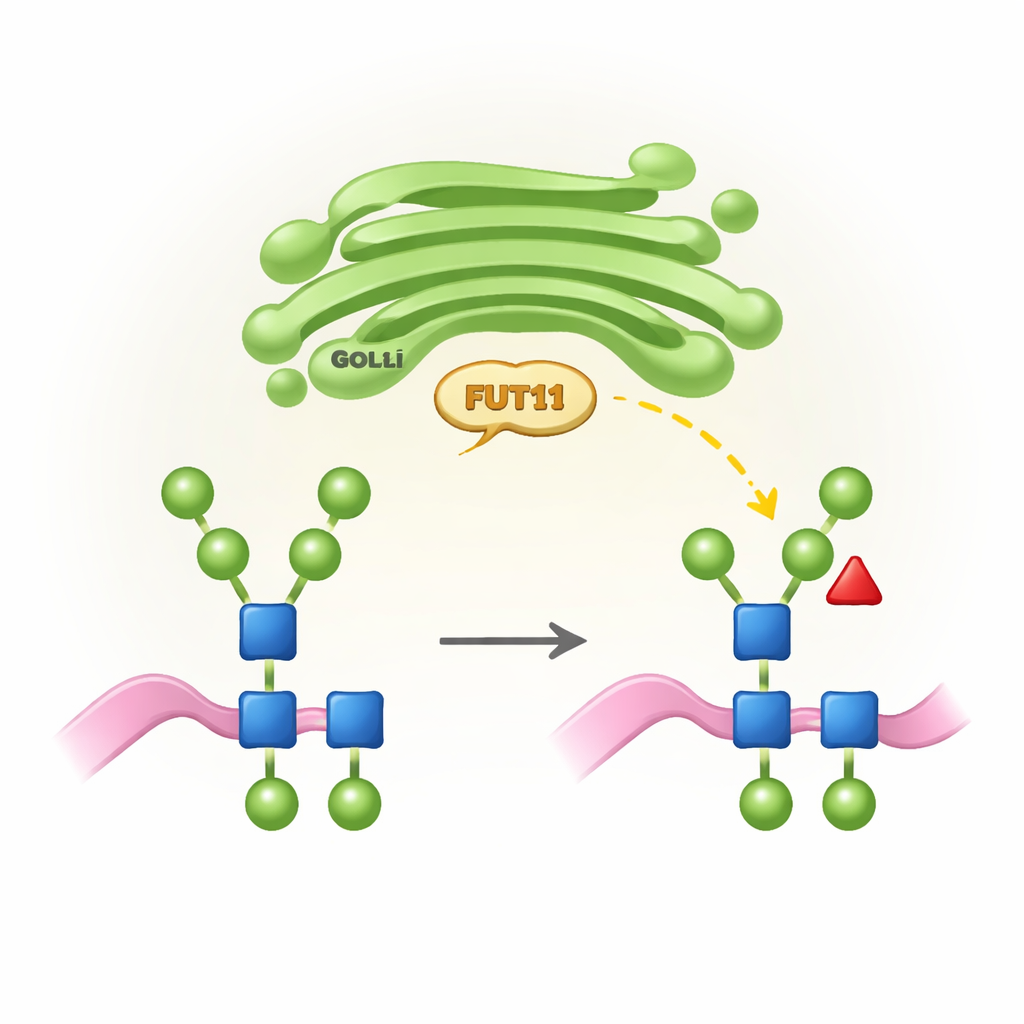
Växtspecifika sockerflaggor och varför de spelar roll
Alla högre organismer använder en process kallad N‑glykosylering för att fästa sockertrådar (N‑glykanker) på vissa ställen på proteiner. I djur omarbetas dessa kedjor i cellens Golgiapparat till invecklade strukturer som ofta slutar med sialinsyra och bär en kärnfukos i en specifik position. Växter följer däremot en annan ”designregel”: deras N‑glykanker saknar vanligtvis sialinsyra men bär en kärnfukos i en annan position (kallad β1,3) samt en extra xylos. Dessa växtspecifika drag är avgörande för normal tillväxt och fertilitet, men kan uppfattas som främmande av människans immunsystem. FUT11 är ett av nyckelenzymerna i växter som installerar denna kärnfukos, och dess aktivitet formar både växtutveckling och hur växtproducerade terapeutiska proteiner kommer att uppfattas i våra kroppar.
Kartläggning av var FUT11 kan verka på komplexa sockergrenar
För att förstå vad FUT11 känner igen testade forskarna enzymet på ett mikroarray med 144 olika N‑glykankonstruktioner. De fann att FUT11 är ganska selektiv för en gren av sockerskogen — den så kallade β1,3‑armen — som måste bära en viss byggsten (en terminal N‑acetylglukosamin, eller GlcNAc) för att reaktionen ska fortgå. Samtidigt är FUT11 tolerant mot andra dekorationer: det fungerar fortfarande när den centrala mannosen bär en växtspecifik xylos, och även när en annan fukos redan lagts till i den däggdjurspositionen i kärnan. Den motsatta grenen (β1,6) ligger mest utsatt mot lösningen och gör bara svaga kontakter med enzymet, vilket förklarar varför FUT11 kan hantera en mängd olika modifieringar där. Dessa bindningspreferenser hjälper till att förklara varför växter bildar en karaktäristisk uppsättning N‑glykankonstruktioner och visar hur FUT11 kan användas eller undvikas vid ingenjörsarbete med växtceller för bioteknik.
En unik struktur för att gripa och positionera socker
Med hjälp av röntgendiffraktion löste teamet den tredimensionella strukturen av FUT11 bunden till sin sockerdonator (GDP‑fukos) och en N‑glykanmottagare. Enzymet har en tvåflikig ”GT‑B”‑arkitektur: en flik omfamnar GDP‑fukos medan en ovanligt invecklad acceptorflik, inklusive en växtspecifik N-terminal subdomän, sveper runt N‑glykankedjan. Denna extra subdomän, fäst vid resten av enzymet genom disulfidbryggor, förankrar den centrala delen av glykankedjan och hjälper till att presentera den reaktiva GlcNAc‑enheten mot donatorn. Mutering av nyckelaminosyror bekräftade deras roller: förändring av en enda glutamat (Glu158) eliminerade aktiviteten, medan förändring av två närliggande rester kraftigt försvagade fukosylering i konstruerade humana celler. Dessa resultat kopplar strukturella ögonblicksbilder till verklig cellulär funktion och visar exakt vilka delar av proteinet som är oumbärliga för bindning och katalys.
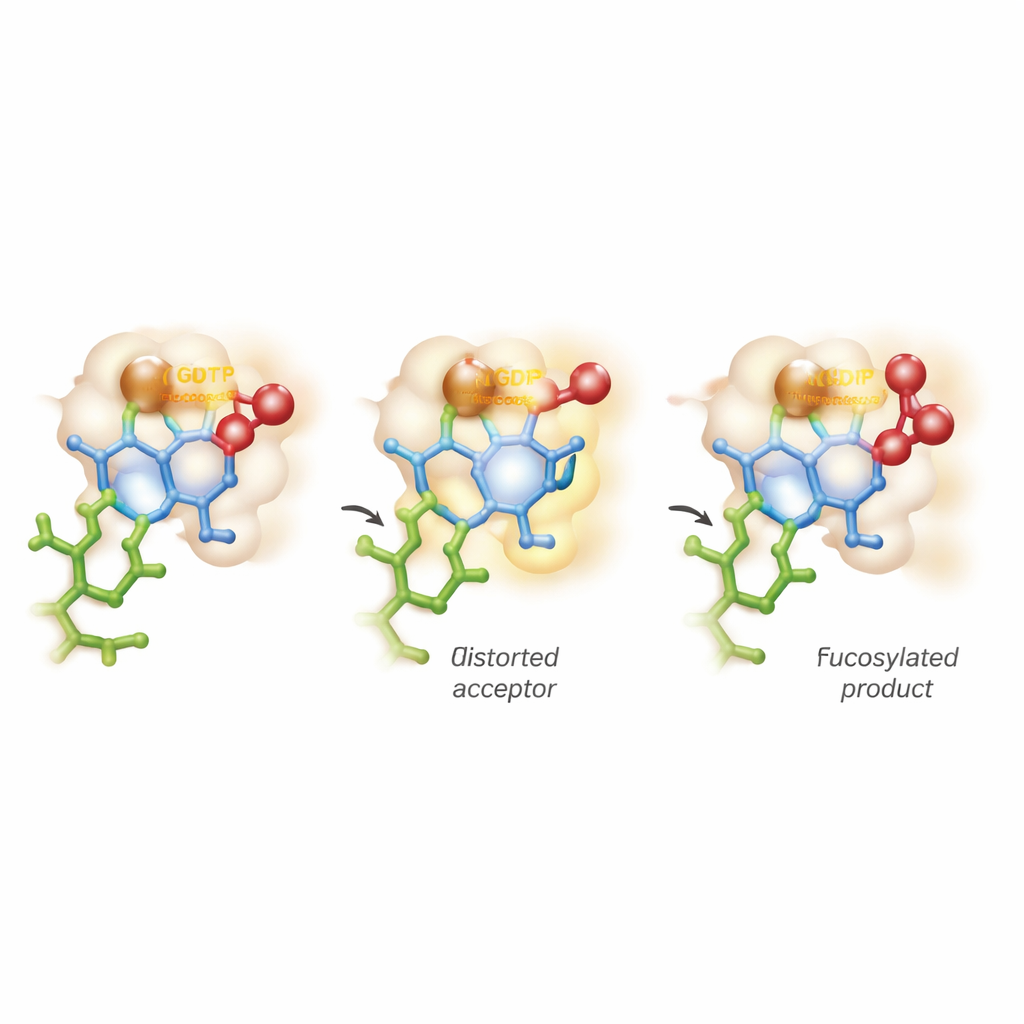
Böjning av sockret och att gå på linjen mellan två reaktionsvägar
Den mest slående insikten kommer från avancerade datorsimuleringar som kombinerar kvantmekanik och molekyldynamik. Traditionella uppfattningar antar att mottagarsockret behåller sin stabila, stolformade form medan enzymet helt enkelt aktiverar donatorn. Här beter sig FUT11 mer aggressivt: interaktioner drivna av Glu158 förvränger tillfälligt den innersta GlcNAc‑ringen till en mindre bekväm pucklad form. I denna spända hållning är den kritiska hydroxylgruppen perfekt inriktad för att attackera fukosdonatorn. Beräkningarna visar att när den kemiska bindningen till GDP bryts uppstår ett kortlivat, positivt laddat ”oxokarbonyum‑liknande” tillstånd på sockret, innan den nya bindningen till mottagaren är fullständigt bildad. Detta innebär att reaktionen inte passar snyggt i lärobokskategorierna SN1 eller SN2, utan fortlöper längs ett kontinuum i en asynkron, nästan stegvis bana.
Gömd flexibilitet och evolutionära ekon
Genom att jämföra FUT11 med ett relaterat humant enzym, FUT9, fann författarna att växtenzymet även, om än svagt, kan modifiera en annan typ av sockermotiv (LacNAc) för att bilda en struktur känd som Lewis X. Denna sidoaktivitet är sannolikt inte biologiskt viktig i växter, där Lewis X normalt inte finns, men den belyser hur liknande proteinramverk kan återanvändas under evolutionen för att verka på olika sockerkontexter. Studien antyder att FUT11 och dess släktingar delar ett modulärt ramverk för igenkänning av N‑glykanker, med subtila justeringar som skiftar specificiteten mellan växtkärnor och djurantenner.
Varför detta böjtrick betyder något för vetenskap och medicin
Sammanfattningsvis visar arbetet att FUT11 gör mer än att bara föra ihop två sockerpartners: det böjer aktivt mottagarsockret till en reaktiv ställning och kanaliserar kemin genom en flyktig, laddad mellanprodukt. För en allmän läsare betyder det att sockret på proteinet inte är en stel dokningsplats utan en flexibel deltagare som enzymet formar efter behov. Denna nya syn på ”konformationell katalys” hjälper till att förklara hur enzymer uppnår både hastighet och selektivitet och erbjuder en ritning för omdesign av glykosyleringsvägar. I praktiska termer kan kunskap om exakt hur FUT11 känner igen och modifierar växt‑N‑glykanker vägleda ingenjörsarbete i grödor och växtbaserade produktionssystem för att minimera immunstimulerande sockermönster i humana terapier, eller för att skapa skräddarsydda glykoproteiner med önskade biologiska egenskaper.
Citering: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Nyckelord: växtglykosylering, fukosyltransferas FUT11, N‑glykanker, enzymmekanism, glykoteknik