Clear Sky Science · sv
Strukturella grunder och patologiska konsekvenser av den dimeriska OS9-SEL1L-HRD1 ERAD-kärnkomplexet
Cellens städpatrull under mikroskopet
Inne i varje cell finns en livlig fabrik som omvandlar genetiska instruktioner till fungerande proteiner. Precis som i en fabrik uppstår misstag. När proteiner felveckas kan de täppa igen systemet och bidra till sjukdom. Denna studie zoomar in på en av cellens viktigaste kvalitetskontroller—SEL1L‑HRD1‑komplexet—för att avslöja dess detaljerade tredimensionella struktur och visa hur små genetiska förändringar kan bryta ned denna maskin och potentiellt leda till mänsklig sjukdom.
ett dolt transportband i cellen
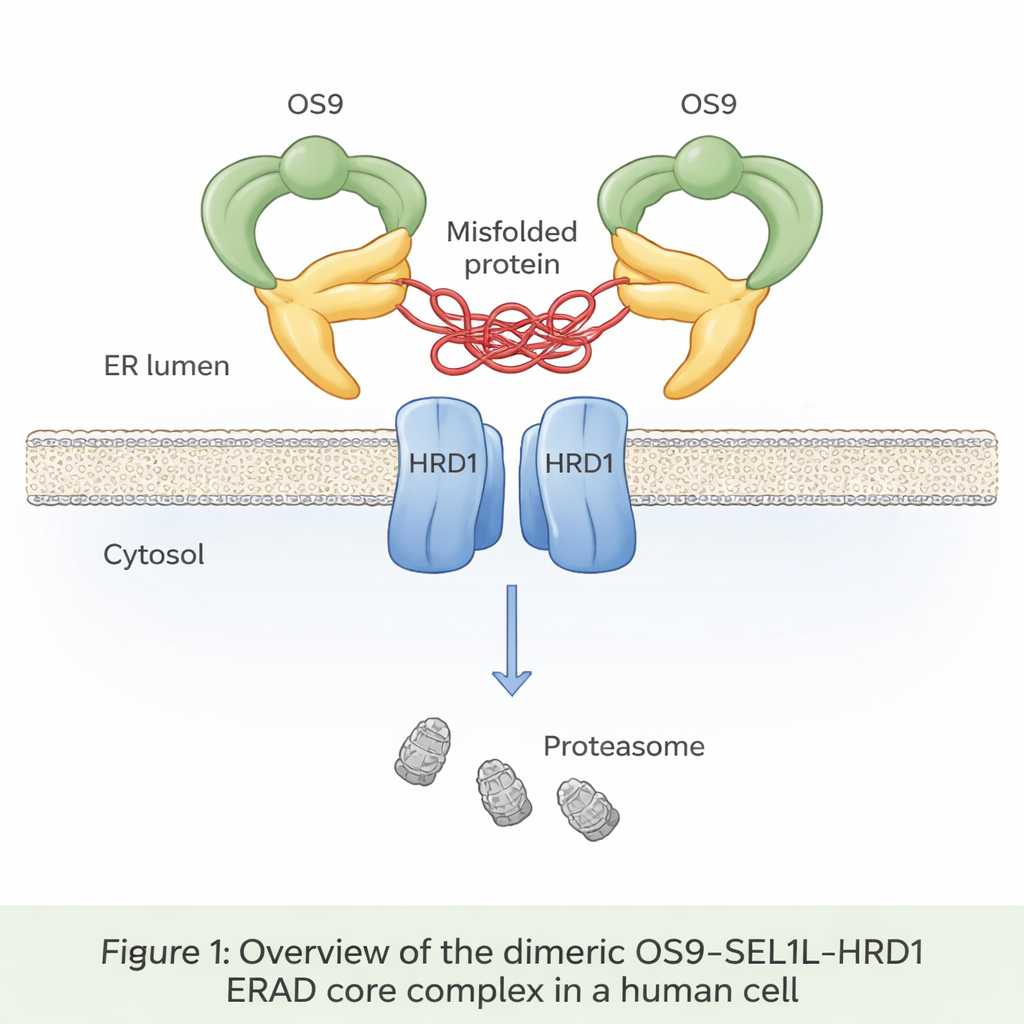
Upp till en tredjedel av alla nybildade proteiner går in i ett utrymme som kallas det endoplasmatiska retiklet, eller ER, där de veckas och kontrolleras. Felveckade proteiner kännetecknas normalt, dras ut ur ER och bryts ner i en process som kallas ER‑associerad nedbrytning (ERAD). I centrum för en huvudsaklig ERAD‑väg finns en trio proteiner: OS9, SEL1L och HRD1. OS9 fungerar som en sensor för felaktiga, sockermärkta proteiner; SEL1L fungerar som en stomme; och HRD1 märker ut dömda proteiner med små ubiquitinflaggor som signalerar för cellens avfallshanterare, proteasomerna. Fram till nu har ingen i atomär detalj sett hur dessa tre delar passar ihop i mänskliga celler.
Avslöja kärnmaskinens form
Författarna använde kryoelektronmikroskopi, en teknik som avbildar snabbfrysta molekyler i närapå atomär upplösning, för att visualisera OS9‑SEL1L‑HRD1‑komplexet renat från mänskliga celler. De upptäckte att det bildar en dimer—i praktiken två identiska kopior sammanfogade—istället för att förbli enskilda enheter. På ER‑lumens sida (insidan av ER) sammanförs två OS9‑ och två SEL1L‑molekyler till en klo‑liknande ring med en central öppning som verkar utformad för att greppa felveckade proteiner. I membranet själv parar sig två HRD1‑molekyler för att bilda en gemensam kanal. Denna organisation placerar ”klon” direkt ovanför HRD1‑dörren och skapar en kontinuerlig bana för felveckade proteiner att förflytta sig från ER‑lumen, genom membranet och mot nedbrytning i cytosolen.
Hur små förändringar saboterar ett stort system
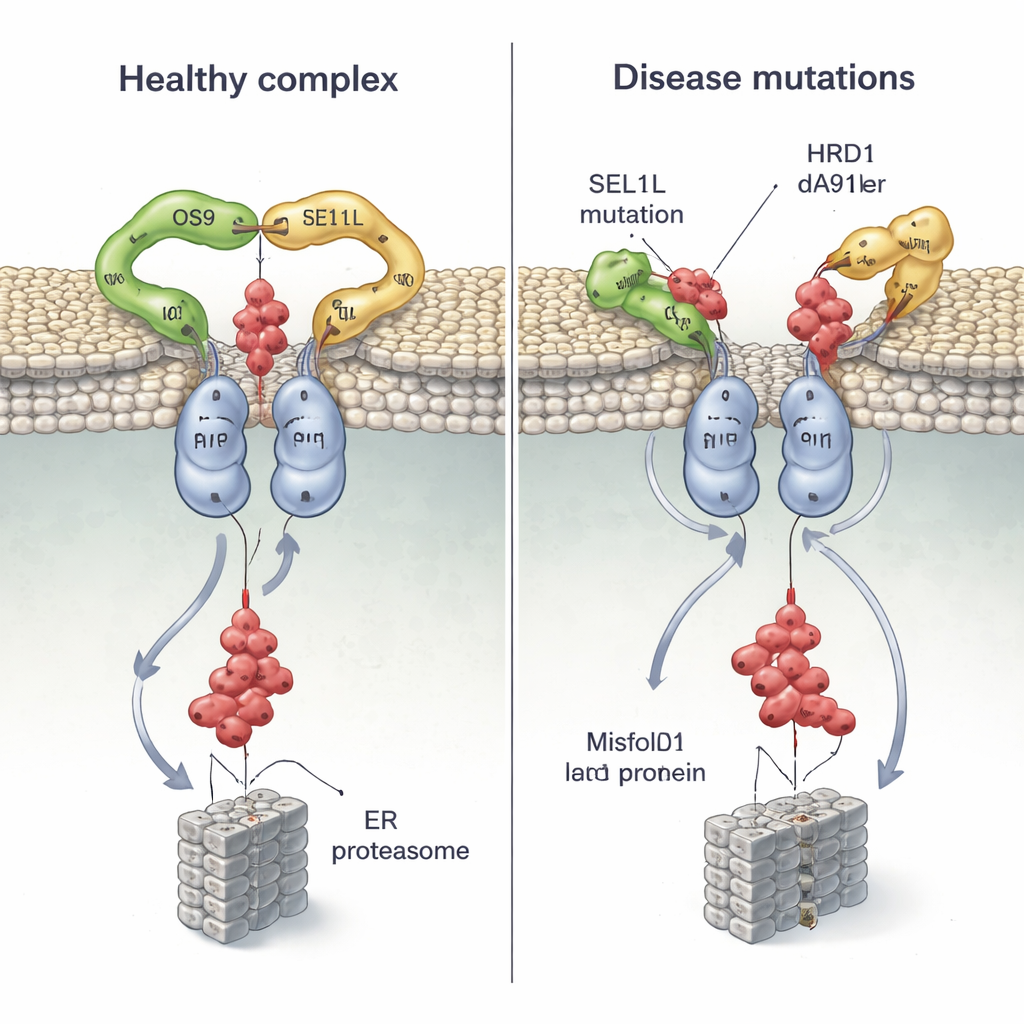
Eftersom mutationer i SEL1L och HRD1 har hittats hos patienter med allvarliga neurodevelopmentala och andra störningar, kartlade teamet flera sjukdomsassocierade varianter på deras struktur och testade hur de beter sig i celler. Två SEL1L‑mutationer, G585D och S658P, sitter precis vid kontaktpunkterna med OS9 respektive HRD1. I cellexperiment försvagade G585D nästan helt SEL1L:s förmåga att binda OS9, medan S658P kraftigt försvagade dess grepp om HRD1; att kombinera båda mutationerna bröt i princip upp kärnkomplexet, samtidigt som andra partners förblev opåverkade. Som en följd hade cellerna svårt att märka och rensa en felveckad hormonprecursor, vilket tillät defekta proteiner att dröja kvar.
En sjukdomsmutation i membrankanalen
Strukturen visar också att HRD1:s transmembrana segment 3 är den centrala ytan där två HRD1‑molekyler möts för att bilda kanalen. Forskarna konstruerade cystein‑”handtag” på specifika positioner och använde kemisk tvärbindning för att bekräfta att dessa regioner kommer i nära kontakt i levande celler, vilket visar att HRD1 verkligen dimeriserar in vivo. När de störde en enda, starkt bevarad rest (T93) vid detta gränssnitt föll dimeren isär och ERAD‑aktiviteten kollapsade, trots att komplexet fortfarande kunde montera med OS9 och SEL1L. De undersökte sedan en nyupptäckt patientvariant, HRD1 A91D, funnen hos ett barn med hjärt‑ och lungproblem. Denna förändring, också i dimergränssnittet, halverade ungefär HRD1‑dimeriseringen och försvårade kraftigt borttransporten av felveckade proteiner, återigen utan att störa det övergripande bindandet av partners.
En ny bild av protein‑kvalitetskontroll och sjukdom
Genom att kombinera strukturell biologi med cellbaserade tester visar detta arbete att OS9‑SEL1L‑HRD1‑komplexet fungerar som en parvis, dimerisk maskin: en klo‑liknande fångare kopplad till en gemensam kanal som för bort defekta proteiner ur ER. Mutationer som luckrar upp klons grepp eller destabiliserar HRD1‑paret justerar inte bara effektiviteten—de kan effektivt sätta igen systemet, vilket tillåter skadade proteiner att ansamlas och bidra till mänsklig sjukdom. För icke‑specialister är huvudbudskapet att även enkla bokstavsändringar i vårt DNA kan subtilt förvränga formen hos väsentliga cellulära maskiner, med långtgående konsekvenser för hjärnans utveckling, immunitet och organfunktion.
Citering: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Nyckelord: protein-kvalitetskontroll, endoplasmatiskt retikulum, ERAD, SEL1L-HRD1-komplexet, proteinfelveckning