Clear Sky Science · sv
Profilering av exons i enskilda celler avslöjar splitsningshändelser som formar genuttryck och celltillståndsdynamik
Hur små redigeringar i RNA kan ändra cellbeteende
Våra celler läser och splitsar ständigt RNA-instruktioner för att bestämma vilka proteiner som ska tillverkas och hur de ska reagera på stress, växa eller dela sig. Denna studie visar att ändringar av mycket små delar av dessa RNA-meddelanden — enskilda segment kallade exons — kan kraftigt omforma genaktivitet och till och med förskjuta hur celler rör sig genom cellcykeln. Arbetet introducerar ett kraftfullt verktyg som låter forskare skanna många av dessa små RNA-val samtidigt, cell för cell, vilket öppnar nya sätt att förstå sjukdom och hitta läkemedelsmål.
Att ta bort utvalda ord ur den genetiska texten
Gener är skrivna som långa DNA-sträckor, men cellerna läser dem inte rakt igenom. Istället klipper och sätter de ihop mindre block, kallade exons, för att bygga ett RNA-meddelande. Genom att välja vilka exons som bevaras kan celler skapa flera proteinversioner från en enda gen, ungefär som att producera olika redigeringar av en film från samma råmaterial. Många sjukdomar, inklusive cancer och autism, kopplas till fel i denna process, men för de flesta exon-val vet vi fortfarande inte vad de faktiskt gör. Författarna ville ändra på detta genom att bygga ett storskaligt system som kan ta bort specifika exons från många gener och sedan i tusentals enskilda celler samtidigt observera hur dessa ändringar påverkar cellens interna nätverk.
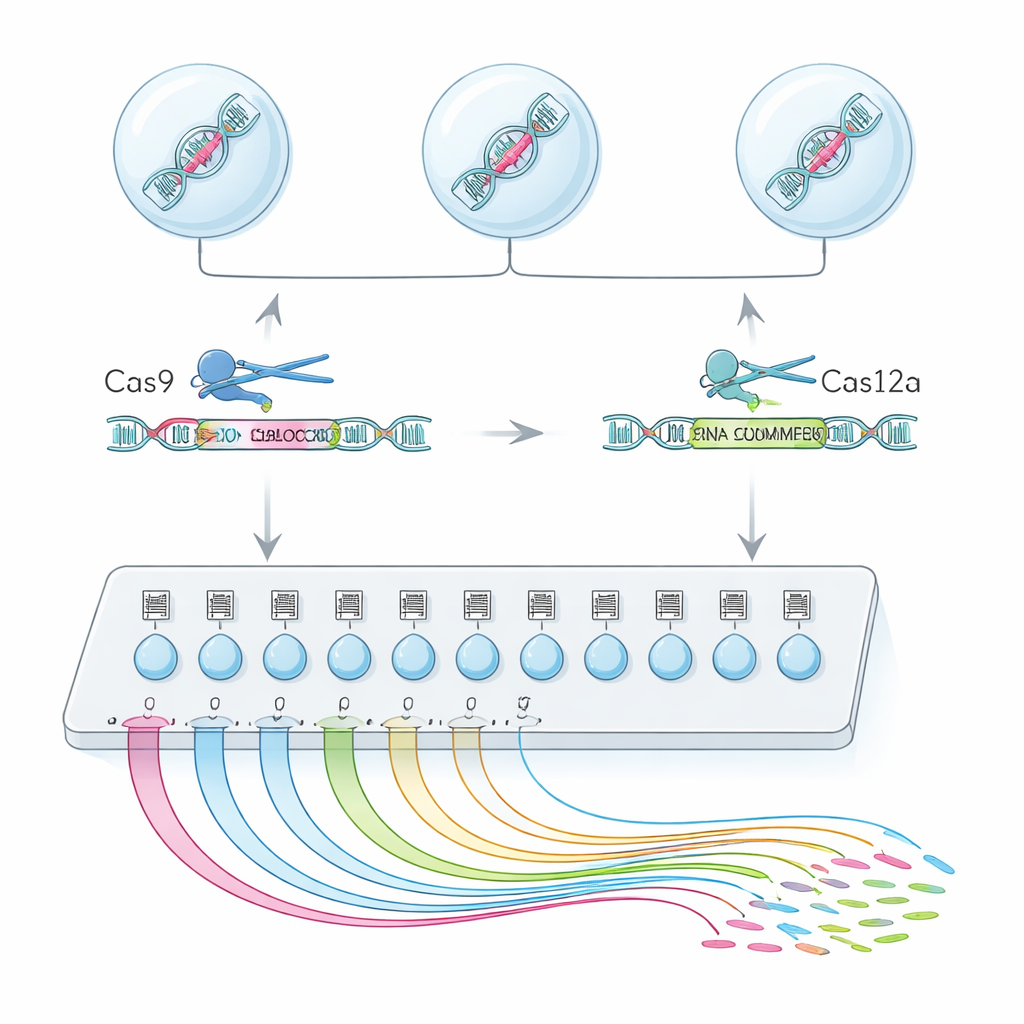
En enskild-cells "sökmotor" för exons funktion
För att uppnå detta kombinerade teamet två genredigeringsenzym, Cas9 och Cas12a, i en hybridplattform kallad CHyMErA. Varje enzym styrs till DNA av korta RNA-”adresser”. Genom att rikta de två enzymerna att klippa precis före och precis efter ett valt exon kan de prydligt ta bort det segmentet medan resten av genen lämnas intakt. Den nya metoden, scCHyMErA-Seq, kopplar denna precisa klippning till single-cell RNA-sekvensering. Varje cells RNA fångas i en droplet tillsammans med en streckkod och de guide-RNA som anger vilket exon som togs bort. Sekvensering avslöjar sedan, för tiotusentals celler, både vilken redigering varje cell fick och det detaljerade mönstret av gener den slog på eller av.
Utforma verktyget för att se båda saxbladen
En viktig utmaning var att pålitligt upptäcka Cas12a-guider tillsammans med Cas9 i samma enskilda-cellsexperiment. Initierande konstruktioner misslyckades antingen med att fånga Cas12a-guide-RNA eller skadade redigeringseffektiviteten. Forskarna löste detta genom att noggrant omdesigna Cas12a-handtagssekvensen för att ta bort delar som för tidigt avbröt transkriptionen, samt genom att lägga till ett litet stabiliserande RNA-element och ett riktat amplifikationssteg. Dessa justeringar ökade förmågan att se båda guiderna till omkring 90 procent av cellerna, samtidigt som stark exon-borttagning bevarades. Med denna optimerade uppställning skannade författarna 224 alternativa exons över 161 gener i humana celler och profilerade mer än 200 000 högkvalitativa enskilda celler.
Upptäcka exons som kontrollerar genprogram och cellcykler
När teamet jämförde genaktiviteten i redigerade celler med kontroller orsakar nästan hälften av de testade exonen betydande skift i hundratals andra gener. Exons från gener involverade i RNA‑bearbetning och transkription tenderade att klustra tillsammans, producera liknande uttrycksfingeravtryck och avslöja delade biologiska vägar, som ribosombildning eller RNA-nedbrytning. I vissa fall hade borttagningen av ett enda exon en tydlig och tolkbar effekt: borttagning av ett exon i TAF5- eller LSM11-generna störde korrekt bearbetning av histon-RNA och ledde till en ovanlig ansamling av polyadenylerade histon-meddelanden. Datasetet lyfte också fram dussintals exons vars förlust förändrade hur många celler som befann sig i olika stadier av cellcykeln, vilket knöt specifika splitsningshändelser direkt till beslut om när en cell pausar, kopierar sitt DNA eller förbereder sig för att dela sig.
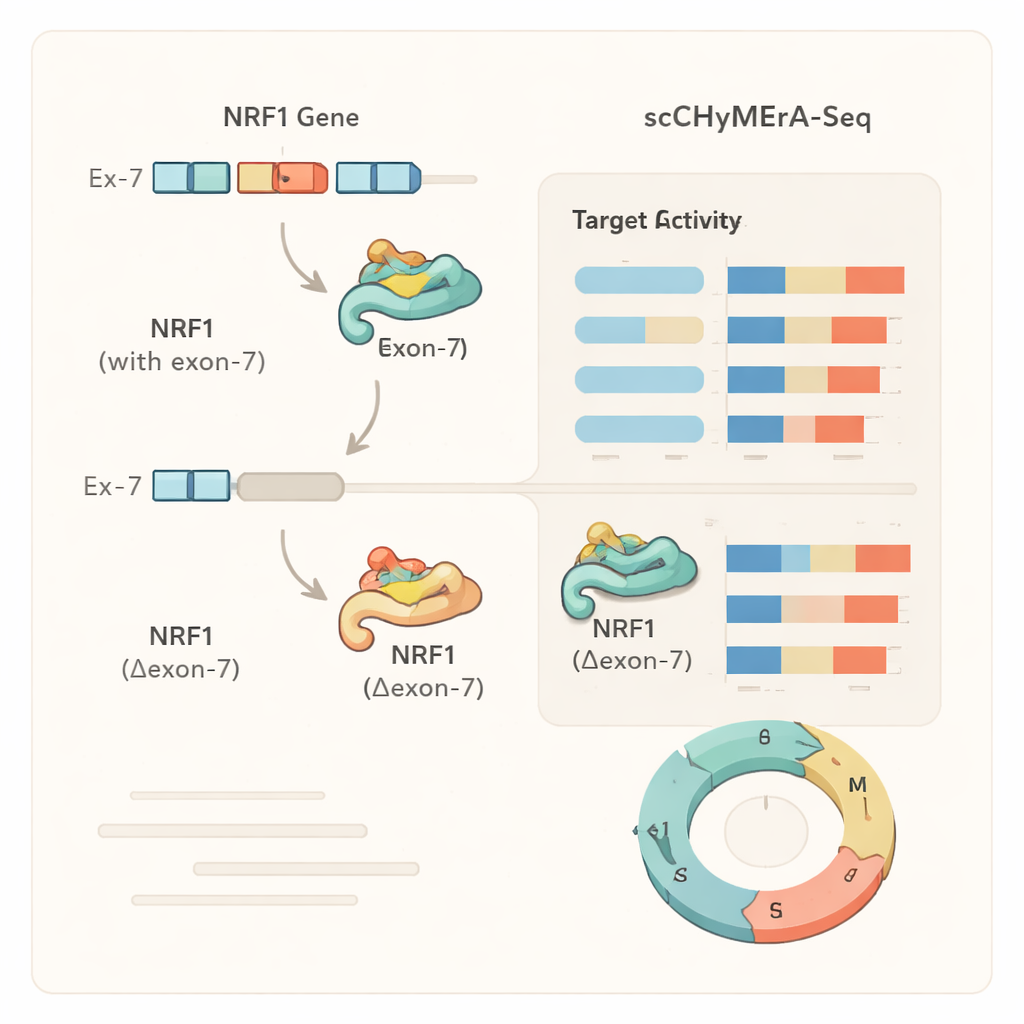
Fallstudie: ett exon som finjusterar en huvudregulator
Ett anmärkningsvärt exempel var exon 7 i genen NRF1, en transkriptionsfaktor som kontrollerar många gener involverade i cellernas energiproduktion. Detta exon överlappar delvis NRF1:s DNA‑bindande region. När exon 7 togs bort förändrades hundratals NRF1‑reglerade gener i sitt uttryck, och detaljerade experiment visade att den förkortade NRF1‑proteinet var mycket mindre benäget att binda sina målförekomster i genomet. Författarna identifierade också en specifik splitsningsregulator, SRSF3, som främjar inkludering av detta exon, vilket avslöjar en kedja från en splitsningsfaktor, via ett exonval i NRF1, till breda förändringar i cellulära genprogram och metabolism. Liknande analyser visade att för vissa gener efterliknade exon‑borttagning en komplett gen‑knockout, medan för andra gav det en mer finjusterad, tillståndsberoende förändring, vilket tyder på att alternativa exons kan subtilt modulera proteinets funktion snarare än att helt slå på eller av den.
Därför spelar detta roll för hälsa och framtida behandlingar
För en icke‑specialist är huvudbudskapet att celler förlitar sig på inkludering eller utelämnande av mycket korta RNA‑segment för att ställa in hur gener fungerar, och att dessa fina justeringar kan förskjuta stora egenskaper såsom hur celler delar sig eller svarar på stress. scCHyMErA‑Seq‑plattformen fungerar som ett höggenomströmmande labbtest för dessa splitsningsval, och identifierar vilka exons som har verklig funktionell betydelse och hur de omformar cellulära tillstånd. Eftersom många cancerformer och neurologiska störningar involverar felaktigt splitsade exons eller förändrade transkriptionsfaktorer, kan detta tillvägagångssätt hjälpa till att prioritera vilka splice‑varianter som bör riktas med framtida läkemedel eller RNA‑terapier, och ge en karta för att förstå hur små ändringar i den genetiska texten sprider sig till stora förändringar i cellbeteende.
Citering: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Nyckelord: alternativ splitsning, single-cell RNA-sekvensering, CRISPR-screening, genreglering, cellcykeln