Clear Sky Science · sv
Granzyme B-mimetisk nanozym för målinriktade nanovesikelantitumörapplikationer
Att nyskapa kroppens cancertörstare
Vårt immunsystem har specialiserade celler som kan spåra upp och döda cancer, men i många solida tumörer har de svårt att ta sig in, blir snabbt utmattade eller angriper fel mål. Denna studie beskriver ett helt artificiellt, nanoskaligt system som imiterar ett av immunsystemets mest kraftfulla vapen och levererar det direkt in i tumörceller. Arbetet är betydelsefullt eftersom det pekar mot cancerbehandlingar som beter sig som levande immunceller, men som är gjorda av stabila, kontrollerbara material i stället för sköra mänskliga celler.
Att förvandla en naturlig lönnmördare till en ritning
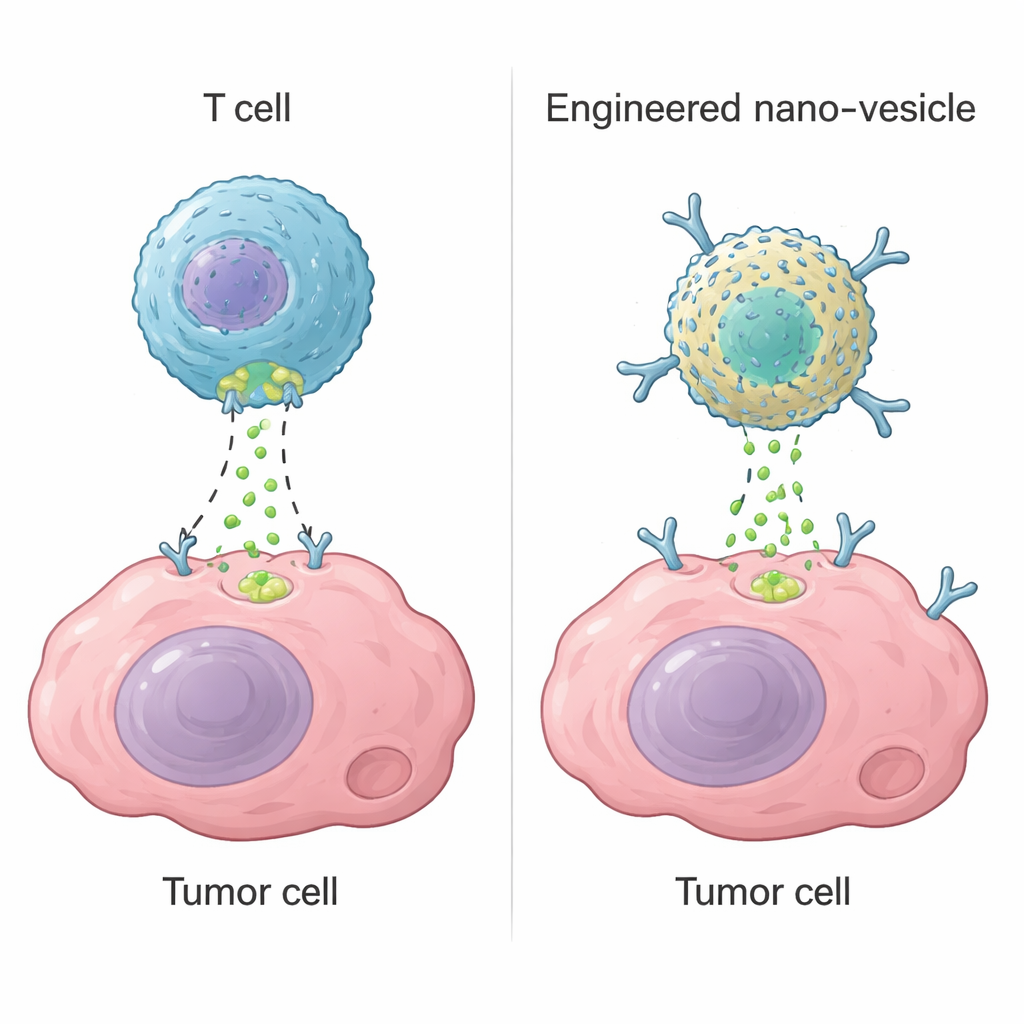
Cytotoxiska T‑celler, en typ av vita blodkroppar, dödar farliga celler med hjälp av ett enzym kallat granzyme B. När de känner igen ett mål skapar de små hål i målcellens membran och injicerar granzyme B, vilket aktiverar självmordsprogram inne i cellen. Denna strategi ligger bakom moderna terapier som CAR‑T‑celler, vilka kan bota vissa blodcancerformer. Men i solida tumörer misslyckas CAR‑T‑celler ofta eftersom de inte kan nå alla tumörområden, blir utmattade eller träffar frisk vävnad av misstag. Författarna frågade sig om de kunde bygga en icke‑levande, nanoskalig enhet som återskapar grunden i granzyme B:s funktion — att slå på cellens självdestruktionsmaskineri — utan att förlita sig på levande T‑celler.
Designa ett litet artificiellt enzym
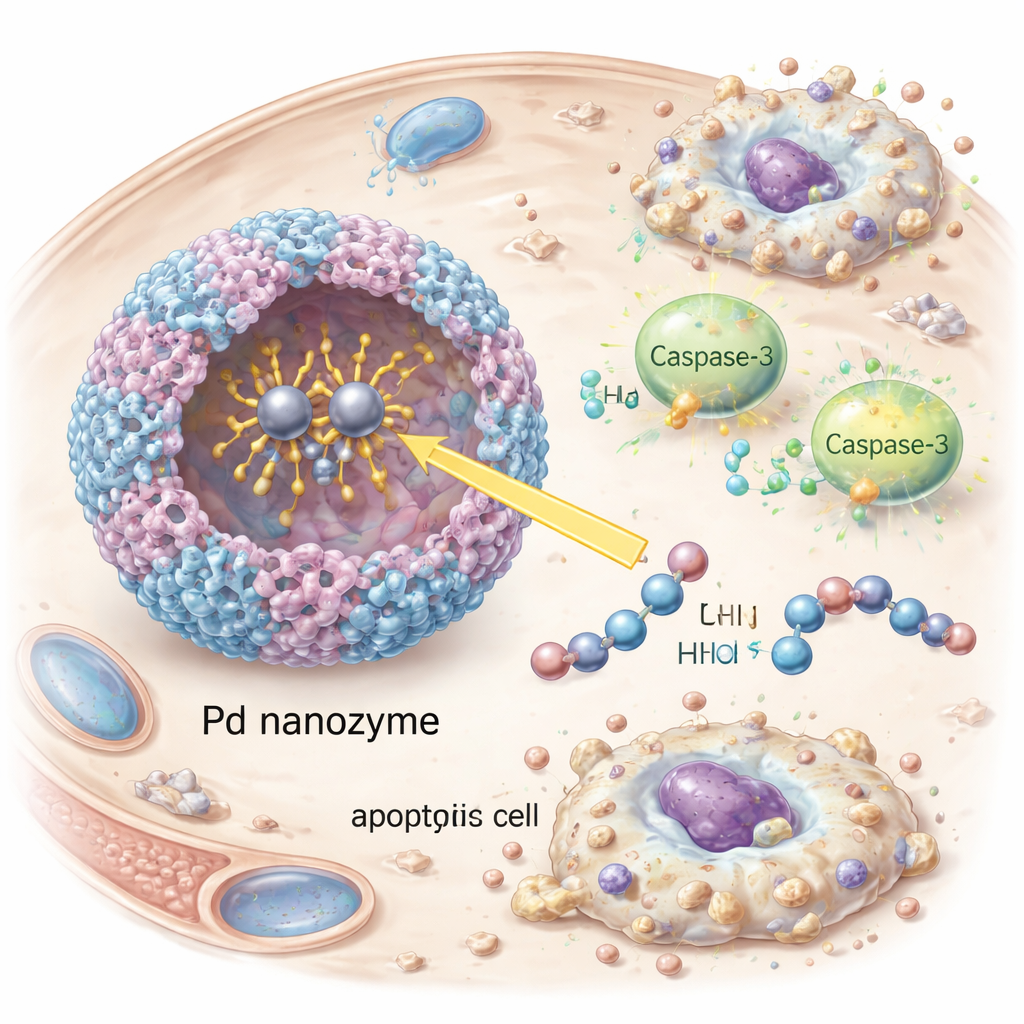
Teamet utgick från ferritin, ett naturligt protein som bildar ihåliga nanokapslar och som är enkelt att producera i stora mängder. Genom att binda palladiumjoner till human ferritin skapade de ett ”nanozym” med enzymliknande beteende. Noggranna strukturella studier visade att två palladiumatomer sitter i en specifik ficka på proteinets yta, hållna på plats av svavel‑ och kväveinnehållande aminosyror och vattenmolekyler. Detta binukleära metallcentrum fungerar som en artificiell klyvningssite som känner igen samma korta sekvens som granzyme B använder på ett avgörande mål känt som caspas‑3. I laboratorietester klippte nanozymet effektivt caspas‑3 på rätt ställe och aktiverade det, samtidigt som näraliggande besläktade proteiner ignorerades. Det artificiella enzymet var något mindre effektivt än naturligt granzyme B men märkbart mer stabilt över ett brett spektrum av temperaturer och pH‑värden.
Smyga in nanozymet i tumörceller
Enzymer som granzyme B fungerar bara om de når insidan av tumörceller. För att åstadkomma detta paketerade forskarna sitt palladium–ferritin‑nanozym inuti lipida nanovesiklar — små, mjuka bubblor gjorda av fettliknande molekyler. De klädde sedan dessa vesiklar med fragment av antikroppar som känner igen HER2, ett protein som ofta överproduceras på bröst‑ och blåscancerceller. När dessa kamouflerade vesiklar stöter på HER2‑rika celler binder de hårt och smälter samman med cellmembranet, vilket tillåter nanozym‑lasten att glida rakt in i cytoplasman i stället för att fastna och brytas ner i cellens återvinningskompartment. Mikroskopi visade vesiklar som dröjde vid cellytan medan nanozymet diffunderade in i insidan, vilket förberedde scenen för kontrollerad självdestruktion inifrån.
Att utlösa cancercellsjälvmord med precision
När nanozymet väl var inne i cancercellerna aktiverade det caspas‑3, en central effektor i programmerad celldöd. Forskarna observerade framträdandet av aktiverat caspas‑3 och dess nedströmsmål PARP, samt tydliga tecken på apoptos — celler som krymper och fragmenteras — i odlade HER2‑positiva tumörceller. Att stänga av caspas‑3 med RNA‑interferens minskade celldöd dramatisk, vilket bekräftade att effekten berodde på denna väg snarare än på ospecifikt skador. Hos möss med HER2‑positiva tumörer cirkulerade de antikroppsdekorerade vesiklarna längre i blodomloppet, ackumulerades starkare i tumörer och bromsade tumörtillväxten mer effektivt än vesiklar som saknade antingen målinriktande antikroppar eller nanozym‑last. Viktigt är att de behandlade djuren inte visade uppenbar viktminskning, blodavvikelser eller vävnadsskador i stora organ, vilket tyder på en fördelaktig säkerhetsprofil i dessa tidiga tester.
Vad detta kan betyda för framtidens cancervård
För icke‑specialister är huvudbudskapet att forskarna har byggt en liten, icke‑levande enhet som beter sig som en nyckelkomponent i vårt immunsystems cancerdödande maskineri. I stället för att konstruera levande T‑celler har de konstruerat ett stabilt nanoenzym som aktiverar samma självmordsknapp inne i tumörceller och inneslutit det i ett smart leveransskal som söker upp specifika cancerformer. Mycket arbete återstår innan mänsklig användning, men detta angreppssätt erbjuder en flexibel plattform: i princip kan antikroppsskiktet bytas ut för att rikta in sig på andra tumörmarkörer, och det artificiella enzymet kan vidareoptimeras. Studien visar en lovande väg mot cellfri immunterapi, där noggrant utformade nanomaterial, snarare än levande immunceller, används för att spåra och förstöra solida tumörer.
Citering: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Nyckelord: cancer-nanomedicin, immunterapi, granzyme B, nanozym, HER2-positiva tumörer