Clear Sky Science · sv
Reaktiva syreradikaler‑aktiverad bioortogonal kemi i levande system möjliggjord av boronat‑inkapslade dihydrotetraziner
Att förvandla cellstress till en exakt strömbrytare
Många sjukdomar, från cancer till hjärtsjukdomar, präglas av celler under oxidativ stress som producerar höga nivåer av reaktiva syreradikaler, till exempel väteperoxid. Denna studie visar hur kemister kan utnyttja just den här stressen som en inbyggd strömbrytare för att slå på kraftfulla behandlingar endast där de behövs. Genom att utforma läkemedelskomponenter som reagerar endast i dessa stressade miljöer försöker forskarna döda tumörceller eller förstöra skadliga proteiner samtidigt som friska vävnader skonas.
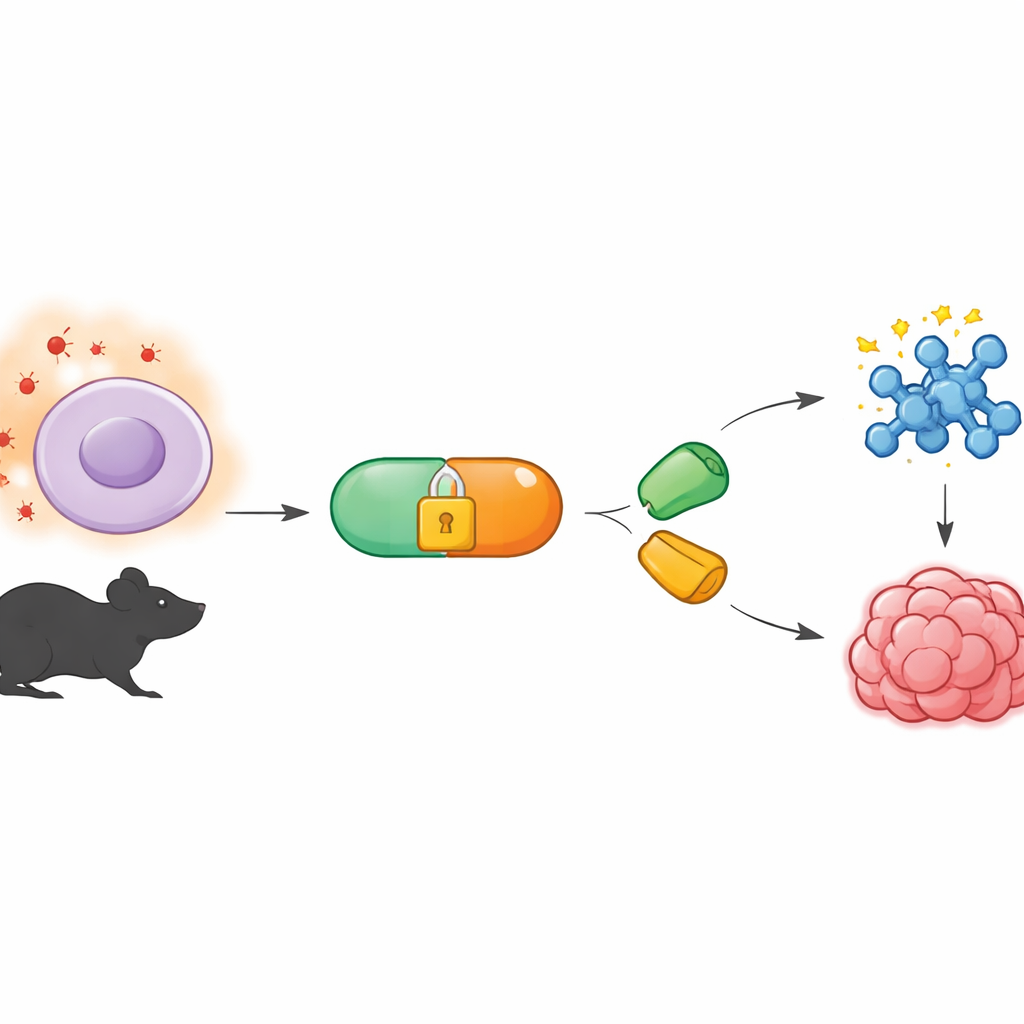
Ett kemiskt verktyg som arbetar diskret i bakgrunden
Arbetet bygger vidare på ett fält kallat bioortogonal kemi, som utvecklar reaktioner som kan ske inne i levande organismer utan att störa normal biologi. En populär variant använder särskilda molekylpar som hakar i varandra som pusselbitar, även i en cells trånga inre. En partner, kallad tetrazin, reagerar mycket snabbt med en matchande ”ring”‑partner, känd som en dienofil. Fram tills nu har många av dessa reaktioner styrts genom ljus eller tillsats av enzymer. Författarna ville istället ha ett system som lyssnar på kroppens egna kemiska signaler—specifikt de ovanligt höga nivåerna av reaktiva syreradikaler som finns i tumörer och annan sjuk vävnad.
Att bygga en ROS‑känslig kemisk utlösare
För att åstadkomma detta skapade teamet tetrazin‑prekursorer som de kallar BTz, vilka är kemiskt ”inkapslade” så att de förblir inaktiva i normala vävnader. Kapseln är uppbyggd av en boronatgrupp kopplad till en reducerad form av tetrazin. När väteperoxid är knappt förekommande är BTz stabil i vatten och i cellkulturer under många timmar. Men när väteperoxid är riklig—på nivåer liknande dem som mäts i tumörer—oxideras boronatgruppen och faller isär genom en självnedbrytande sekvens, vilket blottar den aktiva tetrazinen. I provrörsexperiment ledde stegvisa ökningar av väteperoxidkoncentrationen till en motsvarande ökning av mängden aktiv tetrazin som bildades, vilket bekräftar att reaktionen är både selektiv och starkt dosberoende.
Att utnyttja cellstress för att förgöra ett cancerdrivande protein
Forskarna använde först sin strömbrytare för att kontrollera en modern läkemedelsstrategi kallad riktad proteinnedbrytning. De kopplade BTz till talidomid, en liten molekyl som kan rekrytera ett enzymkomplex ansvarigt för att märka proteiner för bortstädning. I cancerceller förblev detta BTz–talidomid vilande tills väteperoxidnivåerna höjdes, varvid kapseln öppnades och en aktiv tetrazin bildades. Denna tetrazin reagerade sedan med en matchande partner bunden till ett BRD4‑bindande läkemedel och monterade en större ”kimer” som drog det cancerrelaterade proteinet BRD4 till cellens avfallsapparat. I lung‑ och livmoderhalscancercellinjer sjönk BRD4‑nivåerna kraftigt endast när alla delar fanns närvarande och väteperoxid var tillgängligt; att blockera reaktiva syreradikaler förhindrade nedbrytning, vilket understryker att processen verkligen aktiveras av stress.
Att leverera ett giftigt läkemedel endast där det behövs
Nästa steg var att omvandla samma kemi till ett precist leveranssystem för doksorubicin, ett potent men hjärtskadande cytostatika. De kopplade doksorubicin till en spänd ringpartner så att det låstes i en inaktiv prodrug‑form. När denna prodrug mötte BTz i en väteperoxidrik miljö reagerade den nyligen bildade tetrazinen med ringen i en ”click‑to‑release”‑process, vilket förband delarna och frigjorde fritt doksorubicin. I odlingar av koloncancerceller dödade detta tvåstegs‑system celler nästan lika effektivt som den fria substansen, men endast när väteperoxid var närvarande; utan den förblev cellerna till större delen oskadda. En enklare väteperoxidkänslig prodrug av doksorubicin var mindre effektiv och mindre selektiv i dessa tester, vilket framhäver fördelen med att separera sensning och frisättning i två koordinerade steg.
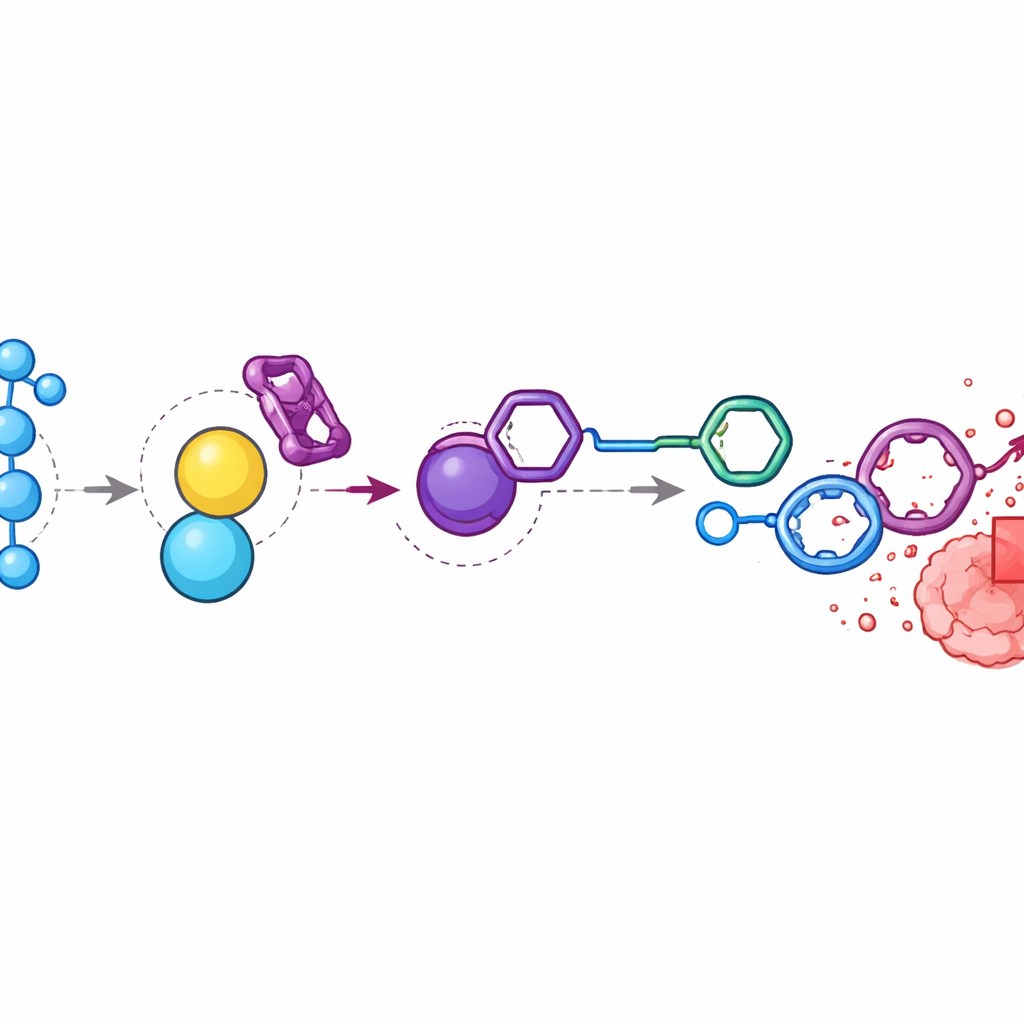
Att fokusera cytostatika inne i tumörer
I möss med kolonstumörer fann forskarna att väteperoxidnivåerna i tumörer var nästan nio gånger högre än i omgivande muskelvävnad. De injicerade doksorubicinline prodrug och BTz i en tidsmässigt styrd följd så att båda samlades nära tumören. Kemisk analys visade att komponenterna till stor del försvann från blodbanan och organen men genererade höga nivåer av fritt doksorubicin inne i tumörerna. Jämfört med djur som fick standarddoksorubicin visade de som behandlades med det aktiverade systemet liknande eller bättre tumörinvolution men bibehöll stabil kroppsvikt och undvek den svåra toxicitet som ses vid högre läkemedelsdoser. När teamet bröt väteperoxid‑signalen genom att injicera katalas, ett enzym som avlägsnar väteperoxid, minskade läkemedelsfrigöring och tumörselektiv ackumulering kraftigt, vilket bekräftar att oxidativ stress vid tumörplatsen är den avgörande drivkraften.
Från stressignal till precisionsbehandling
Sammantaget visar denna studie en mångsidig kemisk plattform som omvandlar ett kännetecken för sjukdom—överskott av reaktiva syreradikaler—till en exakt reglage för kraftfulla reaktioner inne i levande system. Genom att hålla den reaktiva tetrazinhanden låst tills den stöter på väteperoxid, gör tillvägagångssättet det möjligt för forskare att bygga komplexa terapier inne i kroppen endast där de behövs, vare sig för att demontera ett cancerfrämjande protein eller för att släppa ett giftigt läkemedel inne i en tumör. Eftersom oxidativ stress också spelar roller i åldrande, inflammation, diabetes och neurodegenerativa sjukdomar kan liknande stress‑responsiva reaktioner så småningom anpassas för många tillstånd där precision och säkerhet är avgörande.
Citering: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Nyckelord: bioortogonal kemi, reaktiva syreradikaler, tetrazin‑ligering, riktad läkemedelsleverans, PROTAC