Clear Sky Science · sv
Homotypisk membrandriven elektrochemisk mikrofluidisk analys av extracellulära vesiklar för noggrann cancerdiagnostik
Att förvandla cancerens egen rustning till ett diagnostiskt verktyg
Membranen som omger cancerceller är fyllda med karaktäristiska molekylära ”flaggor”. Denna studie visar hur forskare kan avlägsna den rustningen, sprida den över små guldytor och använda den för att fånga ut karakteristiska partiklar från blodet. Resultatet är ett mycket känsligt blodprov som kan avslöja inte bara om bröstcancer föreligger, utan även vilken undertyp det rör sig om — information som är avgörande för att välja rätt behandling.
Varför bröstcancerundertyp spelar roll
Bröstcancer är inte en enda sjukdom. Tumörer delas in i undertyper som östrogenreceptor‑positiv (ER+), HER2‑positiv och trippelnegativ, som alla svarar olika på hormonbehandling, riktade läkemedel eller cytostatika. I dag bestämmer läkare oftast undertyp från ett vävnadsprov taget direkt från tumören. Den proceduren är invasiv, kan inte utföras ofta och kan missa förändringar som sker när sjukdomen utvecklas. Ett blodbaserat test som kan följa dessa undertypssignaturer över tid skulle låta läkare justera behandlingen tidigare och mer precist.
Små budbärare som flyter i blodet
Cancerceller avsöndrar ständigt nanoskaliga blåsor kallade extracellulära vesiklar (EV) till blodomloppet. EV bär proteiner, lipider och genetiskt material som starkt liknar deras modercellers, vilket gör dem till attraktiva kandidater för ”flytande biopsier”. Men det finns en utmaning: EV från olika bröstcancerundertyper kan se mycket lika ut om man bara fokuserar på en eller två proteiner. Befintliga tester riktar sig antingen mot delade markörer — vilket gör det svårt att skilja undertyper — eller förlitar sig på komplexa genetiska analyser som är långsamma och kan ge missvisande resultat. Författarna ville läsa av ett fylligare molekylärt fingeravtryck på EV‑ytor på ett enkelt och robust sätt.
Att bygga ett biomimetiskt fisknät
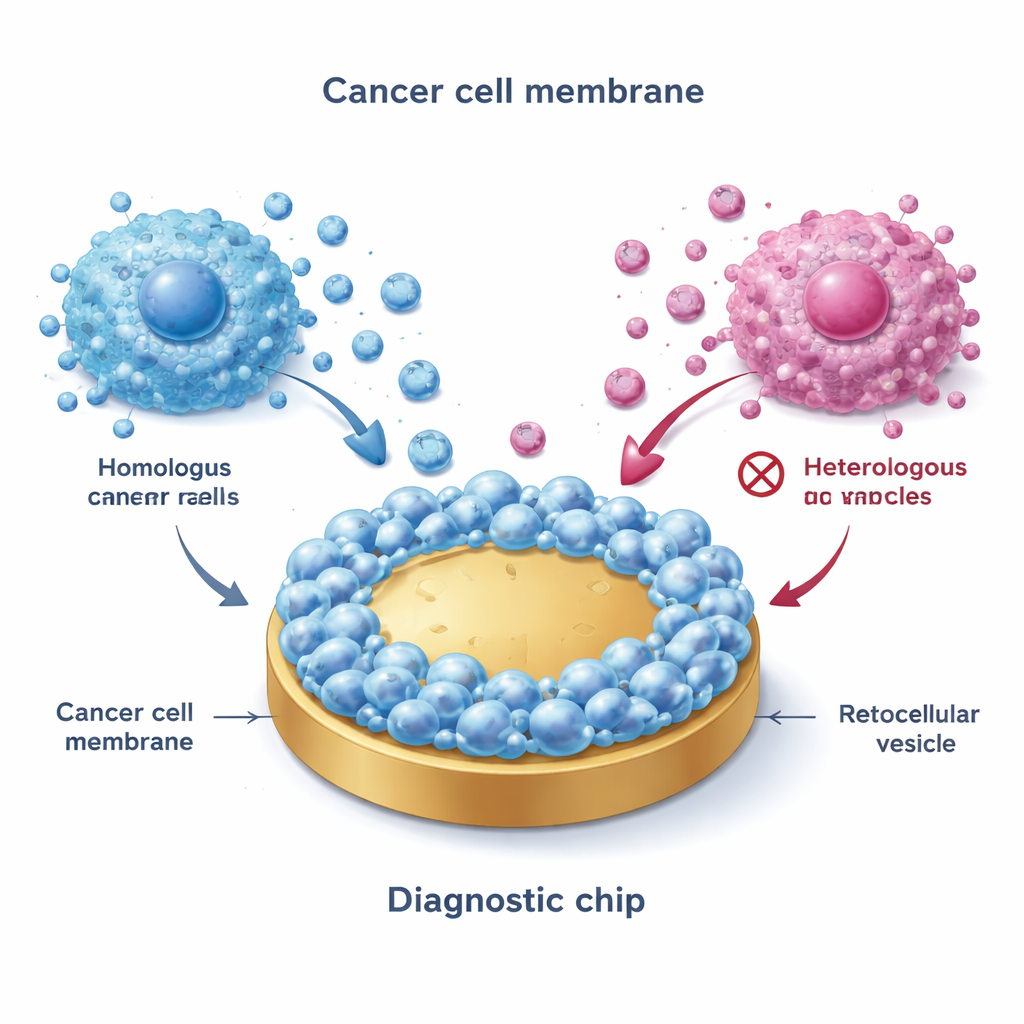
Forskargruppen började med att skörda membraner från odlad bröstcancerceller som representerar huvudtyperna: ER+ (som MCF‑7), HER2‑positiv och trippelnegativ. Genom en frysnings‑tögnings‑process bröt de upp cellerna, isolerade yttermembranen och fusionerade dessa membraner på platta guldytor. Detta skapade ett ”biomimetiskt gränssnitt” som nära efterliknar utsidan av de ursprungliga cancercellerna. Anmärkningsvärt var att när EV flödades över dessa belagda ytor fastnade endast vesiklar från matchande eller närbesläktade cancerundertyper starkt — ett fenomen kallat homotypiskt bindande. Avancerad avbildning och elektriska mätningar bekräftade att membranförsedda ytor var grövre, mer hydrofila och mycket mindre benägna att nonspecifikt binda partiklar än naket guld, vilket gör dem väl lämpade för rena mätningar i komplexa vätskor som blod.
Att omvandla fångande av vesiklar till en elektrisk signal
För att göra bindningen mätbar riktade forskarna in sig på ett rikligt förekommande protein kallat CD47 på EV‑ytan. De fäste CD47‑antikroppar på silvernanopartiklar med en kort DNA‑bro, och skapade små elektroaktiva taggar. När det membranförsedda underlaget hade fångat sina föredragna EV, hakade dessa taggar fast vid CD47 på de bundna vesiklarna. Vid exponering för en sur lösning och därefter elektrokemisk mätning gav silvret en skarp, lätt kvantifierbar ström. Signalstyrkan ökade linjärt över ett brett spektrum av EV‑koncentrationer, ner till bara några hundra vesiklar per milliliter — betydligt känsligare än vanliga metoder som ELISA‑kit eller nanopartikelspårning. Varje typ av cancermembran gav en stark signal endast med sina matchande EV, även i närvaro av vesiklar från andra undertyper, blodplättar eller orelaterade celler.
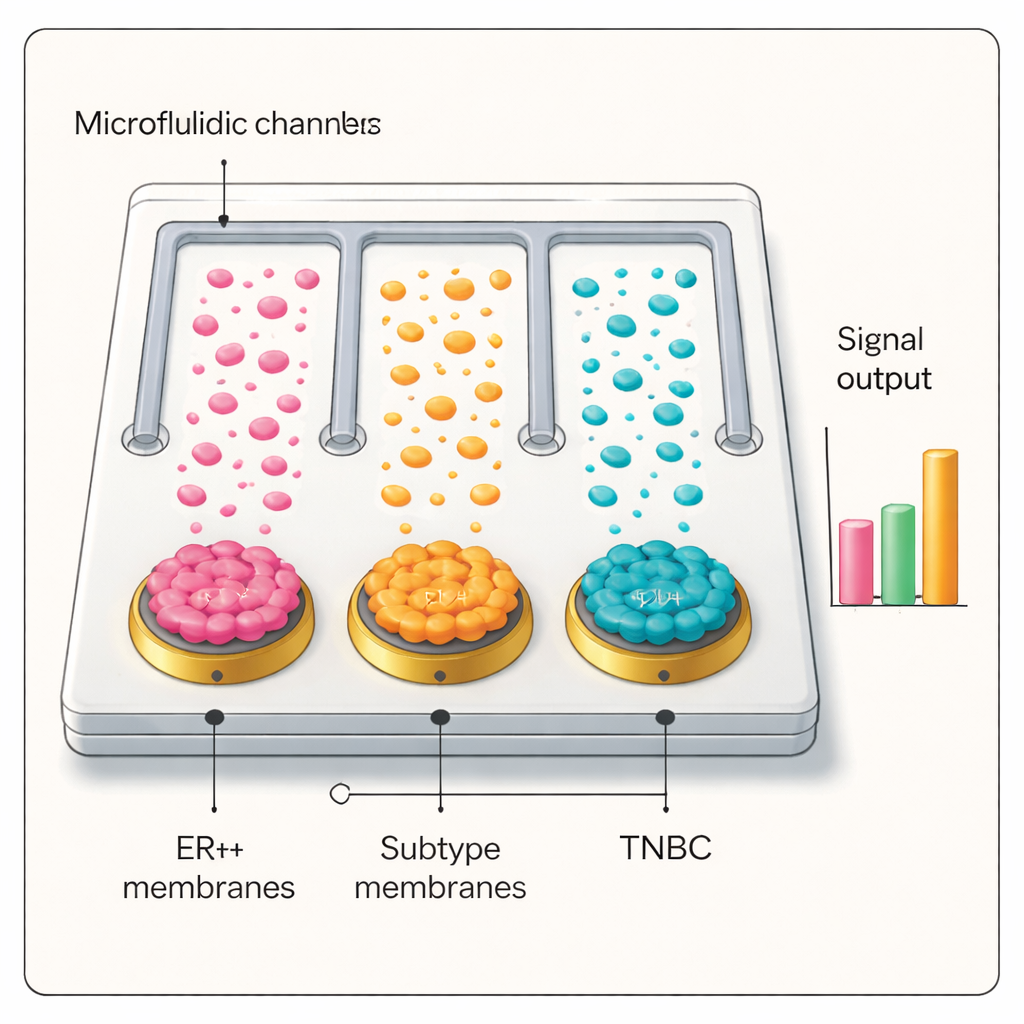
Från laboratoriebänk till patientprover
Med detta selektiva och känsliga gränssnitt byggde teamet ett mikrofluidiskt chip med parallella kanaler, där varje kanal var belagd med ett annat bröstcancercellmembran, plus en obelagd kontrollkanal. När patientplasman fördes genom chippet och proverades med silver‑antikroppstaggarna, gav bara kanalen vars membran matchade patientens tumörundertyp en hög elektrisk signal. I blinda tester med flera dussin personer — inklusive ER+ och trippelnegativa bröstcancerpatienter, individer med godartad bröstsjukdom, lungcancerpatienter och friska frivilliga — skiljde plattformen korrekt cancer från icke‑cancer och identifierade rätt bröstcancerundertyper. Diagnostisk prestanda motsvarade eller överträffade standardpatologi i många fall och visade potential för att stadieindela sjukdomen och följa dess progression.
Vad detta kan innebära för framtidens cancervård
Enkelt uttryckt har forskarna förvandlat cancerens eget yttre skal till ett mycket selektivt bete för de små partiklar som tumörer släpper ut i blodet. Genom att läsa den elektriska signaturen av vilken kanal som ”lyser upp” skulle läkare en dag kunna avgöra inte bara om cancer finns utan vilken typ det är — med bara ett blodprov. Systemet behöver fortfarande vidareutveckling — till exempel genom att lägga till fler markörer och fler membrantyper samt integrera smart dataanalys — men det pekar mot en framtid där rutinmässiga, minimalt invasiva blodtester hjälper till att styra skräddarsydd cancerbehandling och övervaka hur tumörer förändras över tid.
Citering: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Nyckelord: bröstcancerundertyper, flytande biopsi, extracellulära vesiklar, mikrofluidisk diagnostik, cellmembransensorer