Clear Sky Science · sv
Cyklande molekylära assemblage för bildbehandling och störning av Golgi
Gör cellens distributionscentral till ett strategiskt mål
Inne i varje djurcell finns Golgiapparaten, en upptagen sorteringsstation som färdigställer, packar och skickar tusentals proteiner och fetter. Många cancerceller är starkt beroende av denna knutpunkt för att modifiera tillväxtsignaler och utsöndra faktorer som formar deras omgivning. Denna artikel presenterar små designade molekyler som söker sig till Golgi, lyser upp den för snabb avbildning och, när de omkonstrueras, selektivt kan störa dess funktion för att försvaga cancerceller samtidigt som vissa friska celler skonas.
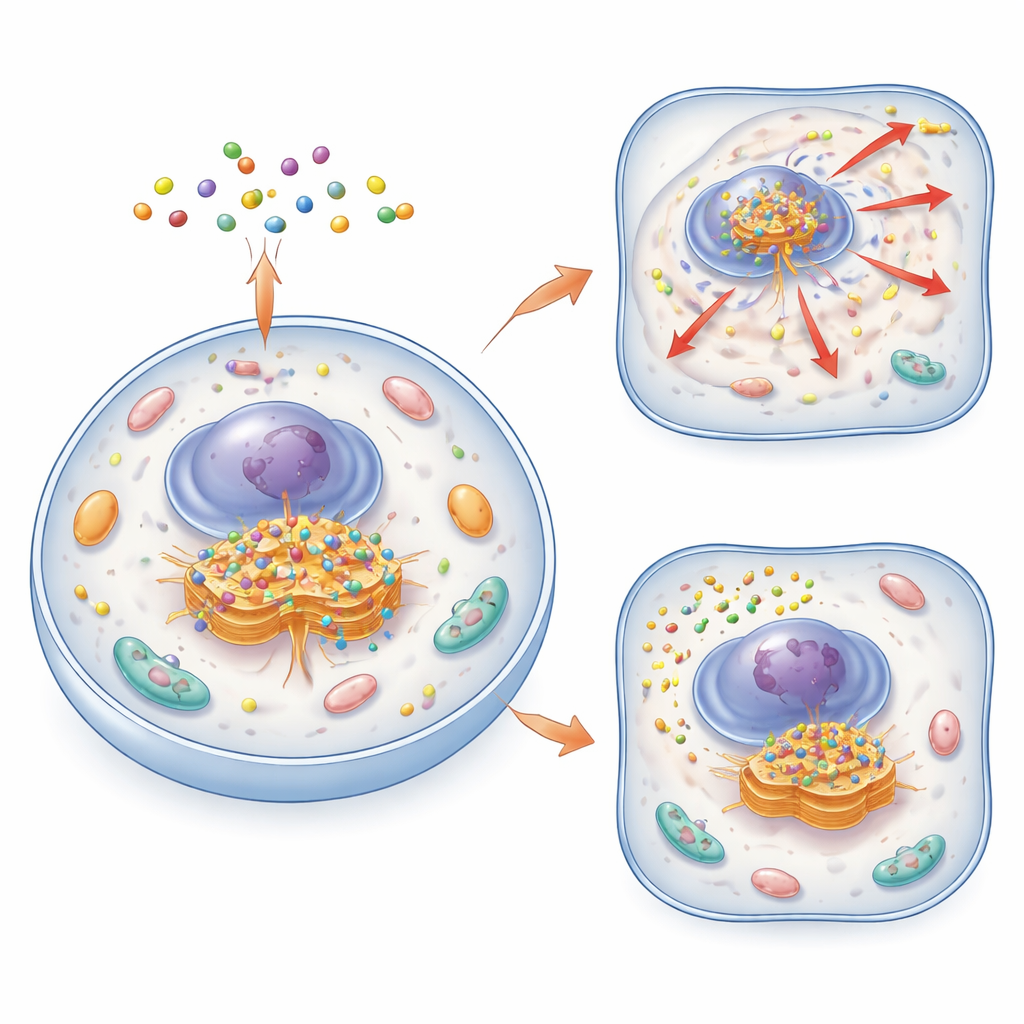
Ett nytt sätt att hitta och övervaka Golgi
Författarna skapade en familj små, smarta molekyler kallade cyklande molekylära assemblage, eller CyMA. Dessa molekyler byggs upp av korta peptider som både kan ta sig igenom cellmembran och klibba ihop sig till små kluster. I deras ”avbildnings”-version (CyMA‑i) bär peptiderna en fluorescerande färg som lyser starkt när molekylerna samlas. När de väl är inne i en cell klipper enzymer av ett skyddande lock från CyMA‑prekursorn och blottar ett reaktivt handtag. Golgi‑lokaliserade enzymer fäster sedan en fet kedja på detta handtag, vilket gör molekylerna mycket mer klibbiga och benägna att självmontera just vid Golgi. Eftersom denna process är snabb och använder cellens egna maskineri kan forskarna skissera Golgis form i levande celler inom minuter och vid mycket låga sonderingskoncentrationer.
En fåfänglig cykel som fäster molekyler vid Golgi
CyMA är inte bara markörer; de är designade för att delta i en ”fåfänglig cykel” vid Golgi. En grupp enzymer fäster fetkedjor vid peptiden medan en annan grupp tar bort dem. I takt med att cellen upprepat lägger till och tar bort dessa kedjor fortsätter de modifierade peptiderna att montera och demontera på plats. Detta ständiga fram‑och‑tillbaka fångar en fast‑liknande kärna av assemblage på Golgi‑membran, samtidigt som enskilda molekyler cirkulerar genom systemet. Cellen måste kontinuerligt förbruka sina egna byggstenar av fettsyror för att upprätthålla denna loop, vilket i praktiken matar assemblagen och hjälper dem att bestå. Samtidigt kan andra enzymer långsamt klyva en särskild esterbindning i CyMA och omvandla dem till mer vattenälskande fragment som driver iväg. Eftersom vissa friska celler, som leverceller och vissa immunceller, är rika på sådana ester‑klyvande enzymer, är de naturligt bättre på att montera ner CyMA och påverkas därför mindre.
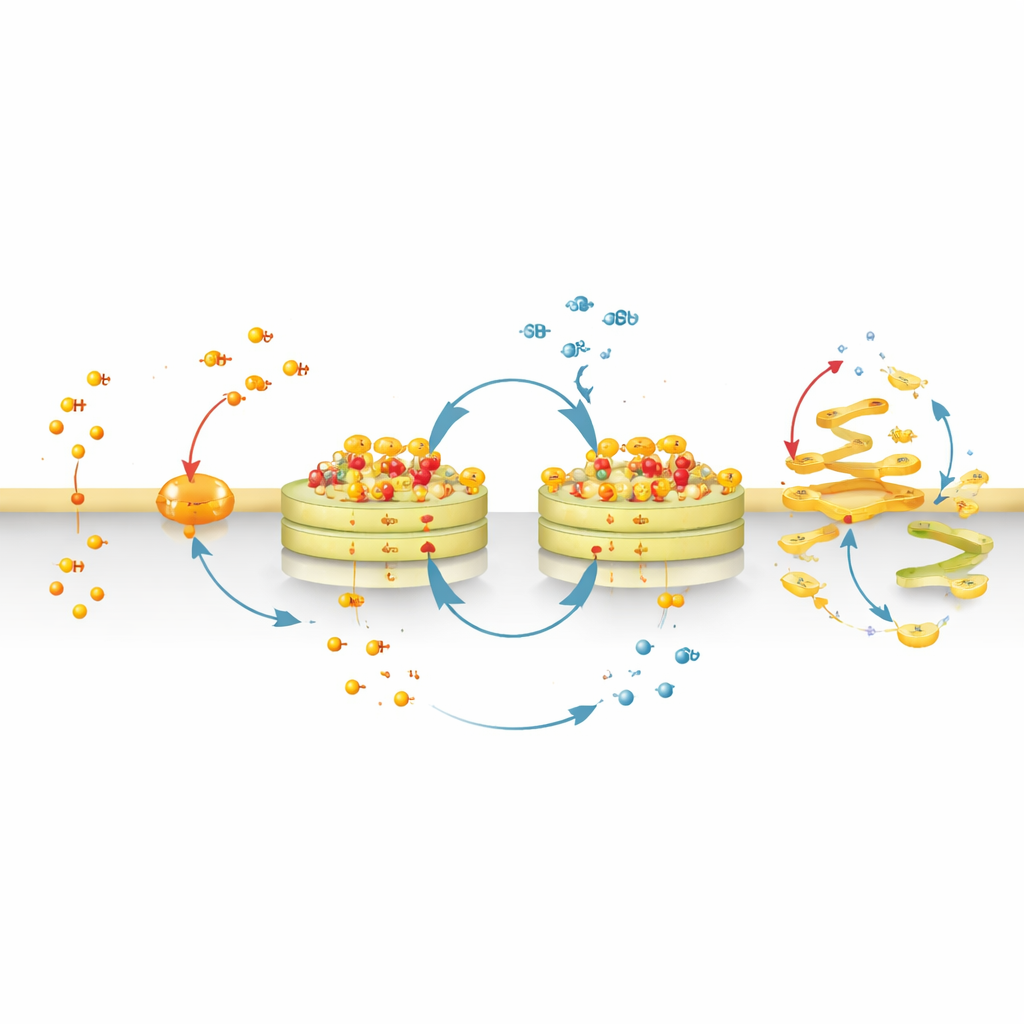
Från skonsamt avbildningsverktyg till Golgi‑störande medel
Genom att byta ut den fluorescerande färgen mot en mer membran‑sökande kemisk grupp omvandlade teamet CyMA‑i till CyMA‑d, en störande version som inte längre lyser men fortfarande cyklar och monterar vid Golgi. Dessa assemblage stör fysiskt Golgis struktur och det ständiga flödet av vesiklar till och från den. Proteiner som normalt färdas från det endoplasmatiska nätverket till Golgi och vidare ut till cellens yta fastnar eller felriktas. Inkommande vägar — från cellytan tillbaka till Golgi eller från Golgi till andra organeller — blockeras också. Som en följd når viktiga ytreceptorer och signalmolekyler antingen inte sina destinationer eller samlas på fel ställen inne i cellen.
Kvävning av signalsystem och sekretoriska budskap
Golgi är platsen där många proteiner får avgörande sista modifieringar, såsom socker‑kedjor och lipid‑svansar. CyMA‑d‑assemblage minskar korrekt lipidisering och glykosylering av många proteiner, inklusive välkända cancerdrivare som Ras och stora receptor‑tyrosinkinaser. Dessa förändringar ställer till det för tillväxtfrämjande banor som AKT och mTOR. Samtidigt dämpas cellens sekretoriska utsläpp: viktiga faktorer som TGF‑β1 och VEGF, som tumörer använder för att dämpa immunitet och stimulera blodkärlsbildning, frigörs inte längre effektivt. Stressen från detta sammanbrott utlöser ihoptrasslade nätverk i det endoplasmatiska retikulumet, förändrade mitokondrier, avstannad autofagi (cellens återvinningssystem) och en ökning av skadade, ubiquitin‑märkta proteiner, vilket tillsammans driver cancerceller mot död.
Selektivt tryck på tumörer och terapi‑löfte
Där CyMA‑d förlitar sig på en gemensam uppsättning enzymer och metaboliter som många cancerceller överanvänder, kan de döda ett brett spektrum tumörtyper, inklusive läkemedelsresistenta ovarialcancermodeller, vid mycket låga doser. Celler med höga nivåer av specifika esteraser demonterar däremot CyMA‑d lättare och påverkas mindre, vilket ger en inbyggd väg till selektivitet. I tredimensionella tumörspheroider, patient‑härledda kulturer och musmodeller krymper CyMA‑d tumörer, minskar metastaser och reducerar ansamling av vätska i buken. När de kombineras med immun‑checkpoint‑terapier förbättrar de dessutom tumörkontroll och överlevnad. I huvudsak visar arbetet att man genom att bygga dynamiska material inne i Golgi — snarare än att rikta in sig på ett enskilt protein — kan stänga ner flera processer som är avgörande för cancer samtidigt.
Vad detta innebär för framtida behandlingar
För en icke‑specialist är huvudidén att författarna har förvandlat Golgi från en passiv åskådare till ett aktivt terapeutiskt mål. Genom att rekrytera cellens egna enzymer att montera och återvinna små molekyler vid denna centrala knutpunkt kan de antingen ofarligt framhäva den eller gradvis överväldiga dess funktion. Denna dubbelanvändningsplattform föreslår en ny typ av behandling: i stället för att designa ett läkemedel för ett protein kan vi kanske konstruera små prekursorer som celler omvandlar till självorganiserande material, kapabla att störa hela kommunikations‑ och transportnätverk som tumörer förlitar sig på för att växa och sprida sig.
Citering: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Nyckelord: Golgiapparaten, molekylära assemblage, proteintransport, cancerterapi, organelletargeting