Clear Sky Science · sv
En stabiliserad tandemantigenkimera som framkallar potent malariatransmissions‑reducerande aktivitet
Varför det är viktigt att stoppa myggöverföring
De malariavacciner som används i dag kan kraftigt minska svår sjukdom och död bland små barn, men de lämnar en stor lucka: personer som inte känner sig sjuka kan fortfarande bära på parasiter som infekterar myggor och upprätthåller smittspridningen. Denna studie presenterar en nästa generations vaccinarkitektur avsedd inte bara att skydda en individ, utan att bryta kedjan av infektion mellan människor och myggor. Genom att noggrant konstruera hur nyckelproteiner från parasiten visas för immunsystemet vill forskarna framkalla antikroppar som gör myggor till dåliga värdar för malaria och hjälper samhällen att närma sig eliminering.
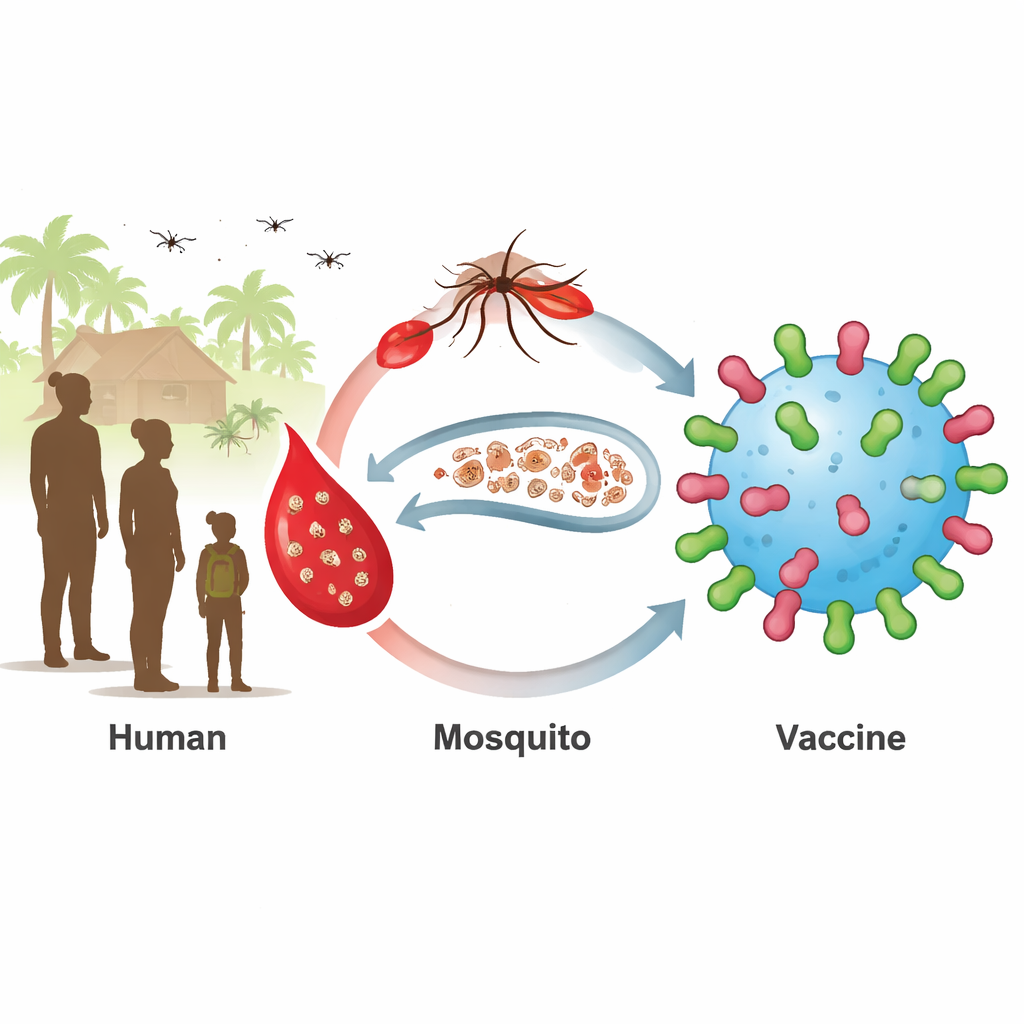
Ett dolt reservoar som håller malarian vid liv
Dagens malariavacciner riktar in sig på den tidiga infektionsfasen i levern och blodet. De fungerar bäst hos små barn, men äldre barn och vuxna bär ofta på mogna sexuella stadier av parasiten, så kallade gametocyter, utan symptom. När myggor bitar dessa personer plockar de upp parasiterna och sprider dem vidare. Två parasitytproteiner, kända som Pfs230 och Pfs48/45, sitter på dessa sexuella stadier och är attraktiva mål för så kallade transmissions‑blockerande vacciner. Vacciner mot fragment av dessa proteiner har nått kliniska prövningar, men de har haft svårt att framkalla starka och varaktiga antikroppssvar hos alla mottagare.
Att bygga en smartare lockbete för immunsystemet
För att förbättra tidigare designer använde författarna en strukturell biologisk ansats och studerade i atomär detalj hur potenta humana antikroppar binder Pfs230 och Pfs48/45. De identifierade små regioner, eller epitoper, som är särskilt effektiva för att blockera parasitutveckling i myggor. Lika viktigt kartlade de ”icke‑funktionella” epitoper som lockar antikroppar som binder men inte stoppar transmissionen—i praktiken ett slöst immunsvar. Med hjälp av datorbaserad modellering och proteiningenjörsverktyg sammanfogade de den mest potenta regionen från Pfs230 (dess första domän) med den nyckelregion från Pfs48/45 (dess tredje domän) i ett enda, omsorgsfullt ordnat protein som de kallar en stabiliserad tandemantigenkimera, eller STAC.
Gömma de värdelösa målen, behålla de användbara
Utmaningen var att visa upp dessa två domäner tillsammans på ett sätt som efterliknar hur de sitter på parasiten, samtidigt som man fysiskt döljer de icke‑funktionella ytor som normalt är begravda i det intakta proteinet. Teamet redesignade iterativt den korta länken och gränsytan mellan de två domänerna och testade varje version för stabilitet, korrekt veckning och om den fortfarande band en panel av välkaraktäriserade antikroppar. Avancerad designmjukvara föreslog mutationer som stramade upp gränsytan och förbättrade uttrycket i odlade celler. Strukturella studier med hjälp av röntgenkristallografi, småvinkel‑röntgenspridning och kryoelektronmikroskopi bekräftade att i den slutliga STAC‑konstruktionen visas de önskade epitoperna med hög trohet medan de kända oönskade ytorna är steriskt blockerade.
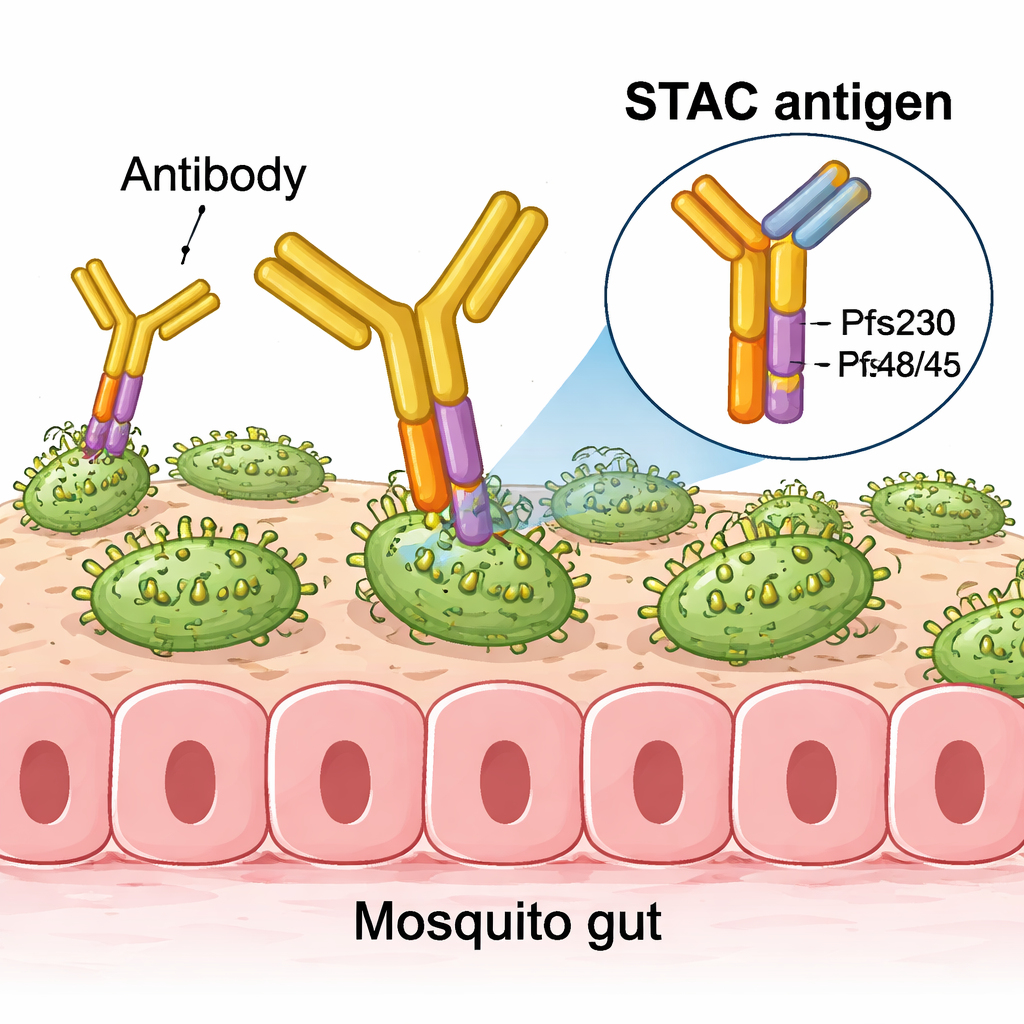
Från enskilda molekyler till kraftfulla nanopartiklar
Tester i möss visade att när STAC fästes på specialiserade liposomer eller på självmonterande protein‑nanopartiklar framkallade det starka antikroppssvar som kraftigt reducerade parasitutveckling i standardiserade myggmatnings‑tester. Vid lika eller lägre doser matchade eller överträffade STAC ofta vacciner som använde Pfs230‑ och Pfs48/45‑fragment separat, oavsett om de gavs ensamma, blandade tillsammans eller samsynliggjorda på samma partikel. I mycket känsliga tester där musserum utspäddes många gånger bibehöll antikroppar framkallade av STAC‑dekorerade nanopartiklar transmissions‑reducerande aktivitet bättre än de från andra formuleringar, vilket indikerar särskilt potenta och fokuserade responser.
Vad detta kan betyda för malaria‑bekämpning
För icke‑specialister är huvudidén att STAC är ett specialbyggt lockbete som visar immunsystemet exakt de delar av malariaparasiten som är viktigast för att blockera spridning, samtidigt som distraherande regioner som inte hjälper döljs. I djurmodeller ger denna design antikroppar som försvårar för parasiter att fullborda sin livscykel i myggor, även när antikroppsnivåerna är relativt låga. Om liknande resultat uppnås hos människor kan STAC bli en kraftfull partner till befintliga malariavacciner: genom att skydda vaccinerade individer från sjukdom samtidigt som det krymper det infektösa reservoaret i samhället. Mer generellt visar arbetet hur detaljerad strukturell insikt och proteiningenjörskonst kan användas för att utforma flerdelade vacciner som är potenta, stabila och potentiellt billigare att tillverka.
Citering: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Nyckelord: malariavacciner, transmissionsblockering, Pfs230, Pfs48/45, nanopartikelimmunogen