Clear Sky Science · sv
NONO‑HOXA1‑Wnt‑axelns avgörande roll vid differentiering till hjärtmuskelceller
Varför små hjärtceller betyder något för oss alla
Varje hjärtslag förlitar sig på miljarder specialiserade muskelceller som bildas i livmodern. När den processen går fel kan barn födas med allvarliga hjärtfel. Denna studie använder mänskliga stamceller för att avslöja ett avgörande styrsystem — byggt av molekylerna NONO och HOXA1 och en välkänd signal kallad Wnt — som hjälper tidiga celler att bestämma sig för att bli frisk hjärtmuskel. Att förstå denna dolda krets kan så småningom leda till bättre diagnostik och behandling av medfödd hjärtsjukdom.
Från tomt blad till tidiga hjärtbyggare
Forskarna började med mänskliga inducerade pluripotenta stamceller — mångsidiga celler som kan ledas att bli nästan vilken celltyp som helst. Med en standardprotokoll styrde de dessa celler att differentiera till kardiomyocyter, hjärtats slagande celler. När NONO‑genen togs bort antog betydligt färre celler en hjärtidentitet. Nyckelmarkörer som normalt uppträder när celler lämnar sitt primitiva tillstånd och går mot hjärtlinjen var kraftigt reducerade. Enkelcells‑RNA‑sekvensering visade att många NONO‑defekta celler fastnade halvvägs, kvar i ett omoget mesendoderm‑liknande tillstånd istället för att utvecklas till fullvärdiga hjärtmuskelceller.
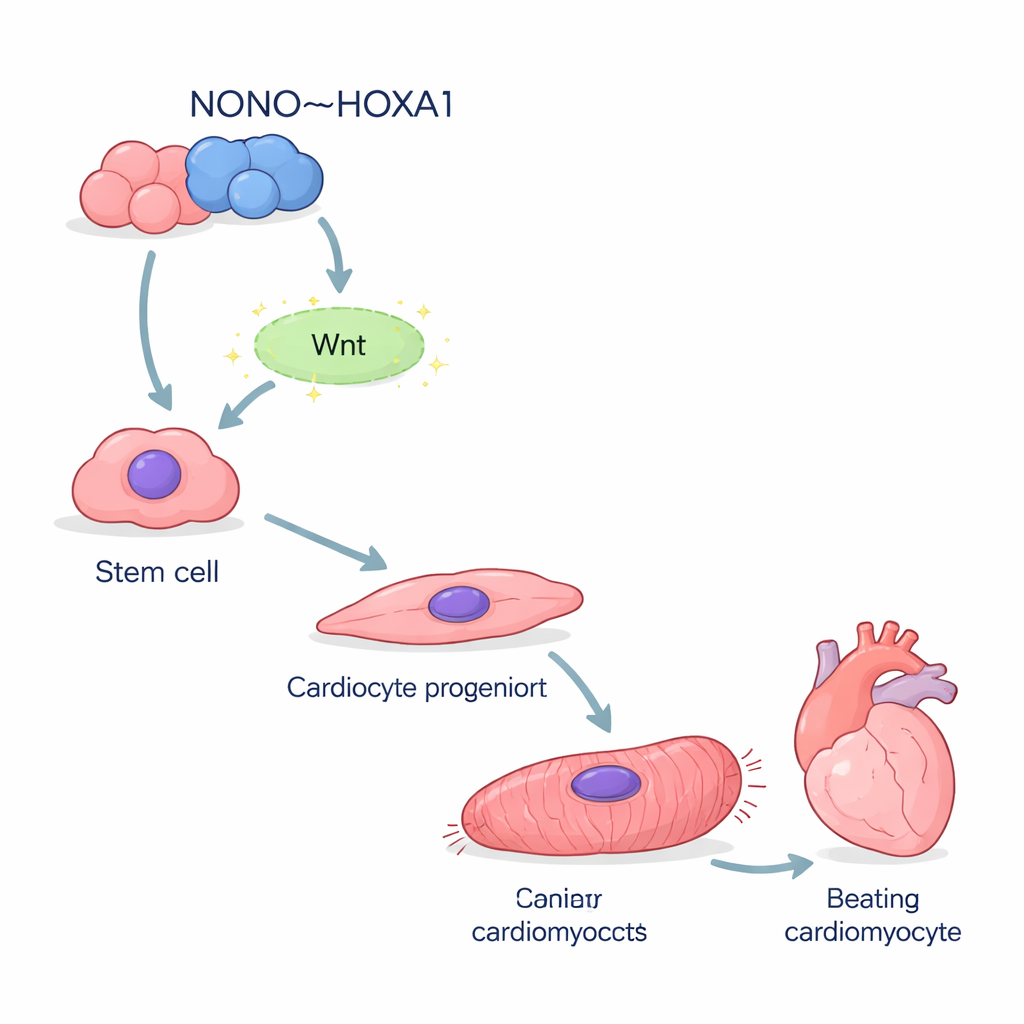
När stommen saknas svajar hjärtcellerna
De celler som ändå blev kardiomyocyter utan NONO var långt ifrån friska. De uttryckte mycket lägre nivåer av strukturella proteiner som bygger sarkomeren, den mikroskopiska apparaten som driver kontraktion. Under mikroskop visade de flesta mutantceller röriga, fragmenterade kontraktila fibrer istället för de prydliga ränderna som ses i normala celler. Elektronmikroskopi bekräftade att de vanliga Z‑disken, ”trappstegen” i den kontraktila strukturen, saknades eller var missbildade. Funktionellt slog dessa celler långsammare och oregelbundet. Mätningar av kalciumböljor — elektriska händelser som triggar varje hjärtslag — visade ryckiga vågformer med fördröjda toppar och långsam återhämtning, vilket speglar genuttrycksdefekter i kalciumhanterande kanaler.
Återställning av utvecklingen och avslöjande av NONO–HOXA1‑samarbetet
För att testa om dessa problem verkligen berodde på förlust av NONO återinförde teamet NONO på ett kontrollerat, läkemedelsinducerbart sätt under de första två dagarna av differentiering. Denna korta puls av NONO återställde till stor del ökningen av tidiga hjärtgener, ökade andelen slagande hjärtceller och byggde upp organiserade sarkomerer och Z‑diskar igen. Genuttrycksprofilering bekräftade att många gener för muskelkontraktion och hjärtutveckling återgick mot normala nivåer. Patient‑härledda muterade varianter av NONO kunde däremot inte rädda fenotypen, vilket stödjer idén att sådana varianter orsakar sjukdom genom att störa detta tidiga program. Protein‑interaktionsförsök visade sedan att NONO fysiskt binder en transkriptionsfaktor kallad HOXA1, och att denna kontakt stabiliserar HOXA1 och hjälper den att bilda dimerer som behövs för att greppa DNA.
Att slå på Wnt‑signalen för att bestämma hjärtödet
Kartan över var dessa proteiner binder i genomet visade att NONO och HOXA1 ofta upptar samma regulatoriska regioner, inklusive sådana som styr viktiga tidiga hjärt‑ och Wnt‑vägsgener. När NONO saknades försvagades HOXA1:s bindning vid många av dessa platser, särskilt vid gener som driver precardiellt mesoderm — den tidigaste hjärtbildande vävnaden. Den nedströms Wnt/β‑catenin‑vägen, som normalt hjälper till att starta mesoderm- och hjärtutveckling, försvagades också: mindre β‑catenin ackumulerades i kärnan och Wnt‑responsiva reporter‑tester minskade. Att förstärka Wnt‑signalen med en högre dos av en Wnt‑aktiverande drog under de tidigaste dagarna av differentiering kunde delvis kompensera för avsaknaden av NONO, återställa fler hjärtceller och öka uttrycket av hjärtgener.
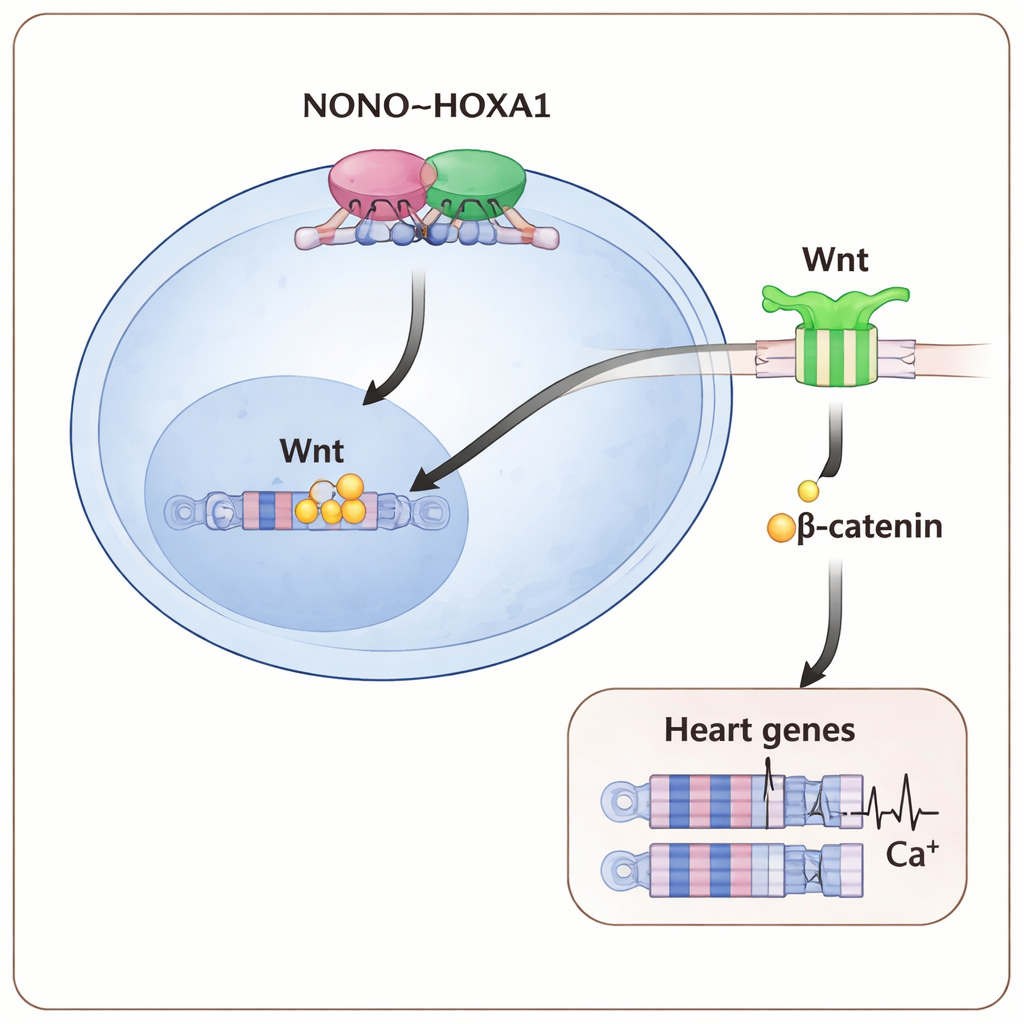
Vad detta betyder för förståelsen av medfödda fel
För icke‑specialister är huvudbudskapet att ett litet molekylärt team — NONO i samarbete med HOXA1 för att finjustera Wnt‑signaler — fungerar som en tidig ”trafikreglerare” som berättar för unga celler att bli hjärtmuskel och förser dem med vad som krävs för att slå korrekt. När någon del av denna NONO–HOXA1–Wnt‑axel störs tvekar cellerna, viktiga hjärtgener förblir avstängda och de resulterande kardiomyocyterna blir strukturellt och elektriskt sårbara. Dessa insikter erbjuder en tydligare molekylär förklaring till varför mutationer i NONO är kopplade till medfödda hjärtfel, och pekar på sätt att manipulera denna väg i stamcellsmodeller eller, en dag, i terapier inriktade på att förebygga eller reparera hjärtmissbildningar.
Citering: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Nyckelord: medfödd hjärtsjukdom, differentiering till hjärtmuskelceller, Wnt‑signalering, hjärtmodeller med stamceller, genreglering