Clear Sky Science · sv
Elektrografisk cue‑reaktivitet samlokaliseras med djup hjärnstimulering i nucleus accumbens vid en fallstudie av opioidberoende
Varför den här berättelsen är viktig
Opioidberoende är fortfarande en dödlig epidemi, och många människor fortsätter att kämpa med starka drogsug trots läkemedel och rådgivning. Den här artikeln berättar historien om en ung man vars behandlingsteam inte bara använde en hjärnimplantat för att stimulera hans hjärna, utan också för att lyssna på den. Genom att hitta en specifik elektrisk signal kopplad till hans opioidsug kunde de finjustera hans djupa hjärnstimulering så att den fungerade bättre, med lägre effekt, och hjälpte honom att förbli drogfri.
Att lyssna på suget
Patienten var en 25‑årig man med en lång historia av svår opioidberoende, som började tidigt i tonåren, samt depression, ångest och andra komplikationer. Standardbehandlingar, inklusive mycket höga doser metadon, hade inte hållit hans sug under kontroll. År tidigare hade han fått djup hjärnstimulering (DBS) i ett djupt liggande område i hjärnan kallat nucleus accumbens, en central nod för motivation och belöning. Med denna stimulering påslagen sjönk hans sug och han förblev abstinent från opioider i flera år. När en kirurgisk komplikation tvingade läkarna att ta bort hans batteri återkom dock suget inom veckor och risken för återfall ökade kraftigt. Detta skapade en ovanlig möjlighet: hans hjärnelektrod kunde tillfälligt kopplas till extern inspelningsutrustning, vilket gjorde det möjligt för forskarna att direkt mäta hjärnaktivitet medan han upplevde sug.
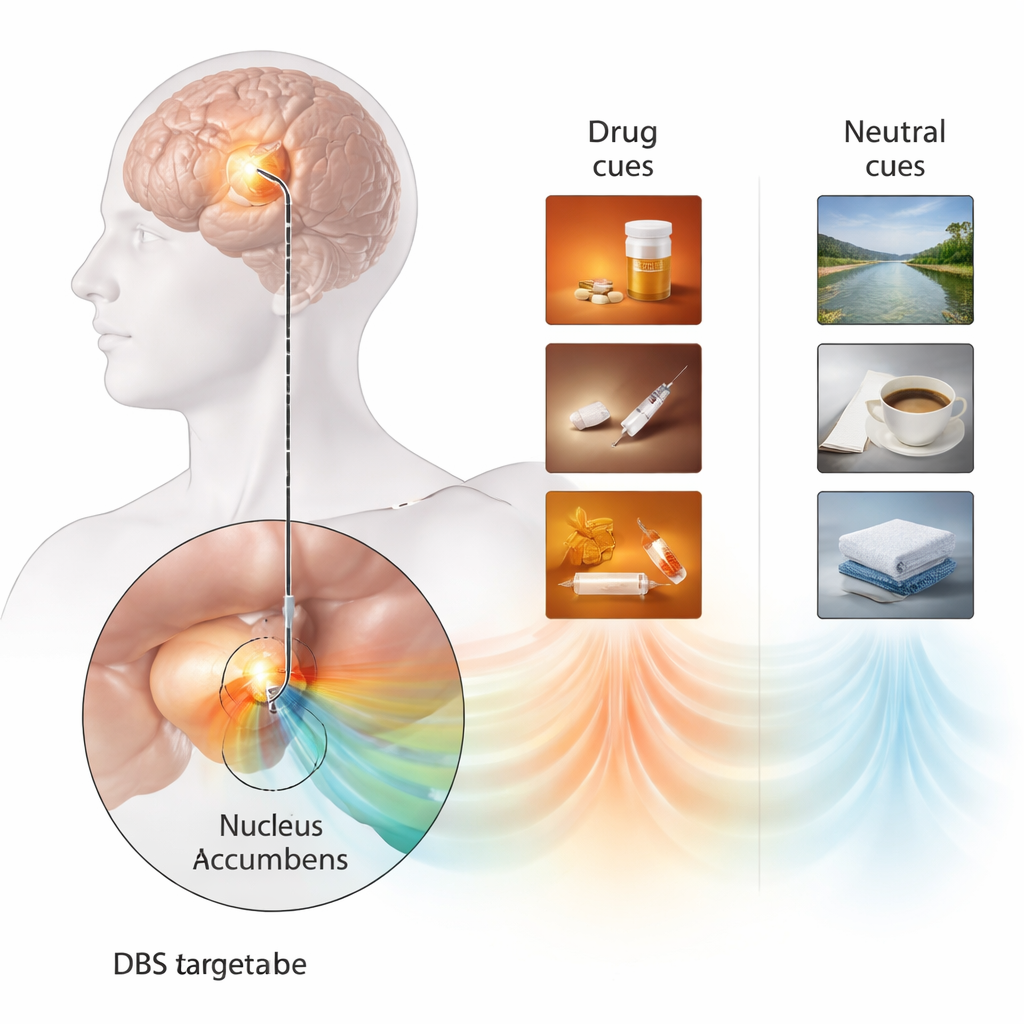
Personliga triggers avslöjar en hjärnsignal
För att fånga hur sug ser ut i hjärnan byggde teamet upp ett mycket personligt cue‑reaktivitetstest. Istället för generiska drogbilder skapade de korta videoklipp som noggrant återspeglade hans tidigare drogbruk—hans föredragna opioid, sprututrustning och förberedelseritualer—och kontrasterade dessa med lugna naturscener. Efter varje sexsekundersklipp bedömde han hur stark hans lust att använda opioider kändes. Samtidigt användes DBS‑ledningen i hans nucleus accumbens som en liten mikrofon och spelade in de lokala elektriska rytmerna i hans hjärna. När drogvideorna visades framträdde en distinkt låg‑frekvent rytm (i 1–6 Hz‑området) i den ventrala delen av nucleus accumbens, ett område som antas motsvara ”shell”‑subregionen. Denna signal var mycket svagare vid neutrala videor och syntes inte i andra delar av elektroden. Viktigt var att högre effekt i denna rytm korrelerade med högre självrapporterat sug, vilket tyder på att det var en direkt hjärnmarkör för drogcues‑reaktivitet snarare än en allmän signal för upphetsning eller uppmärksamhet.
Att förvandla stimulering till ett riktat verktyg
Den avgörande följdfrågan var om stimulering på just den platsen kunde dämpa den sugrelaterade hjärnrytmen och det begär den speglade. Teamet testade systematiskt olika kontaktpar på elektroden och frågade i realtid om sug, humör och biverkningar medan de gradvis ökade stimuleringsstyrkan. Det ventrala kontaktparet i nucleus accumbens shell framträdde som den optimala platsen: det gav stark lindring av sug och förbättrat humör vid relativt låg ström, med minimala biverkningar. Mer dorsala kontaktpar, i en närliggande fiberbunt kallad anteriora lemniscus interna capsula, hjälpte också men krävde mycket starkare stimulering och gav obehagliga känslor. Med ledning av dessa tester upprepade forskarna sedan cue‑reaktivitetstestet samtidigt som de levererade korta stimulanser till nucleus accumbens shell före varje video. Under detta ”stimulerade” tillstånd trycktes den tidigare förhöjda 1–6 Hz‑rytmen under drogcue ned mot neutrala nivåer, och hans genomsnittliga sugpoäng sjönk med mer än hälften.
Varaktig förändring med en lättare beröring
Utrustade med denna konvergerande bevisning—från anatomi, hjärnsignaler och beteende—programmerade klinikerna permanenta inställningar i hans implanterade enhet för att stimulera fokalt inom nucleus accumbens shell vid en mycket lägre ström än tidigare. Under de följande sex månaderna rapporterade han varaktiga minskningar både i frekvensen och intensiteten av opioidsug, bibehållen avhållsamhet och uppfyllda kriterier för tidig remission, utan större förändringar i humör, ångest eller energi. Nätverksmodellering av hjärnan visade att de nya inställningarna aktiverade en mindre, mer fokuserad vävnadsvolym samtidigt som de engagerade en nyckelväg mellan nucleus accumbens och ett område under pannloberna som är involverat i känslor och värdering. Eftersom stimuleringen var mer effektiv minskade också batterikrävningarna markant—en viktig fördel för en ung patient som sannolikt kommer att behöva långvarig behandling.
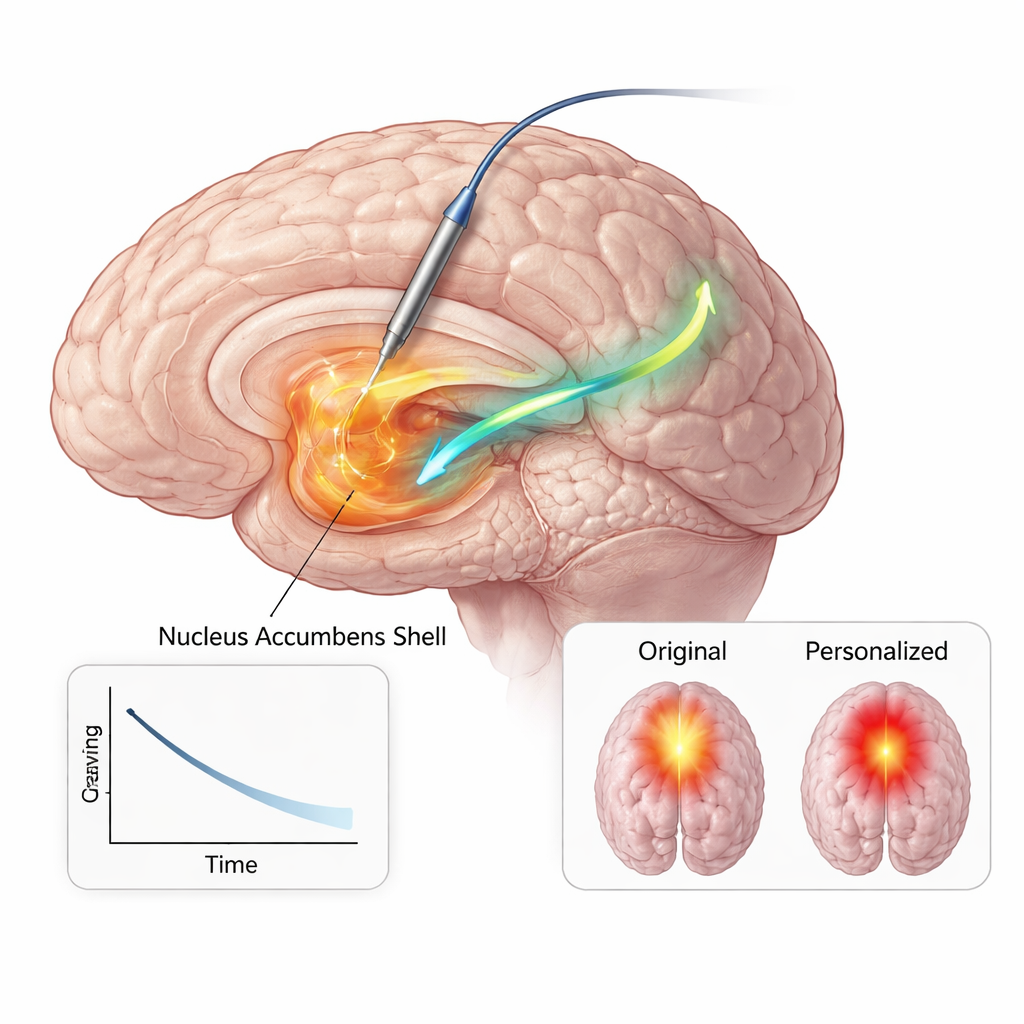
Vad detta kan betyda för framtida vård
Detta N‑of‑1‑fall bevisar inte att samma tillvägagångssätt kommer att fungera för alla med opioidberoende, men det fungerar som ett principbevis. Det visar att i åtminstone en individ följde en specifik elektrisk rytm i ett belöningscentrum noggrant opioidsug och att den kunde tystas med precis riktad stimulering, vilket ledde till bestående symtomlindring med lägre elektrisk dos. Enkelt uttryckt lärde sig teamet att ”stämma” stimulatorn efter patientens egen sugsignal. Om liknande hjärnmarkörer kan hittas och följas hos fler personer, och om enheter som både känner av och stimulerar blir mer tillgängliga, kan framtida behandlingar skräddarsy hjärnstimulering för beroende—agera när sugbanaer flammar upp och potentiellt hjälpa människor att ligga steget före återfall.
Citering: Qiu, L., Nho, YH., Seilheimer, R.L. et al. Electrographic cue-reactivity co-localizes with accumbens deep brain stimulation in a case of opioid use disorder. Nat Commun 17, 1708 (2026). https://doi.org/10.1038/s41467-026-68758-w
Nyckelord: opioidberoende, djup hjärnstimulering, nucleus accumbens, hjärnbiomarkörer, drogsug