Clear Sky Science · sv
Strukturell grund för gaffelreversering och RAD51-reglering av SCF-ubiquitinligas-komplexet hos F-box-helicas 1
Hur celler räddar en fastkörd DNA-kopieringsmaskin
Varje gång en cell delar sig måste den snabbt och noggrant kopiera miljarder DNA-bokstäver. Men den här kopieringsmaskineriet stöter ofta på problem — DNA-skador, svårkopierade sekvenser eller läkemedelsbehandlingar kan få processen att stanna. När det händer förlitar sig celler på akuta reparationslag för att stabilisera och starta om replikeringsgafflarna. Denna artikel avslöjar, i hittills osedda strukturella detalj, hur en sådan insatsledare — ett proteinkomplex byggt kring helicaset FBH1 — omformar fastlåst DNA och håller ett annat nyckelreparationsprotein, RAD51, under strikt kontroll. Att förstå denna koreografi hjälper till att förklara hur celler undviker farlig genombrott och varför störningar i dessa faktorer är kopplade till cancer.
En trafikstockning på DNA-motorvägen
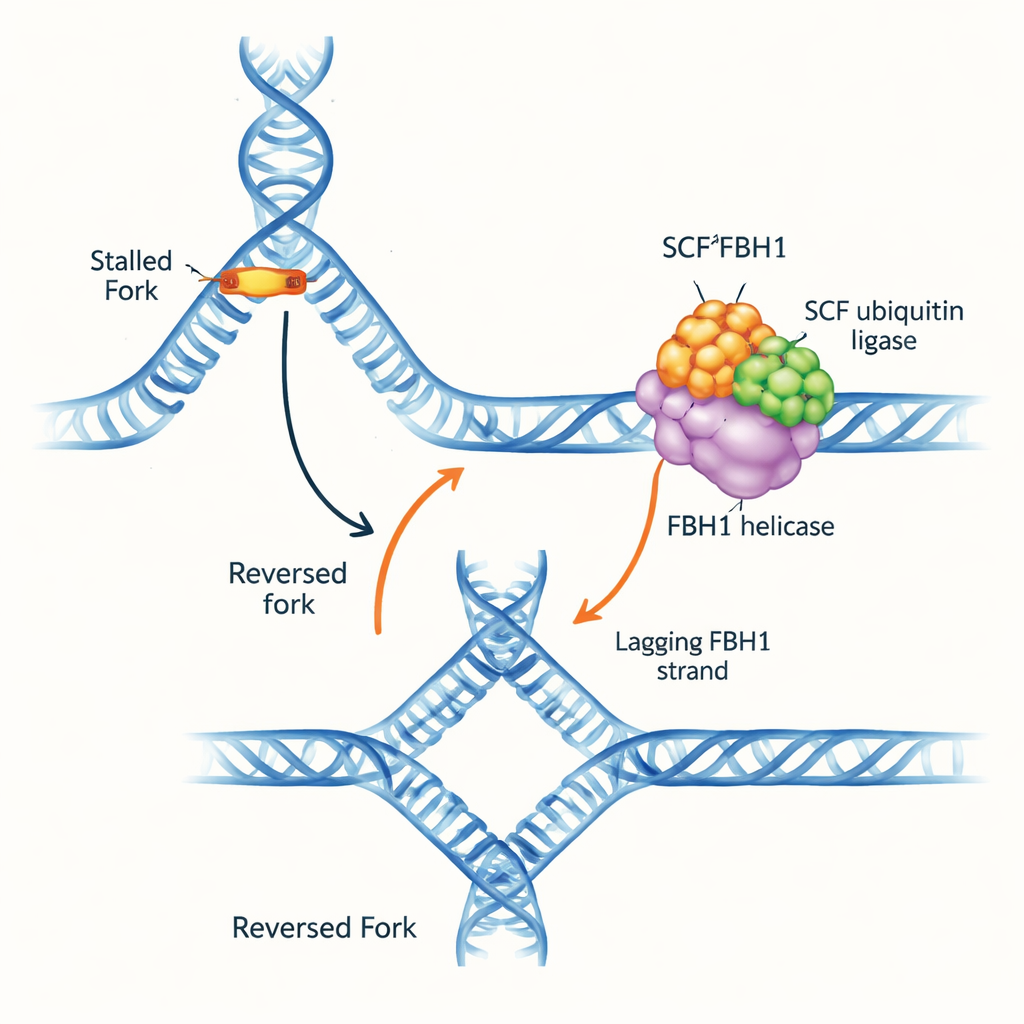
DNA-replikeringsgafflar är Y-formade strukturer där dubbelhelixen öppnas och kopieras. När gaffeln stöter på hinder kan den vända riktning: föräldrasträngarna tvinnas om igen och de nybildade strängarna parar ihop sig med varandra och bildar en fyrvägs DNA-förgrening. Denna ”gaffelreversering” kan vinna tid för reparation och säker omstart av replikationen, men om den hanteras fel kan den också skapa skört DNA som går sönder. Flera molekylära motorer är kända för att trycka gafflar bakåt genom att gripa dubbelsträngat DNA framför gaffeln. FBH1 stack dock ut eftersom det uppträdde annorlunda och ofta förändras i tumörer, vilket tyder på att det arbetar via en distinkt och medicinskt viktig väg.
En gaffelspecialist med en favoritssida
Författarna renade det humana SCFFBH1-komplexet, som kombinerar FBH1-helicaset med en ubiquitin‑märkande modul (SCF). De undersökte först vilka DNA-former FBH1 föredrar. Med hjälp av bindnings- och upplösningsanalyser visade de att SCFFBH1 starkt favoriserar verkliga gaffelliknande strukturer, särskilt där det finns ett kort stycke enkelsträngat DNA på den ”laggande” templatesträngen — den sida som kopieras i små fragment. På dessa strukturer upplöses DNA hundratals gånger snabbare än vid en enkel lös ände, vilket indikerar att korrekt engagemang vid gaffelns korsning kraftigt förstärker dess motoraktivitet. Enkelmolekylära magnettänger bekräftade att komplexet kan upplösa och sedan förflytta sig längs enkelsträngat DNA i tusentals nukleotider utan att lossna, vilket gör det till en kraftfull, processiv motor.
Att reversera gaffeln genom att dra bakifrån
För att ta reda på hur denna motor faktiskt reverserar gafflar testade teamet artificiella gaffelsubstrat med eller utan enkelsträngiga luckor. Till skillnad från andra gaffelomformare kunde SCFFBH1 inte agera på en fullständigt paread gaffel; det krävde en lucka på den laggande templatesträngen och rörde sig i 3′–5′ riktning längs den enkelsträngen. Denna ”dragning bakifrån”-rörelse driver föräldrasträngarna att återpara sig medan enzymet förblir klämt vid gaffelns korsning. En cryo‑elektronmikroskopistruktur av SCFFBH1 bundet till en fastnat gaffel visar hur: en särskild positivt laddad ficka, ett ”korsningsbindningsmotif” i en subdomän av FBH1, lägger sig precis vid förgreningspunkten där de tre DNA‑armarna möts. När forskarna muterade två nyckelaminosyror i detta motiv sjönk gaffelreverseringen ungefär 25‑falt i provrör, men den grundläggande upplösningsmotorn fungerade ändå hyfsat. I celler förhindrade samma mutation den normala förlångsamningen av replikeringsgafflar som svar på ett stressframkallande läkemedel — ett kännetecken för misslyckad gaffelreversering.
En dubbel roll: omforma DNA och avlägsna RAD51
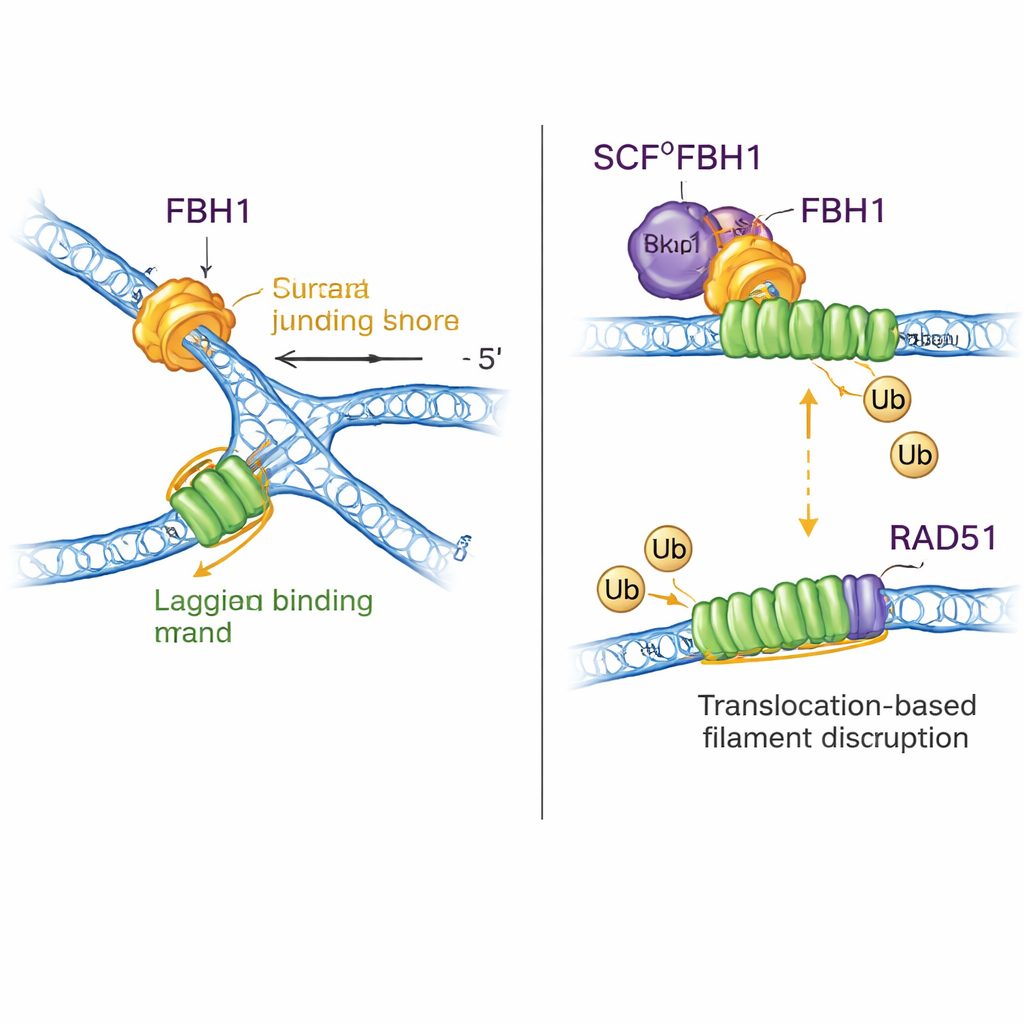
FBH1 är inte bara en motor; genom SCF‑komplexet hjälper det också till att fästa små ubiquitin‑taggar på proteiner. De nya strukturerna sätter ihop nästan hela SCFFBH1–DNA‑komplexet och visar att ubiquitin‑överförings"huvudet" i ligaset sitter mindre än 45 ångström från den laggande strängs DNA som lämnar FBH1. Genom att docka in kända strukturer av andra ubiquitinligaser föreslår författarna att denna geometri placerar RAD51 — ett enzym som bildar filament på DNA för att främja rekombination — rakt i skottlinjen på den laggande strängen vid en fastnad gaffel. Tidigare arbete visade att FBH1 kan mekaniskt ta bort RAD51 från DNA och även märka det med ubiquitin så att det inte lätt binder om. Den nya modellen förenar dessa idéer: när FBH1 drar längs den laggande strängen för att omforma gaffeln kan den närliggande SCF‑modulen märka RAD51‑enheter, vilket hjälper till att montera ner eller förhindra överdrivna RAD51‑filament som annars skulle kunna blockera korrekt gaffelhantering.
Vad detta betyder för genomstabilitet och cancer
Tillsammans visar studien att SCFFBH1 reverserar fastnade DNA‑replikeringsgafflar med en mekanism som skiljer sig från andra kända gaffelomformare: det griper förgreningspunkten hårt samtidigt som det translocerar längs den laggande templaten bakifrån och främjar säker återupprullning av föräldrarnas DNA utan att bilda en långlivad, rörlig fyrvägsförgrening. Samtidigt är dess inbyggda ubiquitinligas strategiskt placerad för att avlägsna RAD51 från samma sträng, vilket förhindrar okontrollerad rekombination under replikationsstress. Eftersom FBH1 ofta förloras eller muteras i cancer förklarar dessa strukturella och mekanistiska insikter hur sådana tumörer ackumulerar DNA‑skador och varför de kan svara annorlunda på läkemedel som framkallar replikationsstress eller riktar in sig på närliggande vägar.
Citering: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
Nyckelord: DNA-replikationsstress, gaffelreversering, FBH1-helicas, RAD51-reglering, genomstabilitet