Clear Sky Science · sv
Automatiserad kartläggning av DNA-replikationsgafflarnas framfart i mänskliga celler med ForkML
Varför det är viktigt att följa hur snabbt DNA kopieras
Varje gång en mänsklig cell delar sig måste den kopiera mer än tre miljarder DNA-bokstäver snabbt och noggrant. Om denna kopieringsprocess saktar ner eller stannar kan det skada genomet och bidra till cancer och utvecklingsstörningar. Ändå har forskare hittills saknat ett enkelt sätt att se exakt hur snabbt enskilda DNA:s "kopieringsmaskiner" rör sig längs specifika delar av mänskligt DNA. Den här artikeln presenterar ForkML, en ny teknik som använder nanopore-DNA-sekvensering och maskininlärning för att automatisera denna uppgift i en hittills oöverträffad skala.
Att iaktta cellens kopieringsmaskiner i realtid
DNA dupliceras av små molekylära maskiner kallade replikationsgafflar som rör sig längs dubbelhelixen och bygger nya strängar. ForkML låter forskare iaktta dessa gafflar indirekt genom att tillföra en ofarlig kemisk markör, BrdU, i nyligen syntetiserat DNA under två mycket korta pulser med en bestämd tidslucka däremellan. Eftersom BrdU kan upptäckas i enskilda DNA-molekyler med nanopore-sekvenserare ser forskarna två märkta "ränder" på varje DNA-sträng där en gaffel passerade under de två pulserna. Genom att mäta avståndet mellan ränderna och dividera med den kända tidsskillnaden kan de beräkna hur snabbt varje gaffel rörde sig i det området av genomet. 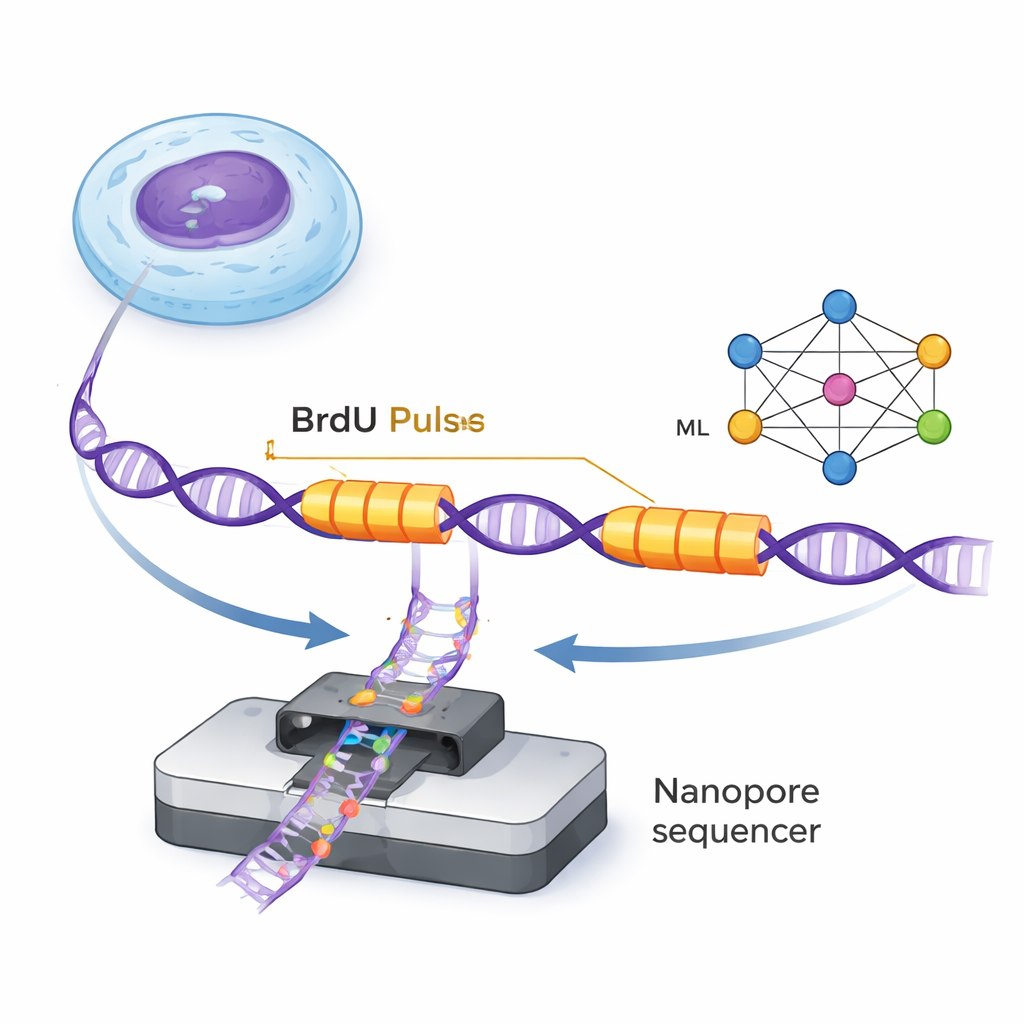
Att lära en dator att läsa de kemiska spåren
I tidigare arbete med jäst kunde författarna upptäcka dessa BrdU-spår med enkla regler, men i mänskliga celler är signalerna svagare och mer komplexa. Mänskliga experter kan fortfarande känna igen det karakteristiska mönstret — en brant ökning av BrdU när pulsen börjar, följt av en mjuk nedgång när den sköljs bort — men att göra detta för miljontals DNA-fragment för hand är omöjligt. ForkML löser detta genom att träna ett neuralt nätverk, en form av maskininlärning, på tusentals manuellt annoterade exempel. Modellen lär sig klassa varje DNA-segment som bakgrund eller som en höger- respektive vänsterrörande gaffel och att med hög noggrannhet fastställa början av varje BrdU-puls. Detta möjliggör fullständigt automatiserad kartläggning av tusentals enskilda gaffelhastigheter från en enda sekvenseringskörning.
Mäta stress och variationer över genomet
Genom att använda ForkML på en mänsklig koloncellslinje fick teamet över 2 000 mätningar av gaffelhastighet per experiment och fann att en typisk gaffel rör sig med ungefär 1,2 kilobaser per minut, i överensstämmelse med tidigare, lägre genomströmningmetoder. När de behandlade celler med läkemedel som är kända för att bromsa DNA-replikation upptäckte ForkML tydligt denna inbromsning, vilket visar att metoden känsligt kan mäta replikationsstress. Eftersom varje gaffel kartläggs tillbaka till sin position i referensgenomet kunde författarna sedan relatera hastighet till andra egenskaper, såsom när en region normalt replikerar under cellcykeln, hur tätt dess DNA är packat och hur aktivt det transkriberas till RNA. 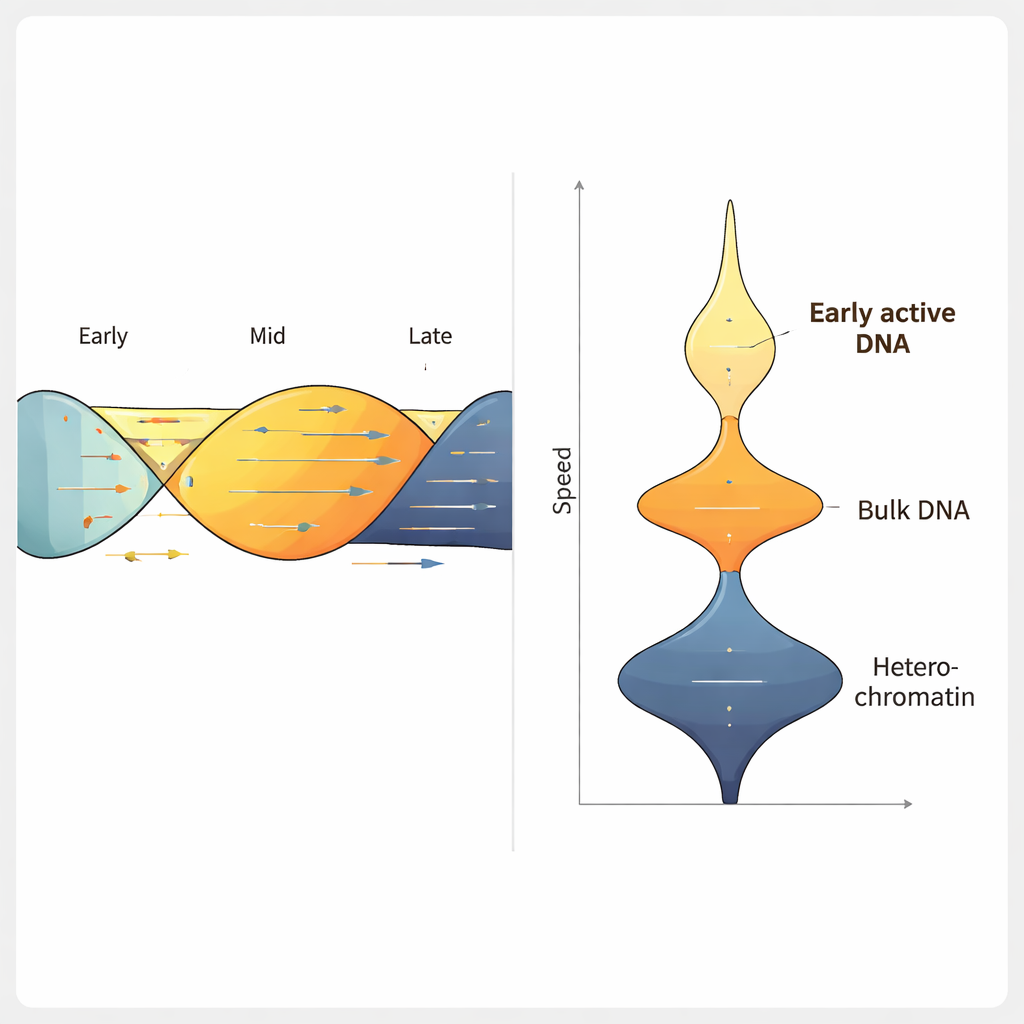
Visa var DNA-kopieringen börjar och hur strängarna skiljer sig
Utöver hastighet identifierar ForkML också var DNA-replikation startar och slutar genom att upptäcka punkter där gafflar divergerar eller konvergerar längs samma molekyl. Genom att kartlägga mer än 20 000 sådana startpunkter bekräftar författarna att mänskliga celler använder en blandad strategi: en del kopiering börjar i väldefinierade initieringszoner, men de flesta startar är utspridda över genomet. Genom att kombinera gaffelriktning med vilken DNA-sträng som lästs av sekvenseraren kan ForkML även skilja hastigheterna för ledande och eftersläpande strängsyntes, något traditionella fiberbaserade analyser inte kan göra. Tester över sex olika mänskliga cellinjer — både normala och cancerösa — visar att samma enkla BrdU-märkningsförhållanden fungerar brett och ger robusta hastighetsuppskattningar i varje fall.
En digital uppgradering av en klassisk metod
För icke-specialister kan ForkML ses som en modern, digital version av den klassiska DNA-fiberassayet: den använder ett liknande märkningsschema men ersätter manuell mikroskopi med långläsande sekvensering och maskininlärning. Detta ger mycket högre genomströmning, direkt placering av varje mätning på genomet och mer detaljerad information om var och hur snabbt DNA kopieras. Eftersom protokollet är enkelt, kompatibelt med nuvarande nanopore-hårdvara och anpassningsbart till andra organismer, är ForkML redo att bli ett standardverktyg för att studera DNA-replikation. I praktiska termer erbjuder det forskare ett kraftfullt sätt att koppla lokal DNA-kopieringshastighet — normal eller stressad — till genaktivitet, kromatinstatus och sjukdomsrelaterade förändringar i genomet.
Citering: Rojat, V., Ciardo, D., Tourancheau, A. et al. Automated mapping of DNA replication fork progression in human cells with ForkML. Nat Commun 17, 1975 (2026). https://doi.org/10.1038/s41467-026-68750-4
Nyckelord: DNA-replikation, replikationsgaffelns hastighet, nanopore-sekvensering, BrdU-märkning, maskininlärning i genomik