Clear Sky Science · sv
En proteogenomisk atlas över 1032 hjärnmetastaser identifierar molekylära subtyper, immunlandskap och terapeutiska sårbarheter
Varför cancer sprider sig till hjärnan
När cancervården förbättras lever fler personer tillräckligt länge för att deras tumörer ska sprida sig till nya platser, inklusive hjärnan. Dessa hjärnmetastaser är nu en vanlig och ofta förödande komplikation, ändå behandlar läkare dem fortfarande till stor del utifrån var den ursprungliga tumören startade—lunga, bröst, hud, kolon—snarare än utifrån hur cancern anpassat sig till livet i hjärnan. Denna studie byggde en detaljerad ”atlas” över mer än tusen hjärnmetastaser för att förstå deras dolda biologi, hur de interagerar med hjärnans egna celler och immunsystem, och var nya behandlingsmöjligheter kan finnas.
Att bygga en jättelik karta över hjärntumörer
Forskarna samlade data från 1 032 hjärnmetastaser som uppstått från många olika primära cancerformer, tillsammans med flera matchande primärtumörer och några aggressiva primära hjärntumörer för jämförelse. De kombinerade flera avancerade metoder: DNA- och RNA-sekvensering, storskaliga mätningar av proteiner och metaboliter, enkelcells- och rumslig kartläggning av tumör- och immunceller samt mini-organoider hämtade från patienter odlade i laboratoriet. Genom att integrera alla dessa lager ville de inte bara lista gener, utan se hur hela biologiska system beter sig inne i hjärnmetastaser.
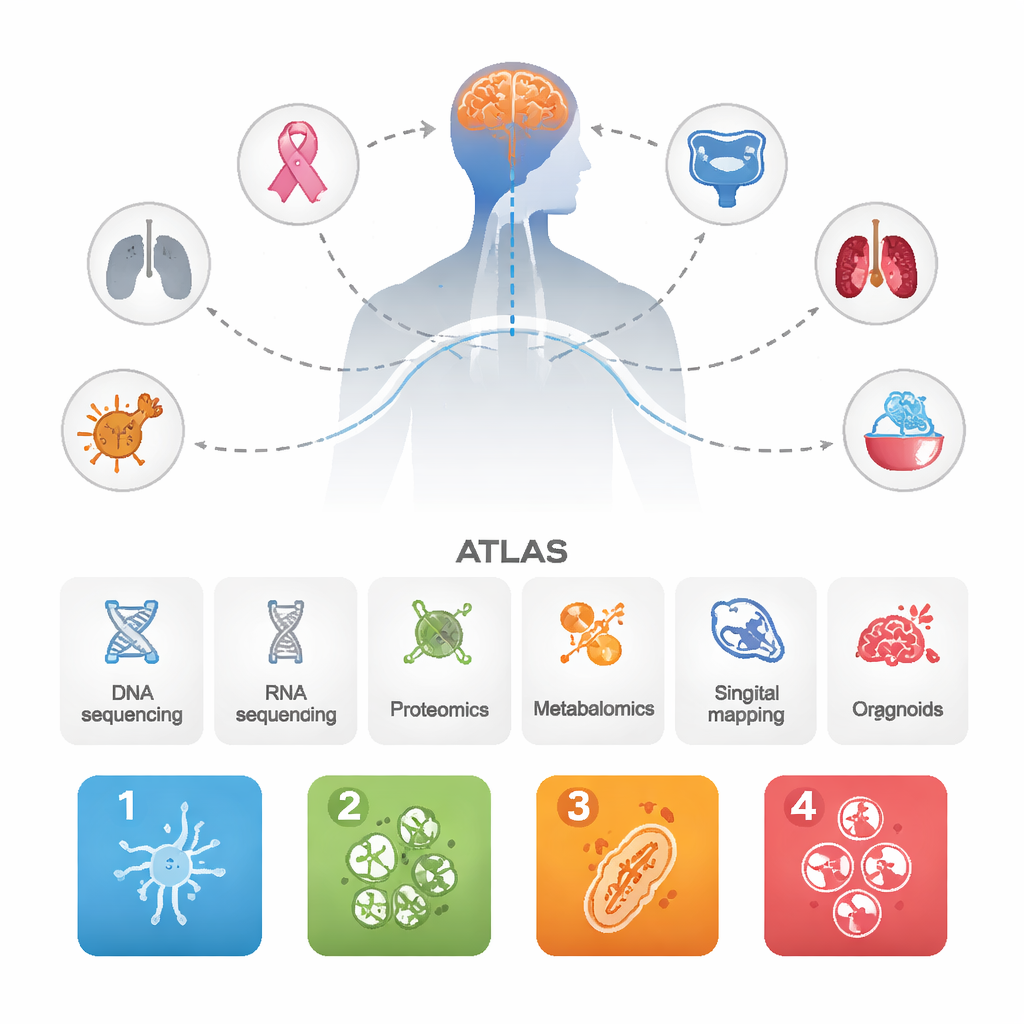
Fyra återkommande ”personligheter” hos hjärnmetastaser
Trots att de härstammade från många organ grupperade sig hjärnmetastaserna upprepade gånger i fyra huvudsakliga molekylära subtyper. En, kallad BrMS1, ser ”neural-lik” ut: tumörceller och omkringliggande vävnad uttrycker många hjärn- och nervcellsprogram och visar relativt aktiv immunövervakning. BrMS2 är ”immuninfiltrerad”, fylld med immunceller, särskilt T‑celler, och uppvisar ett program som kallas epitel–mesenkymal övergång, vilket lossar cellfästen och omformar den lokala miljön. BrMS3 är ”metabolisk”, dominerad av mycket aktiva cancerceller som omprogrammerar sin energianvändning—bränner bränsle genom vägar som fettsyremetabolism och oxidativ fosforylering. BrMS4 är ”proliferativ”, kännetecknad av snabb celldelning, stamliknande drag och hög genomisk instabilitet, men anmärkningsvärt få immunceller.
Vad tumörens omgivning avslöjar
Genom att zooma in med enkelcells- och rumslig upplösning visade teamet att varje subtype lever i ett distinkt kvarter inom hjärnan. BrMS1‑lesioner är rika på hjärnans stödjeceller såsom astrocyter och neuroner, vilket tyder på att tumören nära imiterar och kapar normal hjärnvävnad. BrMS2‑tumörer, i kontrast, är kantade av täta kluster av T‑celler, inklusive många ”utmattade” T‑celler som uttrycker kontrollpunktsmolekyler som PD‑1, och har aktiverade blodkärl och inflammatoriska signaler. BrMS3‑lesioner ligger i metabolt aktiva zoner, medan BrMS4‑lesioner bildar öar av snabbt delande celler omgivna av relativt immunsvaga områden. Överlag fann studien att i hjärnmetastaser—men inte i primära tumörer—har stark aktivering av epitel–mesenkymal övergång oftast en tendens att gå hand i hand med högre T‑cellsinfiltration, vilket antyder att detta program kan hjälpa till att öppna dörren för immunceller att komma in.
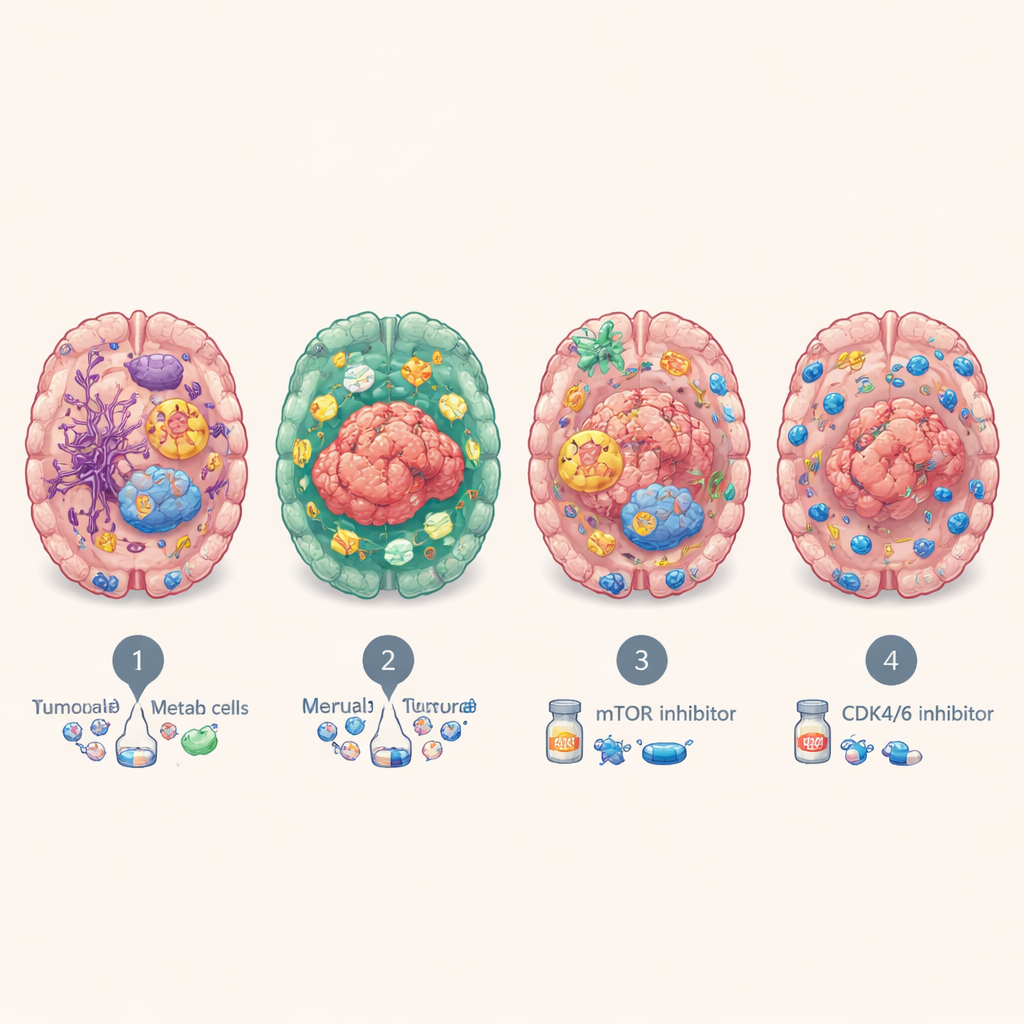
Ledtrådar till behandling och patientutfall
Dessa molekylära personligheter var inte bara akademiska. Patienter med den immuninfiltrerade BrMS2‑subtypen tenderade att leva längre än de med den proliferativa BrMS4‑subtypen, som konsekvent hade sämst utfall. Genom att testa läkemedel på patient‑härledda organoider fann teamet att de metaboliska BrMS3‑tumörerna var särskilt känsliga för att blockera mTOR‑signalvägen, som hjälper till att reglera celltillväxt och metabolism, och att de snabbt delande BrMS4‑tumörerna var mer sårbara för CDK4/6‑hämmare, läkemedel som bromsar cellcykeln. Separata analyser föreslog att BrMS1‑tumörer kan svara bättre på strålbehandling, medan BrMS2:s inflammerade, kontrollpunkt‑rika miljö kan göra dem mer benägna att gynnas av immunterapier som återaktiverar utmattade T‑celler—även om detta behöver bekräftas direkt hos patienter med hjärnmetastaser.
Vad detta betyder för personer med hjärnmetastaser
Denna atlas visar att när cancerceller når hjärnan tenderar de att konvergera mot några delade biologiska tillstånd som korsar var de ursprungligen kom ifrån. Att förstå om en persons hjärnmetastas är neural‑lik, immunrik, metabolisk eller högt proliferativ kan så småningom styra mer skräddarsydda behandlingar—såsom val mellan strålbehandling, immunterapi eller läkemedel som riktar sig mot metabolism eller celldelning. Även om arbetet ännu inte förändrar standardvården ger det en detaljerad färdplan för framtida forskning och kliniska prövningar med målet att omvandla dessa molekylära sårbarheter till bättre, mer precisa behandlingar för patienter med hjärnmetastaser.
Citering: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
Nyckelord: hjärnmetastas, tumörsubtyper, tumörmikromiljö, cancerimmunoterapi, cancermetabolism