Clear Sky Science · sv
Fosfolipidsammansättningen påverkar starkt montering av β‑tunna proteiner i renade bakterie‑yttermembran
Varför bakteriella skikt spelar roll
Läkemedelsresistenta ”superbakterier” är ett växande hot eftersom många antibiotika helt enkelt inte tar sig förbi deras kraftiga yttre försvar. Denna studie granskar en nyckelkomponent i det försvaret hos gramnegativa bakterier som E. coli: ett skyddande yttre skal fyllt med tunnformade proteiner och specialiserade fetter. Genom att reda ut hur blandningen av dessa fetter styr uppbyggnaden av det yttre skiktet, avslöjar författarna svaga punkter som skulle kunna utnyttjas vid design av framtida antibiotika.
Det dubbla skalet
Gramnegativa bakterier är ovanliga eftersom de har två membraner. Det inre membranet sköter vardagliga cellulära funktioner, medan yttermembranet fungerar som en robust regnrock som håller ute många toxiner och antibiotika. Detta yttre lager består av två typer av lipider: vanliga fosfolipider på den inre sidan och ett styvt socker‑fett kallat lipopolysackarid (LPS) på yttre sidan. Genom detta skal löper många ”beta‑barrel”‑proteiner— ihåliga cylindrar som bildar porer och portar för näringsämnen. En molekylär maskin kallad BAM (för barrel assembly machine) ansvarar för att vika dessa proteiner i rätt form och sätta in dem i yttermembranet.
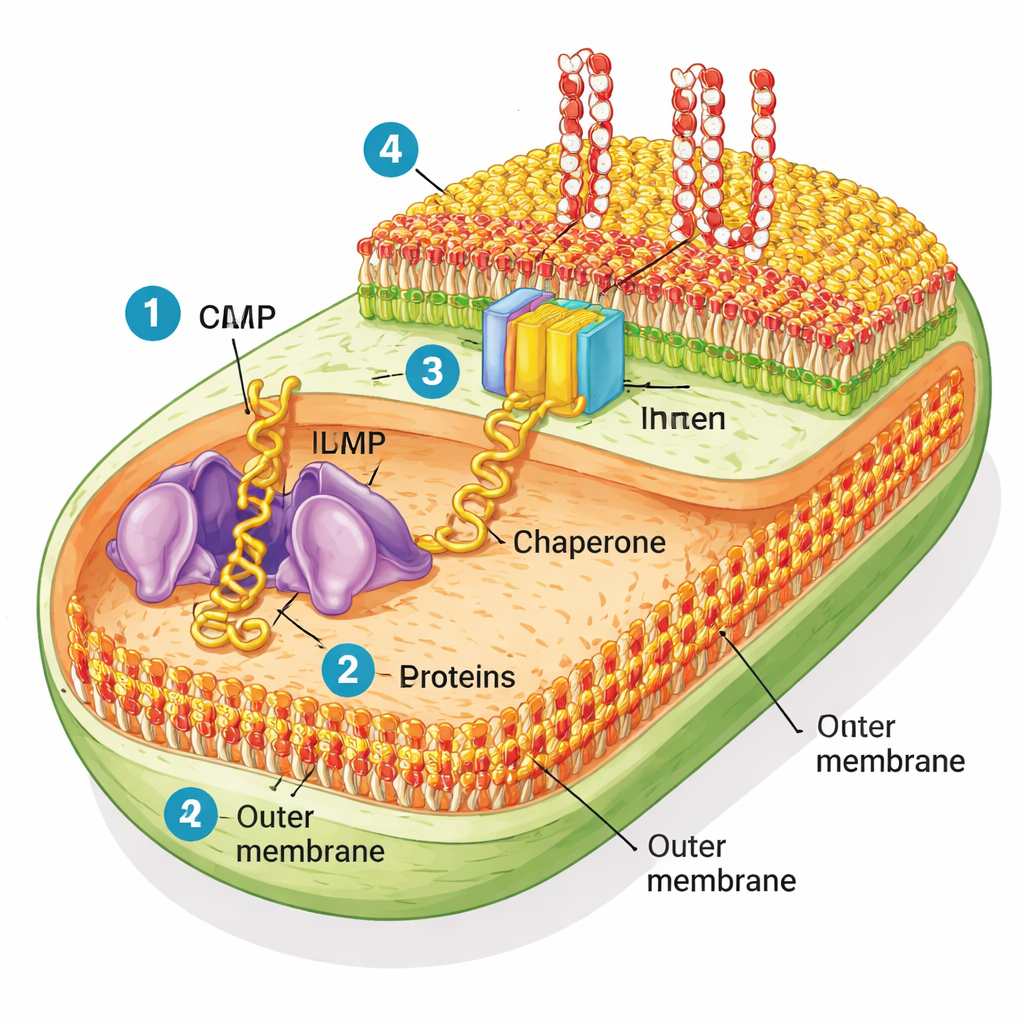
Återskapa det bakteriella skiktet i ett provrör
För att se hur väl BAM fungerar i en realistisk miljö renade forskarna delar av E. coli:s yttermembran och skapade små blåsor de kallar ”native OMs”. Till skillnad från enkla konstgjorda membraner som används i många laboratoriestudier behåller dessa native‑membran sin fulla blandning av proteiner och lipider. Teamet använde sedan ett cellfritt protein‑fabrik för att bygga nya yttermembranproteiner från grunden och observerade om BAM i dessa native‑blåsor kunde vika och infoga dem. De fokuserade på ett modell‑beta‑barrelprotein kallat EspP, tillsammans med några andra. När hjälpproteinet SurA fanns närvarande vek BAM i de native membranen effektivt EspP, och denna process blockerades av ett känt BAM‑riktat antibiotikum kallat darobactin—tydligt bevis att den naturliga maskinen förblev aktiv.
När fettsammansättningen går fel
Författarna frågade sedan vad som händer när lipidbalansen i yttermembranet rubbas. De studerade mutanta stammar av E. coli som saknar nyckelsystem som normalt rättar till felplacerade fosfolipider i det yttre lagret. Ett system, MlaA, hämtar tillbaka kringströdda fosfolipider till innermembranet; ett annat, enzymet PldA, klyver dem. Genom att använda native‑membran från dessa mutanter fann teamet att BAM‑driven montering av EspP sjönk märkbart i stammar som saknade MlaA och var allvarligt försvagad när PldA saknades. Dessa effekter berodde inte på förlust av BAM själv eller andra större proteiner, som fortfarande fanns i normala nivåer, vilket istället pekar på den förändrade lipidmiljön som orsaken.
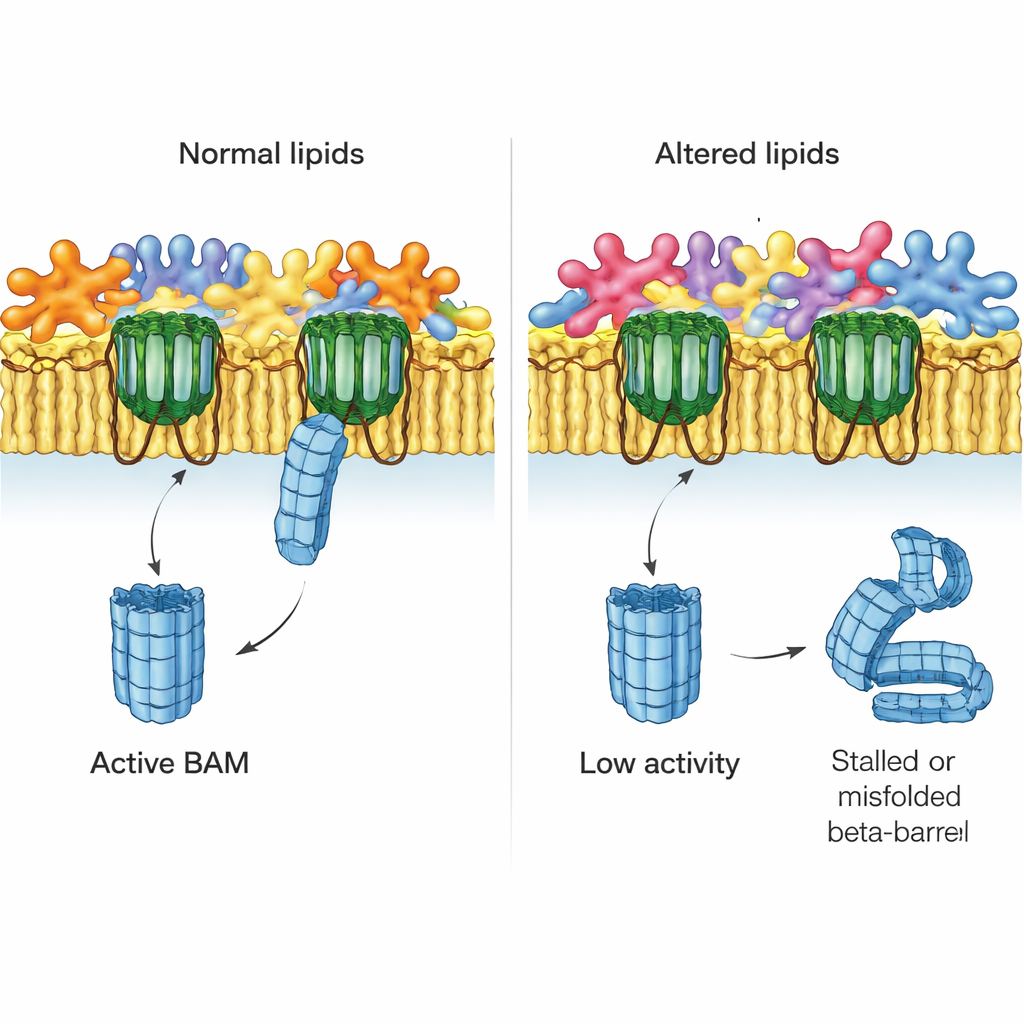
Kartläggning av lipidlandskapet i detalj
För att koppla funktion till kemi utvecklade forskarna en känslig masspektrometrimetod för att katalogisera hundratals enskilda fosfolipider i hela celler och i renade yttermembran. I normal E. coli bekräftade de att en lipidsort (fosfatidylethanolamin, eller PE) är anrikad i yttermembranet, medan andra (fosfatidylglycerol och kardiolipin) är relativt utarmade där. De fann också att ”lyso‑lipider”, som bara har en fettsvans och tenderar att böja membran, oväntat är koncentrerade i yttermembranet. I mutantstammar, särskilt de som saknar PldA, var dessa mönster omkastade: de vanliga skillnaderna mellan inre och yttre membran krympte eller till och med vändes, och längderna och typerna av fettsvansar förändrades. De stammar med mest störda lipidprofiler var samma där BAM fungerade sämst.
Konsekvenser för antibiotikastrategier
Sammantaget visar arbetet att yttermembranet inte bara är ett passivt stöd för proteiner. Dess exakta fosfolipidsammansättning påverkar starkt hur väl BAM kan bygga de beta‑barrel‑porer som håller bakterien vid liv. När lipidbalansen rubbas fungerar färre BAM‑komplex korrekt, och vissa arbetar långsammare. Även om levande bakterier kan kompensera för sådana förändringar på sätt som ett provrörssystem inte kan, lyfter denna studie fram hur man kan tunna ut eller störa specifika lipider för att försvaga det bakteriella skalet. Den insikten öppnar nya möjligheter för läkemedel som antingen riktar sig direkt mot BAM eller subtilt rubbar yttermembranets lipidbalans, vilket gör även de tuffaste gramnegativa bakterierna mer sårbara.
Citering: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
Nyckelord: Gramnegativa bakterier, yttermembranproteiner, beta‑barrel‑montering, bakteriella lipider, antibiotikaresistens