Clear Sky Science · sv
Kynurenin medierar den kemoterapiinducerade tarmtoxiciteten genom modulering av tarmmikrobiotan
Varför detta spelar roll för personer som får kemoterapi
Kemoterapi räddar liv, men den följs ofta av svåra biverkningar i tarmen — smärta, diarré, viktminskning — som kan tvinga läkare att sänka doser eller avbryta behandlingen i förtid. Denna studie avslöjar en dold kedjereaktion mellan ett blodbundet kemiskt ämne, immunceller och tarmens mikrober som hjälper till att förklara varför ett vanligt cancerläkemedel, oxaliplatin, kan vara så hårt mot tarmen, och pekar på nya sätt att skydda patienter utan att försvaga den antitumöreffekten.
En kemisk länk mellan behandling och tarmskada
Forskarna inledde med patienter med kolorektal cancer som fick oxaliplatinbaserad kemoterapi. De jämförde blodprover från personer som utvecklade svåra tarmsbiverkningar med dem som tålde behandlingen bättre. Med riktad kemisk profilering fann de att flera nedbrytningsprodukter av aminosyran tryptofan var högre i gruppen med hög toxicitet, där en molekyl — L‑kynurenin — utmärkte sig som den mest kraftigt förhöjda. Patienter med mer L‑kynurenin i blodet visade också fler tecken på inflammation och lägre vita blodkroppstal, vilket antyder att denna molekyl kan vara direkt kopplad till behandlingsrelaterad skada.
Bevisa orsak och verkan i möss
För att gå bortom korrelation vände sig teamet till musmodeller. När friska möss gavs höga doser oxaliplatin utvecklade de klassiska tecken på tarmsskada: viktnedgång, förkortade tjocktarmar, svullnad i tarmväggen, färre delande celler och fler döende celler i tarmens slemhinna. Dessa möss uppvisade också en kraftig ökning av L‑kynurenin i blodet, vilket speglade de mänskliga fynden. När forskarna gav extra L‑kynurenin till oxaliplatinbehandlade möss förvärrades tarmbesvären — men läkemedlets tumörbekämpande effekt förblev intakt. Omvänt, när de tog bort eller blockerade enzymet IDO1, som kroppen använder för att omvandla tryptofan till L‑kynurenin, var mössen mycket mer motståndskraftiga mot tarmtoxicitet samtidigt som de fortfarande drog nytta av kemoterapin.
Immunceller och tarmmikrober i krysselden
När forskarna grävde djupare undersökte de vilka celler som ansvarade för att producera överskottet av L‑kynurenin under behandling. De fann att oxaliplatin stimulerar vissa immunceller (CD8 T‑celler) att frisätta signalproteinet interferon‑gamma, vilket i sin tur slår på IDO1 i närliggande myeloida celler — en klass vita blodkroppar. Möss konstruerade så att endast deras myeloida celler saknade IDO1 producerade mycket mindre L‑kynurenin och var skyddade från tarmskada, medan borttagning av IDO1 endast i tarmepitelceller hade liten effekt. Samtidigt förändrades sammansättningen av tarmmikrobiotan. Hos normala möss kopplades oxaliplatin och höga nivåer L‑kynurenin till förlusten av en hjälpsam bakterie, Lactobacillus johnsonii. I kontrast behöll möss med minskat L‑kynurenin högre nivåer av L. johnsonii. När tarmbakterier utplånades med antibiotika försvann den skyddande effekten av lågt L‑kynurenin, och när bakterier från låg‑kynurenin‑möss transplanterades till normala möss blev mottagarna mer motståndskraftiga mot oxaliplatins tarmpåverkan.
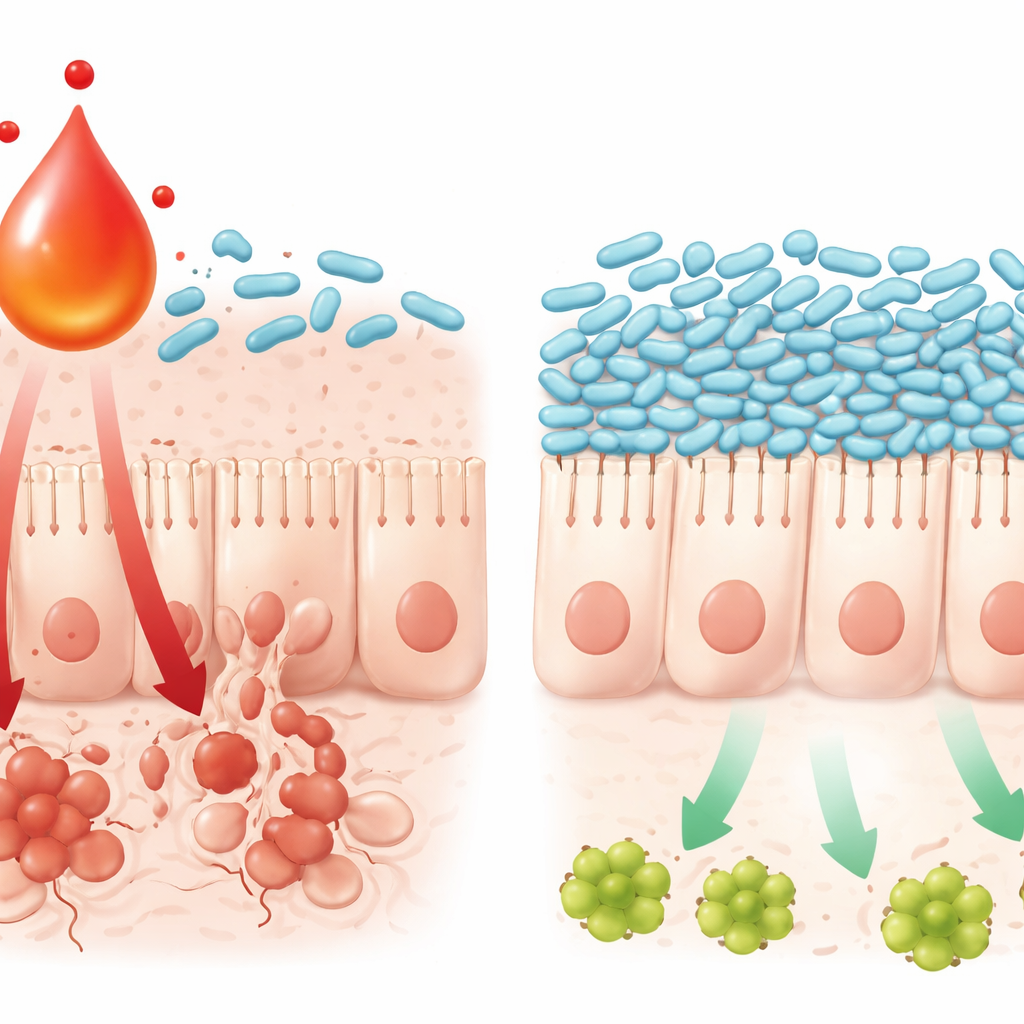
Hur en metabolit driver celldöd i tarmen
Studien följde också hur denna kemi–mikrob‑interaktion skadar tarmens slemhinna. Höga nivåer av L‑kynurenin förknippades med ökad aktivitet i en välkänd inflammatorisk väg i tarmvävnaden, TNFα/JNK‑vägen, som skjuter celler mot programmerad död. I cellkultur gjorde kombinationen av oxaliplatin och L‑kynurenin tarmceller mer benägna att aktivera denna väg och dö, medan tillsats av L. johnsonii försvagade signalen och bevarade cellöverlevnad. L‑kynurenin kunde i sig sakta ned tillväxten och undergräva överlevnadsmekanismer hos L. johnsonii i laboratoriediskar, vilket hjälper till att förklara varför bakterien försvinner när metaboliten ackumuleras. Tillsammans ritar dessa fynd upp en självförstärkande slinga: kemoterapi utlöser immunsignalering, immunceller ökar L‑kynurenin, detta stör vänliga bakterier som L. johnsonii, och det förändrade mikrobiella samhället i sin tur förstärker inflammatoriska signaler som dödar tarmceller.
Nya sätt att skydda patienter under behandlingen
Hoppfullt pekar arbetet också på praktiska strategier. Behandling av möss med ett läkemedel kallat Epacadostat, som hämmar IDO1, sänkte L‑kynureninnivåerna och minskade markant oxaliplatininducerad tarmskada utan att försämra tumörkontrollen. I en kompletterande metod konstruerade teamet en ofarlig stam av E. coli att överproducera ett enzym som bryter ner L‑kynurenin i tarmen. Möss som gavs dessa ingengörda bakterier var likaledes skyddade från tarmtoxicitet, återigen utan att kompromettera kemoterapins antitumöreffekt. Tillskott av L. johnsonii i sig lindrade också symtomen och bevarade tarms strukturen.
Vad detta betyder för personer med cancer
Sammantaget visar denna studie att en enda behandlingsdriven metabolit — L‑kynurenin — fungerar som en viktig mellanhand mellan kemoterapi, immunsystemet, tarmmikrober och tarmsskada. Genom att visa att blockera dess produktion, öka dess nedbrytning eller återställa skyddande bakterier alla kan mildra kemoterapins inverkan på tarmen, öppnar forskningen en väg mot tilläggsbehandlingar som kan hålla patienter starkare och mer bekväma medan de kämpar mot cancer.
Citering: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
Nyckelord: biverkningar av kemoterapi, tarmmikrobiom, tryptofanmetabolism, L-kynurenin, kolorektal cancer