Clear Sky Science · sv
Nikelkatalyserade divergerande sulfoneringar av propargylkarbonat
Varför denna kemi betyder mer än laboratoriet
Svavelhaltiga molekyler står i centrum för många moderna läkemedel, växtskyddsmedel och avancerade material. Att framställa dessa föreningar på ett precist, effektivt och flexibelt sätt är emellertid ofta svårt. Denna artikel beskriver en nikeldriven katalytisk metod som kan omvandla enkla utgångsmaterial till flera olika familjer av svavelrika molekyler, alla med strikt kontrollerade tredimensionella former. Den typen av kontroll kan påskynda läkemedelsupptäckt och hjälpa kemister att bygga komplexa molekyler på ett renare och mer hållbart sätt.
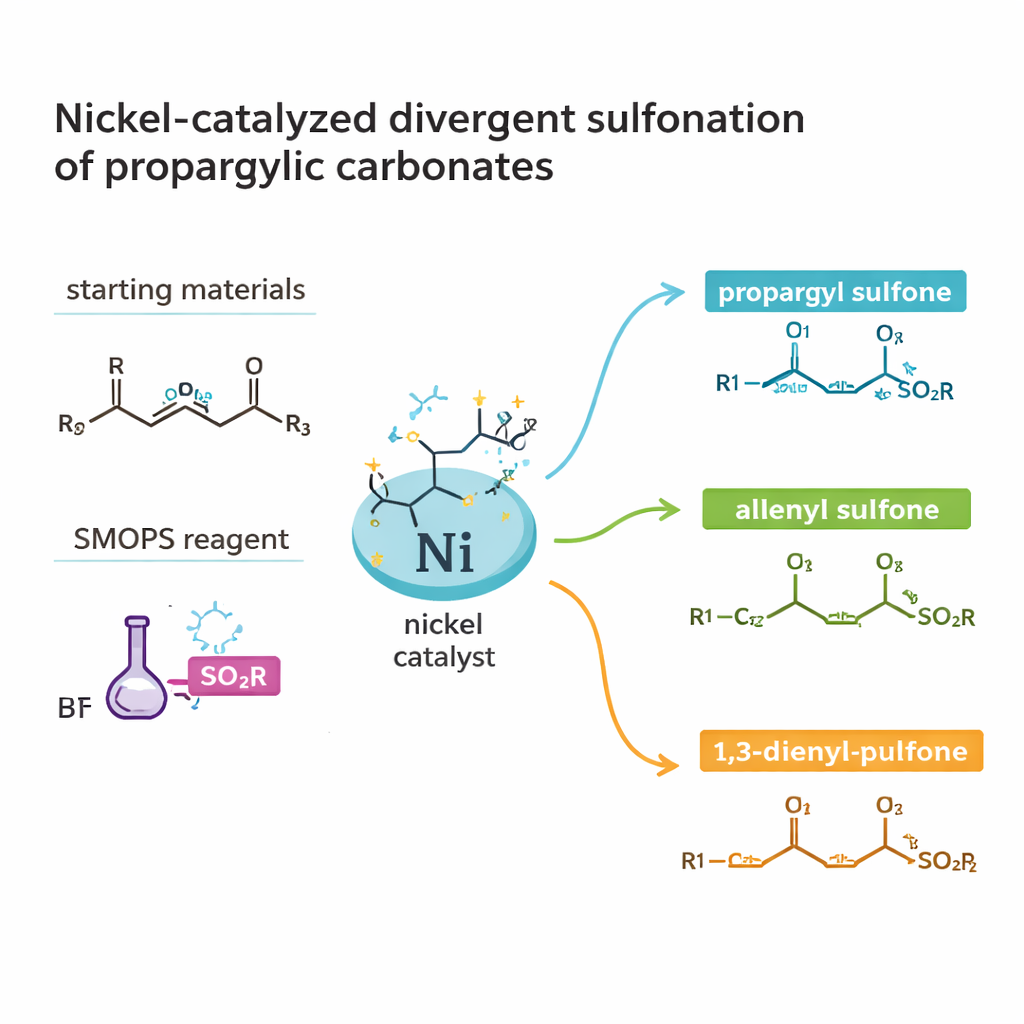
Bygga användbara molekyler från enkla delar
Arbetet fokuserar på en klass av molekyler kallade sulfoner och sulfinater, som innehåller svavel bundet till syre och kol. Dessa strukturer förekommer i många bioaktiva naturprodukter och läkemedel, men traditionella vägar till dem kan vara långa och slösande. Författarna riktar in sig på en särskilt värdefull undergrupp: kirala sulfinater, vars spegelbildsformer kan bete sig väldigt olika i kroppen. Istället för att börja från redan komplexa byggstenar använder de två lättillgängliga partner: propargylkarbonater (en sorts liten kolryggrad med en inbyggd lämnargrupp) och en kommersiell svavelkälla känd som SMOPS. Genom att kombinera dessa under nikelkatalys strävar de efter att generera högvärdiga svavelhaltiga produkter i bara ett eller två steg.
En katalytisk system, tre produktfamiljer
Ett slående drag i studien är att samma grundläggande ingredienser kan styras att bilda tre olika typer av produkter: propargylsulfoner, allenylsulfoner och 1,3‑dienylsulfoner. Var och en av dessa kolramverk leder till olika vidare kemi och biologisk aktivitet. Genom att noggrant välja liganden bundet till nickel, lösningsmedel, temperatur och tillsatser kan teamet "styra" reaktionen mot ett visst utfall. Under milda förhållanden i acetonitril och med en kiral fosfinligand erhåller de propargylsulfoner i hög avkastning och med utmärkt kontroll över handighet. Genom att behandla dessa produkter med aluminiumoxid omformas kol–kol trippelbindningen försiktigt till en allen utan att den kirala informationen går förlorad. Genom att byta till en annan ligand och lösningsmedel kanaliseras processen istället mot 1,3‑dienylsulfoner, vilket förlänger kolramen.
Testa utbredning och flexibilitet
För att se hur generell metoden är varierade forskarna båda reaktantsidorna. De visade att många olika natriumsulfinater, inklusive enkla alkyl-, aryl- och mer komplexa ringsystem, deltar rent och ger kirala produkter med hög enantiomerisk övervikt. Likaså fungerar ett brett urval av propargylkarbonater med olika substitutioner på den aromatiska ringen eller kolkedjan väl, även om vissa substrat med mycket stora grupper eller terminala alkyner faller utanför den nuvarande metoden. Gruppen visar också att kvantiteterna kan skalas upp utan att effektivitet eller selektivitet går förlorad, ett viktigt steg mot praktisk användning. Denna breda räckvidd innebär att kemister kan koppla in många olika fragment och snabbt få tillgång till ett bibliotek av närbesläktade svavelhaltiga molekyler.
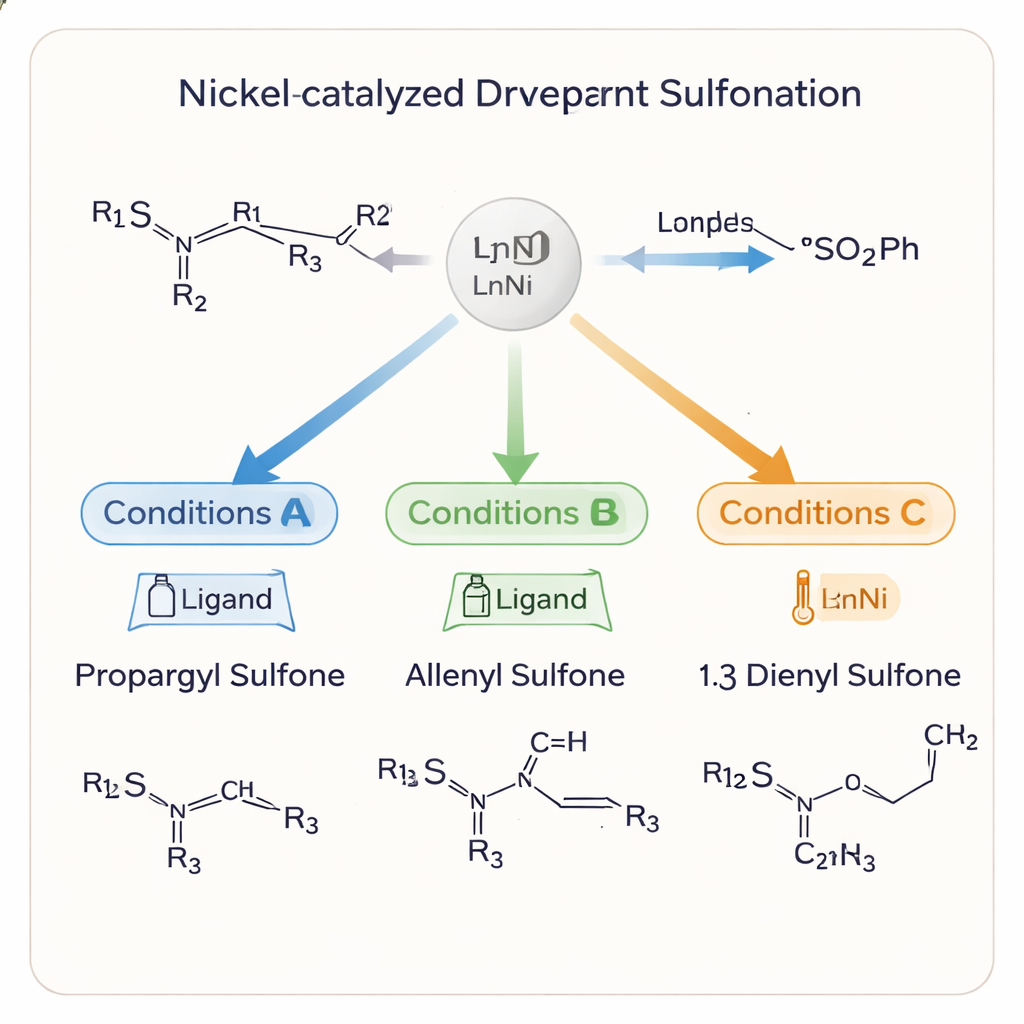
Förvandla byggstenar till komplexa mål
Utöver att enbart framställa dessa sulfoner visar författarna hur enkelt de kan omvandlas till andra användbara strukturer. Hydrogenering omvandlar trippelbindningen till alkaner eller alkener samtidigt som den kirala centern intill svavlet bevaras. Enkla uppföljningsreaktioner omvandlar sulfonenheterna till sulfinater, sulfonamider och sulfonylfluorider—motif som ofta förekommer inom medicinsk kemi och i "click-liknande" bindningsbildande reaktioner. Som en höjdpunkt använder de sin metod som det centrala steget i en koncis syntes av en kiral β‑sulfinylhydroxamsyra, en typ av molekyl känd för att hämma bakteriella enzymer. Denna väg undviker flera äldre, mer omständliga steg och understryker den syntetiska kraften i att ha kirala sulfinater tillgängliga på begäran.
Hur reaktionen väljer sin bana
Forskargruppen undersöker också hur och varför reaktionen växlar mellan produkter. Tidsförloppsexperiment visar att propargylsulfonen vanligtvis bildas först, sedan kan den omarrangera till allenen och slutligen till 1,3‑dienen under vissa förhållanden. Nikelkatalysatorn, tillsammans med den valda liganden och tillsatsen, styr vilka intermediärer som favoriseras och hur svavelgruppen förflyttar sig längs kolkedjan. Aluminiumoxid möjliggör till exempel alkin‑till‑allenomformningen vid mycket låg temperatur samtidigt som den tredimensionella atomordningen bevaras. En förenklad mekanism antyder att subtila förändringar i reaktionsvillkoren omdirigerar ett vanligt nickelintermediat längs olika vägar, vilket förklarar hur ett system kan ge flera noggrant definierade produkter.
Vad detta betyder för framtida läkemedel och material
För icke‑specialister är huvudpoängen att denna nikelkatalyserade metod erbjuder en mångsidig kemisk "kopplingspanel": från samma enkla utgångsdelar kan kemister välja vilket svavelrikt skelett de vill ha och få det i ett enda, mycket selektivt steg. Eftersom dessa produkter är utmärkta byggstenar för läkemedel och andra funktionella molekyler kan tillvägagångssättet förkorta vägen från koncept till kandidatförening. Det visar också hur noggrant utvald katalysator och villkor kan förvandla en tidigare utmanande omvandling till ett rutinverktyg, vilket öppnar dörren för snabbare, renare konstruktion av komplexa, kirala svavelhaltiga molekyler.
Citering: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
Nyckelord: nickelkatalys, kirala sulfoner, asymmetrisk syntes, organisk reaktionsdesign, läkemedelslika byggstenar