Clear Sky Science · sv
Tumör-intrinsiska egenskaper formar T-cellsdifferentiering genom förstadium till symptomatiskt multipelt myelom
Varför denna forskning är viktig
Multipelt myelom är en blodcancer som bildas i benmärgen och nästan alltid föregås av tystare, tidiga tillstånd som eventuellt kan utvecklas till full sjukdom. Många lever i åratal med dessa förstadier utan att veta om eller när de kommer att progrediera. Denna studie ställer en aktuell fråga: kan vi avläsa immunsystemets ”sinne” och historia — särskilt T‑cellerna — för att förstå hur myelom utvecklas, hur det svarar på behandling och vem som löper störst risk att få progress?
Kroppens cancermedarbetare
T‑celler är mångsidiga immunceller som kan känna igen och förstöra onormala celler, inklusive cancer. I solida tumörer som lung‑ eller hudcancer kan långvarig stimulans driva T‑celler in i ett utmattat tillstånd där de blir ineffektiva, ett tillstånd som moderna immunoterapier försöker vända. Författarna sammanställde en enorm singelcellskarta med mer än en miljon celler från benmärg och blod hos personer med multipelt myelom, dess förstadier (MGUS och smoldering myelom) och icke‑cancerkontroller. Genom att avläsa både genaktivitet och de unika receptorsekvenserna som definierar varje T‑cellsklon rekonstruerade de hur T‑celler är organiserade, hur ”åldrade” eller ”erfarna” de ser ut och hur väl de följer den underliggande tumören.
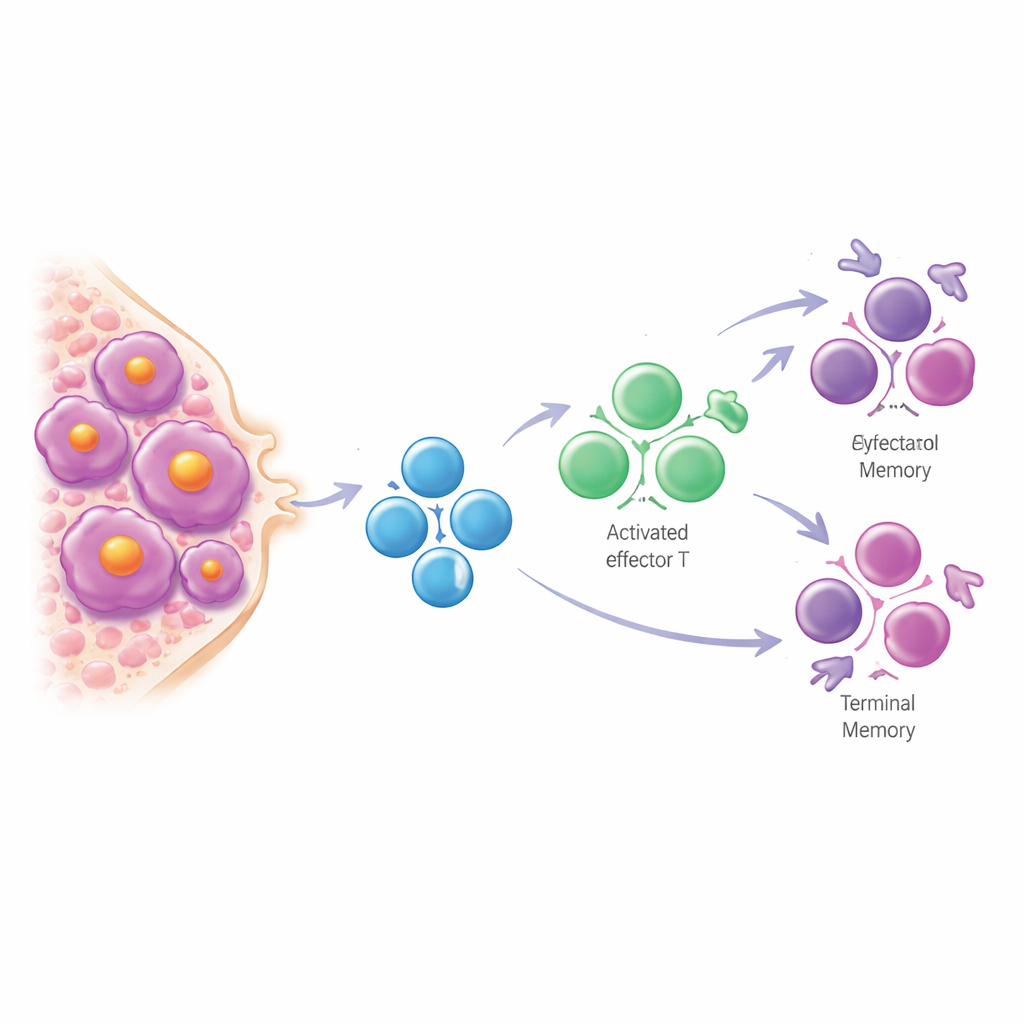
Inte utmattade, utan för tidigt åldrade
Till skillnad från vad som ses i många solida tumörer fann teamet att T‑celler i myelom sällan är verkligt utmattade. Celler med klassiska utmattningsmarkörer var i stor utsträckning begränsade till en enda ovanlig patient. Istället försköts benmärgs‑T‑celler i smoldering och symptomatiskt myelom bort från naiva, tidiga stadier och mot höggradigt erfarna ”terminala minnes”-typer som påminner om T‑celler hos äldre individer. Detta mönster — kallat T‑cellsförskjutning — parallellerade immunsystemets naturliga åldrande men verkade överdrivet hos patienterna, som om deras T‑celler åldrats snabbare än resten av dem. Ju mer avancerad sjukdomen och ju större tumörbördan var, desto starkare var förskjutningen mot sena minnesceller, och liknande förändringar syntes även i blodet.
Ledtrådar från T‑cellsfingeravtryck
Varje T‑cell bär en unik receptor, och celler som delar samma receptorsekvens tillhör en klon som expanderat som svar på någon trigger. Genom att spåra dessa receptorer visade forskarna att myelombenmärgar innehåller många expanderade T‑cellskloner med drag av potenta mördarceller. Dessa kloner kände inte främst igen vanliga virus. Istället bar de en distinkt ”icke‑viral” gensignatur kopplad till ett kraftfullt cytotoxiskt maskineri och var berikade hos personer med myelom jämfört med förstadier. Tumörer som var bättre på att visa upp proteinfragment på sin yta — genom högre aktivitet i antigenpresentationsgener — tenderade att vara associerade med dessa icke‑virala, högdifferentierade T‑celler. Patienter vars tumörer visade denna starkare immunengagemang hade i allmänhet bättre överlevnad, vilket antyder att dessa T‑celler åtminstone delvis verkligen är antitumorala.
Behandling, återfall och tidiga varningssignaler
Studien följde också patienter som genomgick autolog stamcellstransplantation, en vanlig intensiv behandling. Efter transplantation blev T‑cellreceptorrepertoaren mer dominerad av några få stora kloner. Många av dessa expanderande kloner kunde härledas till terminalt differentierade CD8‑T‑celler som redan fanns före behandlingen och bar samma icke‑virala, myelomassocierade signatur. Patienter som fortfarande hade kvarvarande cancer efter transplantationen tenderade att ha särskilt klonala, förskjutna T‑cellrepertoarer, vilket tyder på att ett kraftfullt men åldersliknande T‑cellsvar kanske inte klarar att helt rensa sjukdomen. Tidigare i sjukdomsförloppet fann författarna att smoldering‑patienter som senare progredierade till aktivt myelom ofta hade en minskning av regulatoriska CD4‑T‑celler — celler som normalt hjälper till att hålla immunsvar och benmärgsmiljön i balans. Låga nivåer av dessa celler förutsade snabbare progress, oberoende av befintliga kliniska riskpoäng.
Vad detta betyder för patienter
För personer som lever med myelom och dess förstadier omformulerar detta arbete hur immunsystemet svarar på cancern. Istället för att helt enkelt bli utmattade verkar T‑celler i myelom drivas kroniskt in i ett sent, åldrat tillstånd av pågående strider med tumörceller. Detta förskjutna, klonala T‑cellslandskap speglar tumörbörda, påverkar svaret på behandlingar som transplantation och T‑cellsengagerande läkemedel, och kan — i fallet med förlust av regulatoriska T‑celler — även peka ut individer med högre risk för progression från smoldering till symptomatisk sjukdom. På sikt kan dessa insikter vägleda nya immunoterapier som föryngrar eller omdirigerar T‑celler och hjälpa kliniker att använda immunegenskaper tillsammans med traditionella markörer för att tajma övervakning och tidiga insatser mer precist.
Citering: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
Nyckelord: multipelt myelom, T-celler, immunåldrande, single-cell-sekvensering, cancerimmunologi