Clear Sky Science · sv
Klickbaserad bestämning av molekylackumulering i Escherichia coli
Varför små läkemedel har svårt att nå farliga bakterier
Modern medicin förlitar sig på antibiotika, men några av de farligaste bakterierna skyddas nu av robusta yttre skikt som hindrar många läkemedel från att ta sig in. Gramnegativa bakterier såsom Escherichia coli har ett särskilt effektivt yttre membran som utgör en barriär, vilket gör det svårt att utforma mediciner som verkligen når sina mål inuti cellen. Denna artikel presenterar ett nytt laboratorietest, kallat CHAMP‑analysen, som låter forskare snabbt mäta hur väl tusentals olika småmolekyler smyger förbi dessa försvar och ackumuleras i levande E. coli‑celler.
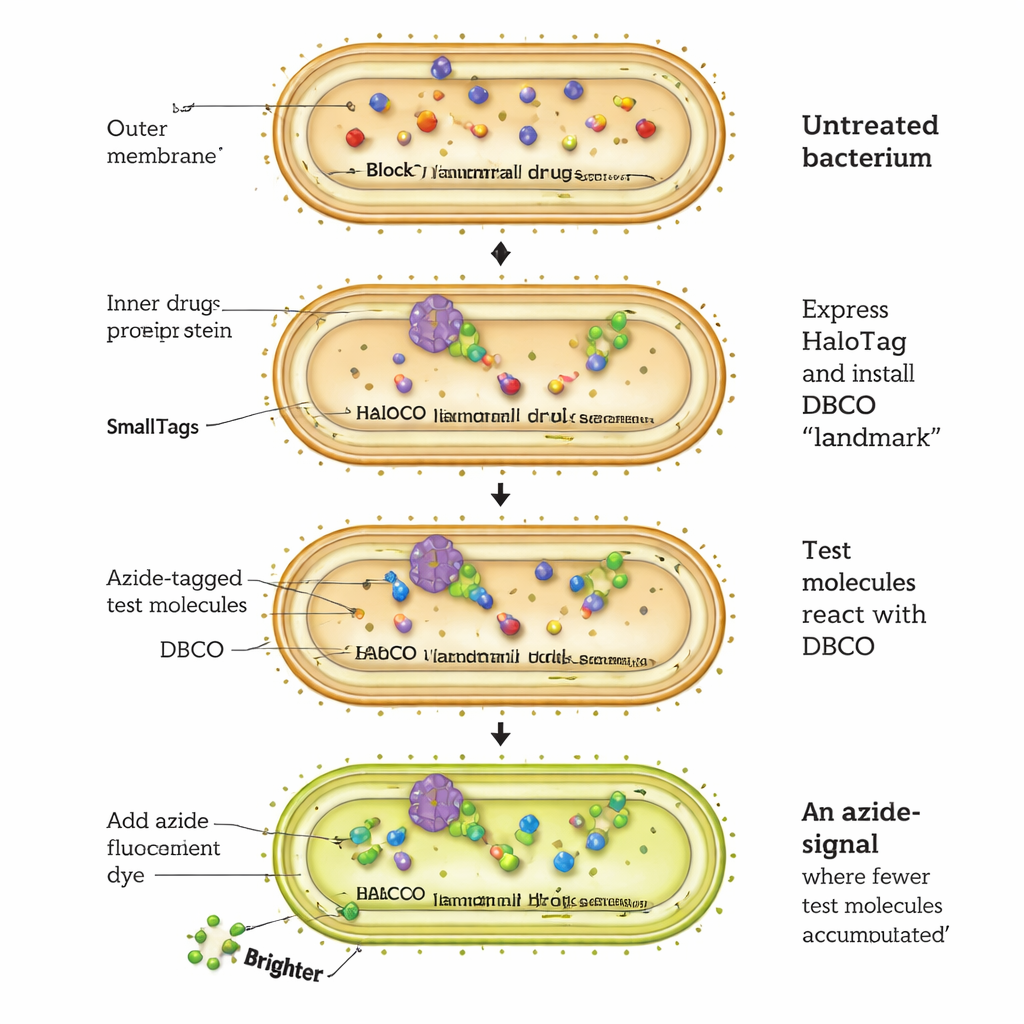
Ett nytt sätt att följa hur läkemedel går in i bakterieceller
Traditionell antibiotikaupptäckt förlitade sig på naturprodukter och enkla tillväxttester för att se om bakterier överlevde eller dog. Dessa tester avslöjar inte hur mycket läkemedel som faktiskt kom in i cellen, eller vart det tog vägen när det väl var inne. Författarna ville skapa en direkt, allmänt användbar metod för att spåra läkemedelsinträngning i bakteriellt cytosol — den vätskeinre delen där många antibiotikatmål finns. Målet var att gå bortom grova mått som minsta hämmande koncentration (MIC), som blandar effekter av upptag, målbindning och efterföljande biologiska händelser, och istället få en ren mätning av intracellulär ackumulering.
Att förvandla bakterier till små kemiska inspelare
CHAMP‑analysen fungerar genom att omkoda ett bakteriellt protein kallat HaloTag till en sorts molekylär landningsplatta. E. coli‑celler konstrueras för att producera HaloTag i sitt cytosol. Forskarna fäster först ett särskilt kemiskt handtag, en "spänd" alkin kallad DBCO, på HaloTag med en kort kloroalkanförbindelse. Därefter utsätts bakterierna för testmolekyler som var och en bär en mycket liten azid‑tagg. Endast de testmolekyler som korsar det yttre membranet, passerar det inre membranet och når cytosolen kan reagera med DBCO‑handtaget i en högselektiv "click"‑reaktion och permanent märka HaloTag. Slutligen behandlas cellerna med ett azid‑märkt fluorescerande färgämne som endast kan binda till kvarvarande fria DBCO. Ju starkare fluorescens, desto färre testmolekyler nådde cytosolen; svagare celler indikerar bättre ackumulering.
Att undersöka hur kemi och biologi formar läkemedelsintrång
Med CHAMP finjusterade teamet först uttrycket av HaloTag, mängden DBCO‑anker och valet av fluorescerande färgämnen för att få ett stort och pålitligt signalspann. De använde sedan serier av nära besläktade småmolekyler för att se hur kemiska förändringar påverkar inträdet. Att omvandla karboxylsyror till amider och att lägga till eller ta bort basiska aminogrupper kunde märkbart ändra cytosolära nivåer. I många fall förbättrade primära aminer ackumuleringen, vilket speglar oberoende "eNTRy‑regler" som utvecklats av andra grupper. Analysen hanterade också azid‑märkta varianter av verkliga antibiotika och avslöjade stora skillnader: skrymmande läkemedel som vankomycin nådde knappt cytosolen alls, medan mindre antibiotika som trimetoprimderivat och vissa oxazolidinoner trängde in mycket lättare.
Avslöja bakteriella försvar som pumpar ut läkemedel
Eftersom metoden körs i levande, genetiskt programmerbara bakterier kan den reda ut rollerna för olika cellulära försvar. Författarna jämförde normala E. coli med stammar som saknar TolC, en nyckelkomponent i en stor multidrogseffluxpump, eller med celler behandlade med en småmolekylär TolC‑hämmare. För novobiocin och flera andra azid‑märkta antibiotika visade CHAMP klart högre cytosolära nivåer när TolC var inaktivt, vilket bekräftar att dessa föreningar är effluxsubstrat. De testade också sätt att luckra upp det yttre membranet, antingen kemiskt med peptiden PMBN eller genetiskt genom att överuttrycka en vidöppen porinkanalen. Många molekyler som tidigare ackumulerade dåligt visade stora ökningar när membranet permeabiliserades, vilket belyser hur inträde och efflux tillsammans bestämmer interna läkemedelsnivåer.
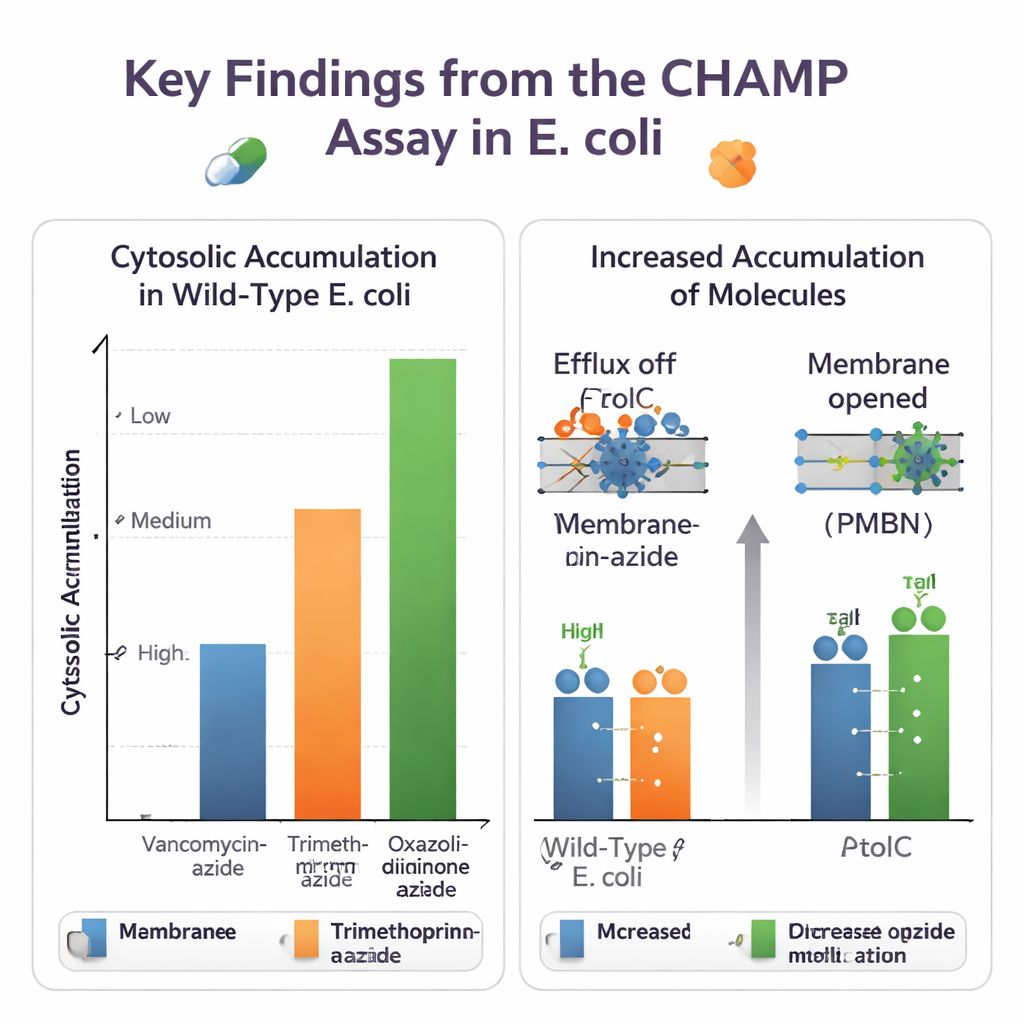
Skalning upp till tusentals molekyler för mönster och regler
För att visa verklig storskalighet screenade forskarna ett kommersiellt set med 404 azid‑märkta föreningar och ett anpassat bibliotek på 1 152 azid‑bärande molekyler. De mätte ackumulering i flera bakteriella kontexter, inklusive obehandlade celler, PMBN‑behandlade celler, hyperporinerade celler och hyperporinerade celler utan TolC. Genom att jämföra samma molekyl över dessa förhållanden kunde de se vilka förändringar som berodde på cellbiologin snarare än på variationer i click‑reaktionshastighet. Genom att kombinera CHAMP‑data med beräkningsanalys kopplade de vissa fysikalisk‑kemiska egenskaper — såsom polar yta, vätebindningskapacitet och specifika ringskelett — till starkare igenkänning av TolC‑baserad efflux. Denna typ av storskalig profilering börjar formulera designregler för molekyler som antingen undviker pumpar eller utnyttjar poriner mer effektivt.
Vad detta betyder för framtida antibiotika
Kort sagt förvandlar detta arbete E. coli till en höggenomströmningsensor som rapporterar exakt hur mycket av en testförening som når den del av cellen där många läkemedelsmål finns. CHAMP ersätter inte tester som visar om bakterier dödas, men fyller en avgörande lucka genom att separera "att ta sig in" från "att orsaka skada." Med förmågan att mäta mer än tusen molekyler i olika mutant- eller kemiskt modifierade stammar på några dagar kan forskare nu systematiskt lära vilka kemiska egenskaper som främjar inträde, minskar efflux eller gynnas av membran‑störande medhjälpare. Den kunskapen bör snabba på utformningen av nya antibiotika och hjälpläkemedel som kan bryta igenom de formidabla försvaren hos gramnegativa patogener innan resistens urholkar mer av antibiotikaarsenalen.
Citering: Ongwae, G.M., Liu, Z., Feng, S. et al. Click-based determination of accumulation of molecules in Escherichia coli. Nat Commun 17, 2008 (2026). https://doi.org/10.1038/s41467-026-68717-5
Nyckelord: antibiotikaresistens, Escherichia coli, läkemedelspenetration, effluxpumpar, clickkemi