Clear Sky Science · sv
TREM2-uttrycksnivå är avgörande för mikroglials tillstånd, metabola kapacitet och effekten av TREM2-agonism
Varför hjärnans städceller spelar roll vid Alzheimer
Alzheimers sjukdom är mest känd för klibbiga proteinavlagringar i hjärnan, men en lika viktig berättelse är hur hjärnans egna immunceller reagerar på denna skada. Dessa celler, kallade mikroglia, fungerar som städare och sjukvårdspersonal: de rensar upp skräp, reglerar inflammation och hjälper neuroner att överleva. Denna studie ställer en förenklat formulerad men långtgående fråga: hur mycket av en nyckelreceptor på mikroglia, TREM2, är ”lagom” för att skydda hjärnan — och när kan läkemedel som förstärker TREM2 vara till hjälp eller skadliga?
En dimmerknapp, inte en av/på-brytare
Tidigare genetiska studier visade att personer med vissa funktionsnedsättande förändringar i TREM2-genen har ökad risk för sen debuterande Alzheimers sjukdom. Ändå har TREM2 ofta setts som en av/på-brytare: antingen närvarande eller frånvarande. Författarna byggde i stället en speciell ”reportermus” där mikroglia lyser i proportion till hur mycket TREM2 de producerar. Detta gjorde det möjligt att sortera mikroglia i låga, medel och höga TREM2-grupper och undersöka vad varje grupp gjorde. De studerade dessa celler både i friska möss och i möss som utvecklar amyloida plack, ett kännetecken för Alzheimerliknande patologi. 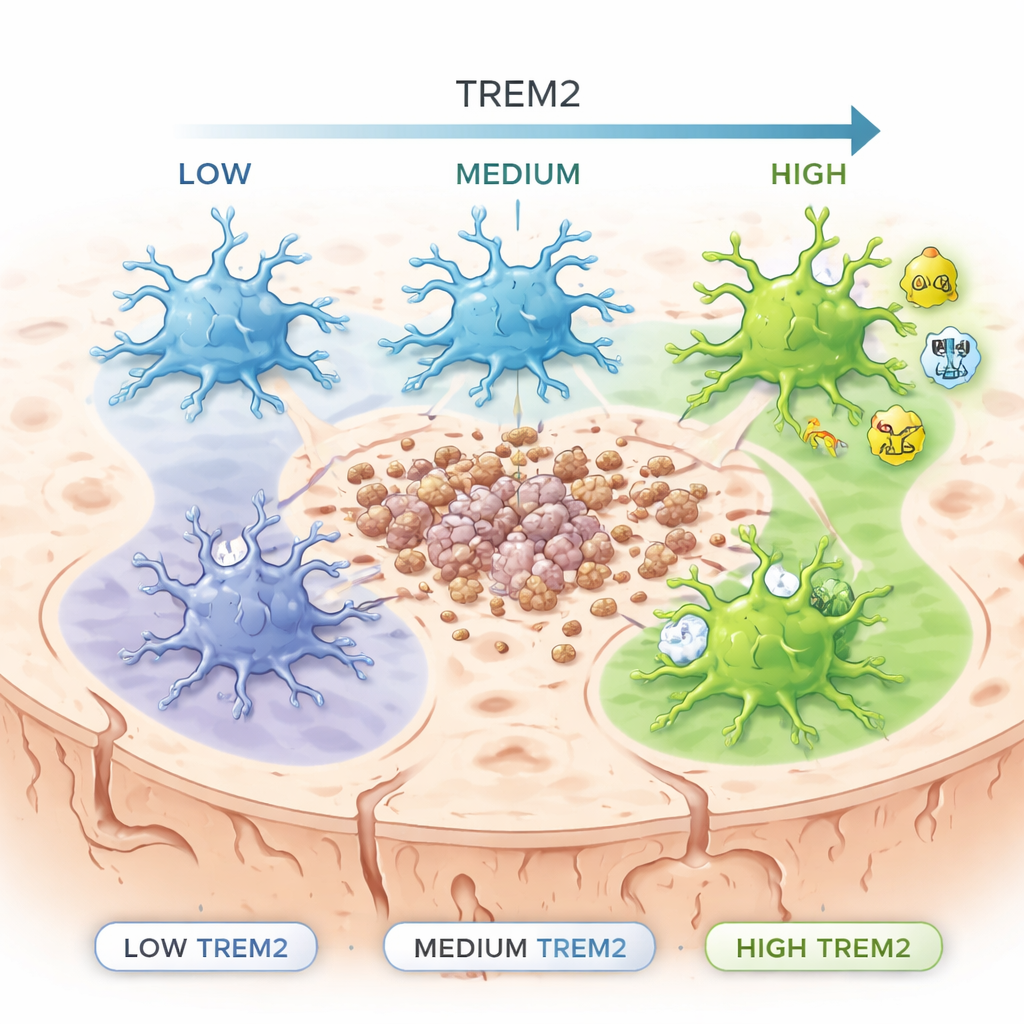
Energianvändning och kolesterolhantering förändras med TREM2-nivån
När de kunde separera dessa mikrogliaundergrupper analyserade forskarna vilka gener som slog på, vilka metaboliter som fanns närvarande och hur aktivt cellerna använde energi. Mikroglia med mer TREM2 uppvisade starkare aktivitet i banor kopplade till oxidativ fosforylering (cellens huvudsakliga energiproducerande system) och till kolesterol- och lipidmetabolism. Mätningar av märkt glukosupptag bekräftade att celler med högre TREM2 tog upp mer socker, särskilt i sjuka hjärnor. Detaljerade metabolit- och lipidprofiler visade att hög-TREM2-mikroglia hade fler byggstenar för cellulär energi och antioxidativt försvar, och mindre fritt kolesterol och vissa fettdelar, vilket pekar på effektivare bränsleanvändning och bättre utsöndring av kolesterol.
Från metabolism till städkraft
Dessa molekylära signaturer översattes till verkliga funktionella skillnader. I kontrollerade laboratorietester exponerade teamet mikroglia för fluorescensmarkerade myelinfragment — en modell för den typ av skräp mikroglia måste rensa i sjukt hjärnvävnad. Mikroglia med låg TREM2 tog upp minst skräp; de med medelnivåer gjorde bättre ifrån sig; och hög-TREM2-cellerna var mest glupska. Samma mönster framkom i två olika Alzheimerliknande musmodeller, vilket understryker att TREM2-nivån är tätt kopplad till cellens ”städkapacitet.” Samtidigt visade gen-nätverksanalyser att högre TREM2 inte bara var förknippat med förbättrad metabolism utan också med vissa immunsvarprogram, inklusive interferonrelaterade signaler som kan vara fördelaktiga i vissa sammanhang och skadliga i andra. 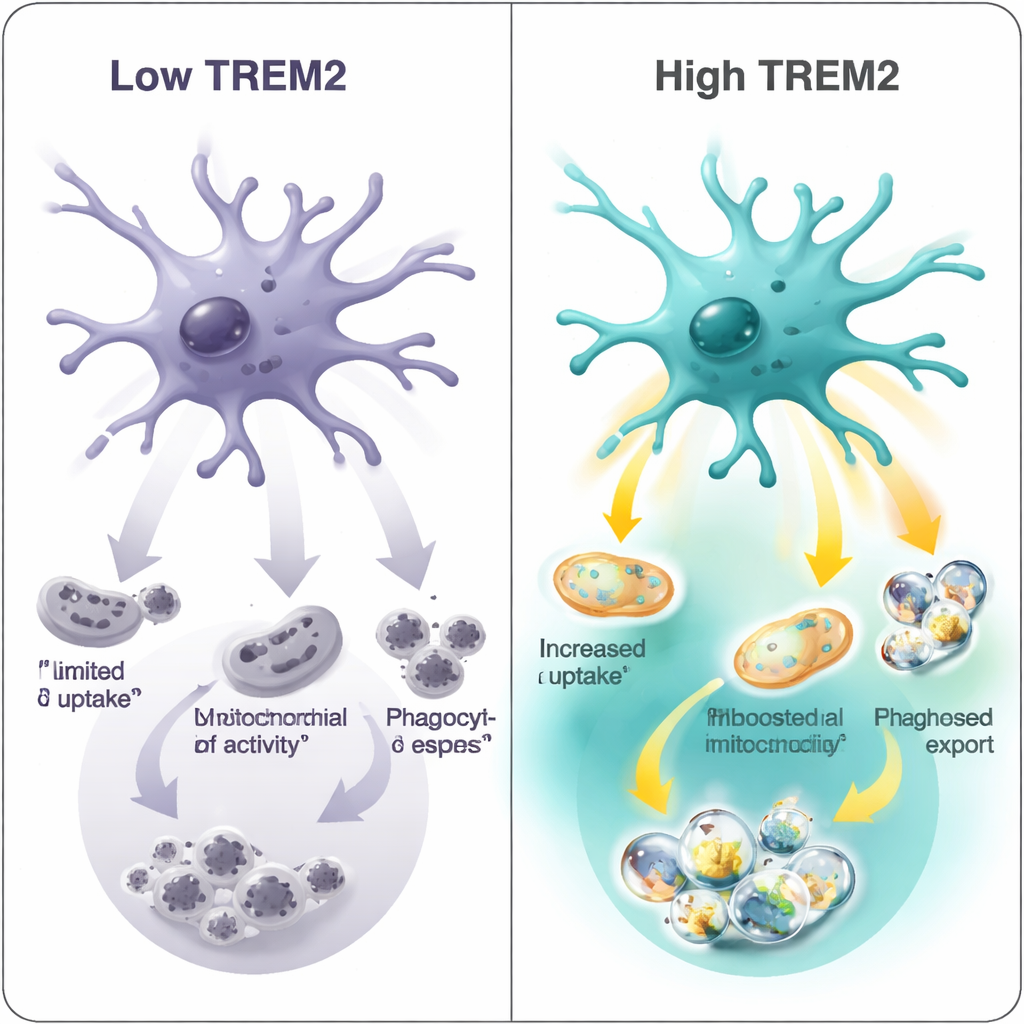
När ökning av TREM2 hjälper — och när det kan bli för mycket
Eftersom läkemedelsföretag testar antikroppar som aktiverar TREM2, undersökte författarna hur ett sådant läkemedel påverkar mikroglia med olika utgångsnivåer av TREM2. De behandlade reportermöss med amyloidpatologi med en TREM2-aktiverande antikropp som kan passera blod-hjärnbarriären och sorterade sedan återigen mikroglia efter TREM2-uttryck. Slående nog svarade cellerna med medelhöga TREM2 starkast: deras metabola markörer visade ökad glykolys, bättre lysosomal och peroxisomal aktivitet och förhöjda nivåer av vissa skyddande membranlipider. Mikroglia med låg TREM2 förändrades knappt, sannolikt för att de inte gav tillräckligt mål för läkemedlet. I hög-TREM2-mikroglia tycktes samma behandling däremot skjuta metabolismen tillbaka mot ett mer måttligt tillstånd, vilket antyder en ”tak-effekt” där överdriven aktivering dämpas snarare än förstärks.
Vad detta betyder för framtida Alzheimer-behandlingar
För en lekmannaläsare är huvudpoängen att mikroglia med rätt mängd TREM2 är bättre drivna, bättre på att hantera kolesterol och bättre på att rensa skadligt material runt amyloida plack. Men balansen är skör. Läkemedel som stimulerar TREM2 kommer sannolikt att fungera bäst inom ett visst fönster av receptornivåer — för lite TREM2 och det finns inte tillräckligt att aktivera; för mycket och systemet kan redan vara nära eller förbi sin optimala punkt. Detta hjälper till att förklara varför en tidig klinisk prövning av en TREM2-ökande antikropp misslyckades och antyder att framtida prövningar kan behöva mäta TREM2-aktivitet och mikroglialt tillstånd över tid, kanske med hjärnavbildning, för att välja rätt patienter och tidpunkt för behandling. Kort sagt omformulerar detta arbete TREM2 som en fint ställbar ”dimmer” för mikroglial metabolism och rengöring snarare än en enkel av/på-brytare, och erbjuder en karta för smartare, mer målade immunterapier vid Alzheimers sjukdom.
Citering: Feiten, A.F., Dahm, K., Schlepckow, K. et al. TREM2 expression level is critical for microglial state, metabolic capacity and efficacy of TREM2 agonism. Nat Commun 17, 2002 (2026). https://doi.org/10.1038/s41467-026-68706-8
Nyckelord: mikroglia, TREM2, Alzheimers sjukdom, hjärnmetabolism, immunterapi