Clear Sky Science · sv
Funktionella och strukturella insikter i interaktioner mellan β-arrestin 1 och Gαs eller Gαi1
Varför detta är viktigt för hälsa och medicin
Många av dagens läkemedel, från allergitabletter till hjärtmediciner och psykiatriska behandlingar, verkar genom att rikta sig mot en stor familj av cellmembranproteiner som kallas G-proteinkopplade receptorer, eller GPCR:er. Dessa receptorer förmedlar budskap in i cellen med hjälp av två huvudhjälpare: G-proteiner och proteiner kallade beta-arrestiner. Denna studie undersöker hur en beta-arrestin (beta-arrestin 1) direkt kommunicerar med två typer av G-proteiner inne i cellen. Att förstå denna dolda konversation kan hjälpa forskare att designa mer precisa läkemedel med färre biverkningar genom att finjustera hur signaler flödar i våra celler.
Två huvudbudbärare inne i våra celler
När ett hormon eller läkemedel binder till en GPCR på cellens yta utlöser det två breda kommunikationsvägar. Den ena vägen använder G-proteiner, som slås på och av som molekylära tidtagare genom att byta ett litet ämne (GDP) mot ett annat (GTP). Den andra vägen använder beta-arrestiner, som både kan stänga av G-proteinsignalering och starta egna signalvägar. Under lång tid har forskare i huvudsak studerat hur receptorer kommunicerar antingen med G-proteiner eller med beta-arrestiner. Nyare arbete antydde dock att G-proteiner och beta-arrestiner också kan binda till varandra eller till och med bilda stora ”mega-komplex” med receptorn. Men detaljerna i hur dessa proteiner kopplar samman och vad det innebär för signaleringen har varit oklara.
Att mäta vem som binder till vem
I denna studie fokuserade forskarna på beta-arrestin 1 och två G-proteinets "alfa"-subenheter: Gαs, som vanligtvis stimulerar cellaktivitet, och Gαi1, som generellt dämpar den. Med en känslig bindningsteknik testade de hur starkt renad beta-arrestin 1 och varje G-protein håller ihop under olika villkor. De fann att nyckelfaktorn inte är om G-proteinet är "på" eller "av", utan om beta-arrestin 1 befinner sig i en mer aktiv, flexibel form. En variant av beta-arrestin 1 som saknar sin svans — och som beter sig som en lös, aktiv uppsättning konformationer — band starkt till både Gαs och Gαi1. Däremot band den vilande formen av beta-arrestin 1, eller en form låst av ett receptor-svans-liknande peptid, svagt eller inte alls. Detta tyder på att G-proteiner föredrar att känna igen beta-arrestin 1 när den provar aktiva-liknande former som kan uppstå efter receptoraktivering. 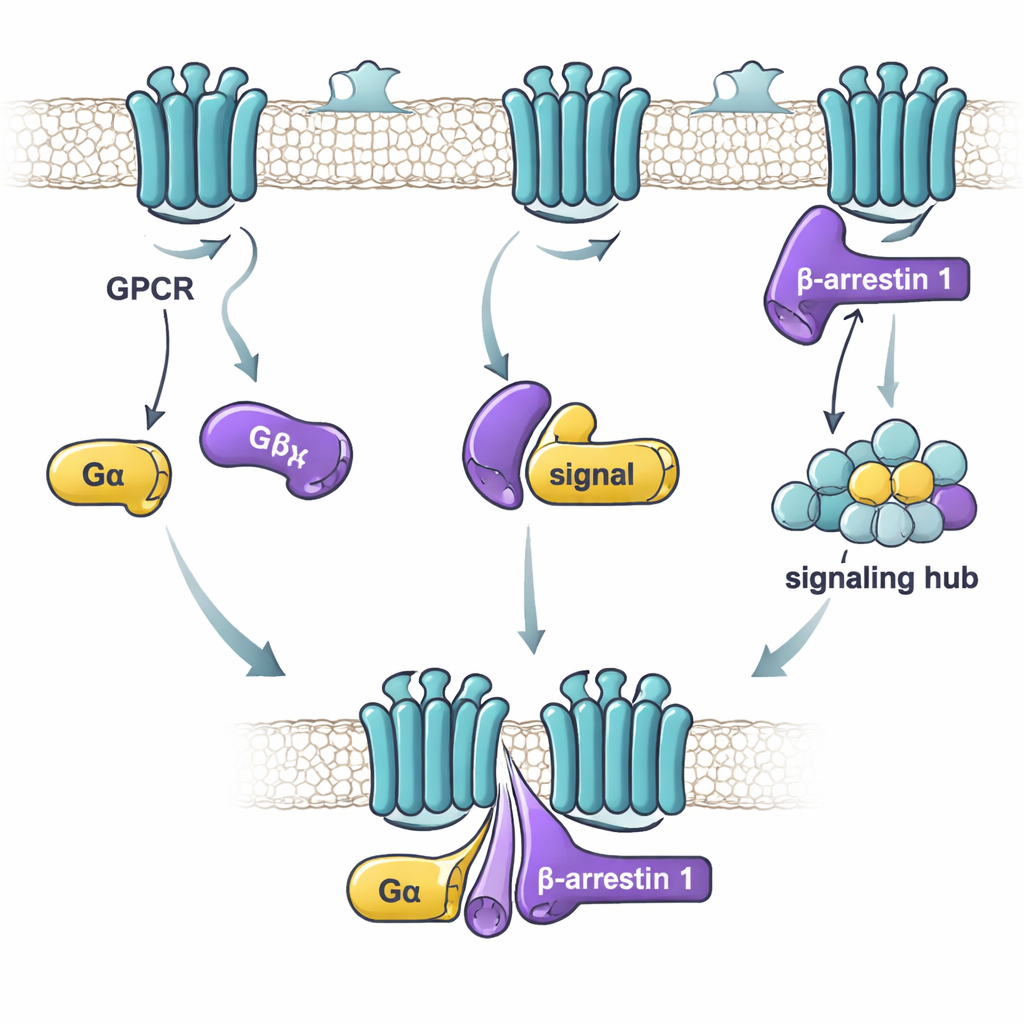
Att observera subtila formförändringar
För att se hur bindning påverkar proteinernas form använde teamet en metod som följer hur snabbt väteatomer i proteinet byts mot tungt väte från lösningsmedlet. Långsammare utbyte betyder oftast att ett område blivit mer skyddat eller styvt; snabbare utbyte betyder att det blivit mer flexibelt eller exponerat. När den aktiv-liknande beta-arrestin 1-fragmentet band till Gαs eller Gαi1 visade båda G-proteinerna tydliga mönsterförändringar i flera regioner, vilket indikerar att de omformade sig kring komplexet. Däremot förändrades beta-arrestin 1 själv endast marginellt, främst i flexibla slingor. Genom att arbeta med isolerade domäner av G-proteinerna visade forskarna också att både den huvudsakliga katalytiska "Ras-liknande" delen och den omgivande alfa-helikala delen bidrar till bindningen. För Gαs spelar den helikala regionen en särskilt stark roll; för Gαi1 är båda regionerna ungefär lika viktiga.
Funktion utan att växla huvudbrytaren
Nästa fråga var om denna direkta kontakt ändrar hur G-proteiner slås på. Teamet använde en fluorescerande GTP-mimik som lyser upp när ett G-protein byter från GDP till GTP, ett standardmått på aktivering. Överraskande nog förändrade inte tillsats av beta-arrestin 1 hastigheten eller graden av detta nukleotidbyte för varken Gαs eller Gαi1. Med andra ord fungerar inte beta-arrestin 1 som ett klassiskt "på-slut"-enzym för G-proteiner. Istället visar dess inflytande sig i dess egen struktur. Med en smart konstruerad beta-arrestin 1 vars svansrörelse kunde följas via fluorescens fann man att aktivt Gαs, men inte Gαi1, ökar frisättningen av beta-arrestins C-terminala svans när ett receptor-deriverat peptid är närvarande. I levande celler bekräftade ytterligare avbildning och energitransfer-sensorer att Gαs och beta-arrestin 1 kommer nära varandra vid hormonstimulering och att Gαs hjälper till att trycka beta-arrestin 1 mot en mer aktiv konformation. 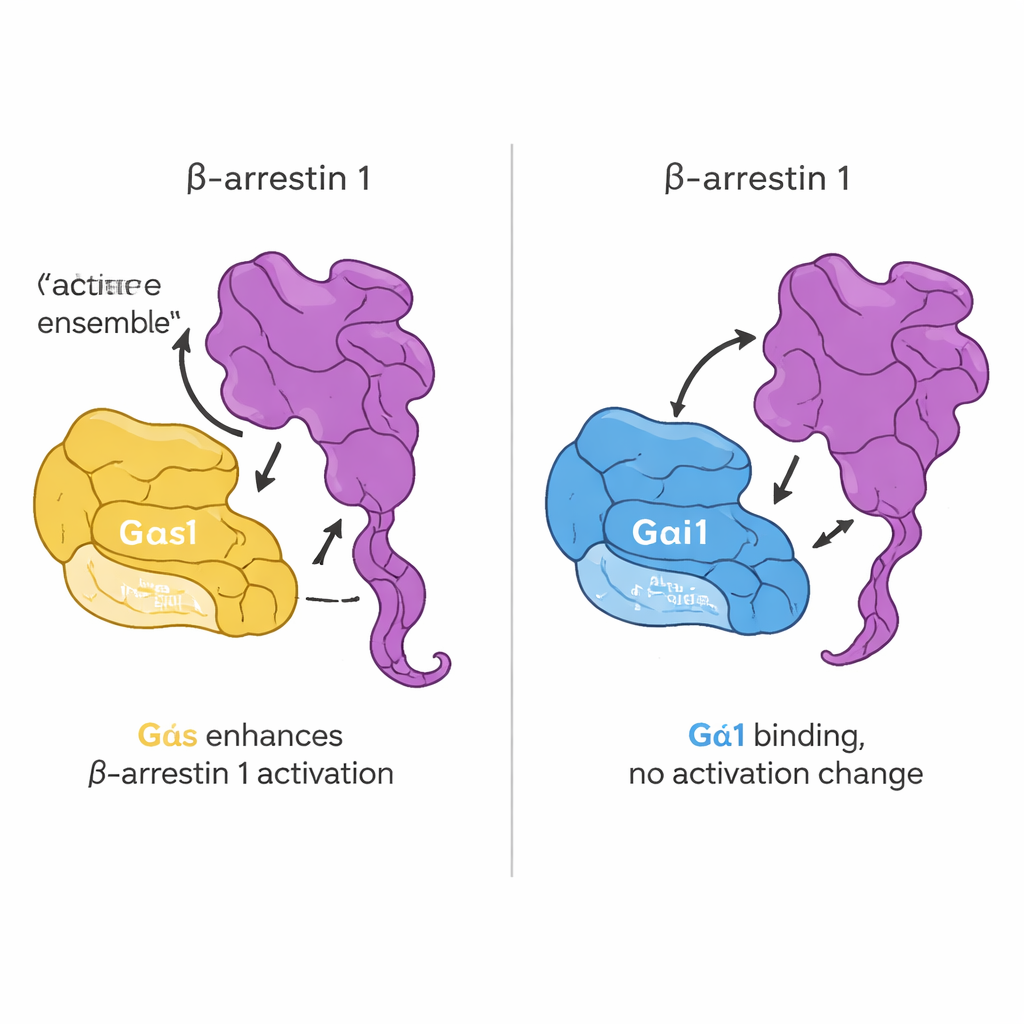
Ett nytt kontrollager i cellsignalering
Sammantaget föreslår studien att Gαs och Gαi1 båda binder direkt till beta-arrestin 1, men på något olika sätt och med distinkta konsekvenser. Ingen av G-proteinerna får sitt huvudsakliga "på/av"-beteende förändrat av denna kontakt. Istället fungerar interaktionen, särskilt för Gαs, mer som en finjusteringsknapp på beta-arrestin 1 och skjuter eller stabiliserar den i en mer aktiv, svans-utsläppt form. Detta lägger till ett tidigare underskattat lager i GPCR-signaleringen: inte bara kan receptorer koordinera G-proteiner och beta-arrestiner, utan G-proteiner och beta-arrestiner kan också påverka varandra direkt. På sikt kan kartläggning av dessa subtila interaktioner hjälpa läkemedelsutvecklare att styra signalering längs gynnsamma vägar — förstärka hjälpsamma banor samtidigt som man undviker sådana som orsakar biverkningar.
Citering: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
Nyckelord: G-proteinkopplade receptorer, beta-arrestin, G-proteinsignalering, cellsignaleringens mekanismer, strukturell biologi