Clear Sky Science · sv
Epigenomöversikt identifierar DNAs metyleringsmediatorer för behandlingsrelaterad kardiometabol risk hos överlevare av barndomscancer
Varför cancerens efterverkningar dröjer kvar i kroppen
Tack vare bättre behandlingar växer numera de flesta barn med cancer upp. Men många av dessa överlevare möter nya hälsoproblem decennier senare, bland annat fetma, högt blodtryck och diabetesliknande tillstånd. Denna studie ställer en angelägen fråga: hur lämnar behandlingar som gavs i barndomen sådana långvariga spår i hjärta och ämnesomsättning? Genom att undersöka kemiska märken på DNA i blodceller upptäcker forskarna ledtrådar som tyder på att tidigare cytostatikabehandlingar och strålning kan ”omprogrammera” kroppen på sätt som ökar långsiktig kardiometabol risk.
Spåra dolda risker hos vuxna som överlevt barndomscancer
Teamet studerade nästan 3 000 vuxna som överlevt barndomscancer och följs i den långsiktiga St. Jude Lifetime Cohort. Dessa överlevare hade som barn fått olika cytostatikabehandlingar och strålning mot hjärnan eller bålen (bröstkorg, buk, bäcken) och återkom år senare för detaljerade hälsoundersökningar och blodprov. Forskarna koncentrerade sig på fem centrala kardiometabola problem som är kända för att öka risken för hjärtsjukdom och för tidig död: fetma, onormala blodsockervärden, höga triglycerider, högt kolesterol och högt blodtryck. Genom att jämföra överlevare med och utan dessa tillstånd sökte de igenom miljontals platser i genomet efter skillnader i DNA-metylering — små kemiska strömbrytare som hjälper till att kontrollera hur gener slås på eller av.
Kemiska märken på DNA som ett minne av behandling
I genomet fann forskarna nästan 1 900 DNA‑platser där metyleringsnivåerna var kopplade till minst ett av de fem kardiometabola tillstånden. De flesta av dessa platser var förknippade med ett enskilt problem, men en mindre grupp verkade vara ”nav” knutna till flera. Fem nyckelplatser, belägna nära två gener kallade CPT1A och LMNA, var associerade med alla fem kardiometabola risker samtidigt. Dessa gener är kända för att påverka hur kroppen hanterar fetter och hur celler upprätthåller sin struktur, vilket antyder att behandling kan störa gemensamma metabola och kardiovaskulära vägar. Många av metyleringsförändringarna överlappade signaler som tidigare setts i allmänbefolkningen, särskilt de kopplade till inflammation, men andra verkade unika för canceröverlevare — vilket tyder på att behandling lämnar sitt eget särskilda biologiska avtryck.
Koppla terapi, DNA‑förändringar och sjukdom
Nästa steg var att testa om dessa metyleringsförändringar faktiskt bidrar till att förklara hur behandling leder till senare sjukdom, snarare än att bara följa med i förloppet. Forskarna fokuserade på nya eller förvärrade kardiometabola problem som utvecklades först efter att blodprovet tagits, vilket bevarade tidsordningen från behandling till DNA‑förändring till sjukdom. Med statistiska medlingsanalyser identifierade de 24 metyleringsplatser som tillsammans förklarade upp till ungefär en fjärdedel av sambandet mellan specifika behandlingar och senare kardiometabola problem. Strålning mot hjärnan och bålen visade särskilt starka mönster: grupper av metyleringsplatser förklarade tillsammans ungefär 10–20 % av effekten av dessa strålbehandlingar på onormala blodsockervärden. En framträdande plats, nära en gen kallad ANTXR2, verkade mediera ungefär 20 % av effekten av bålsstrålning på senare glukosproblem.
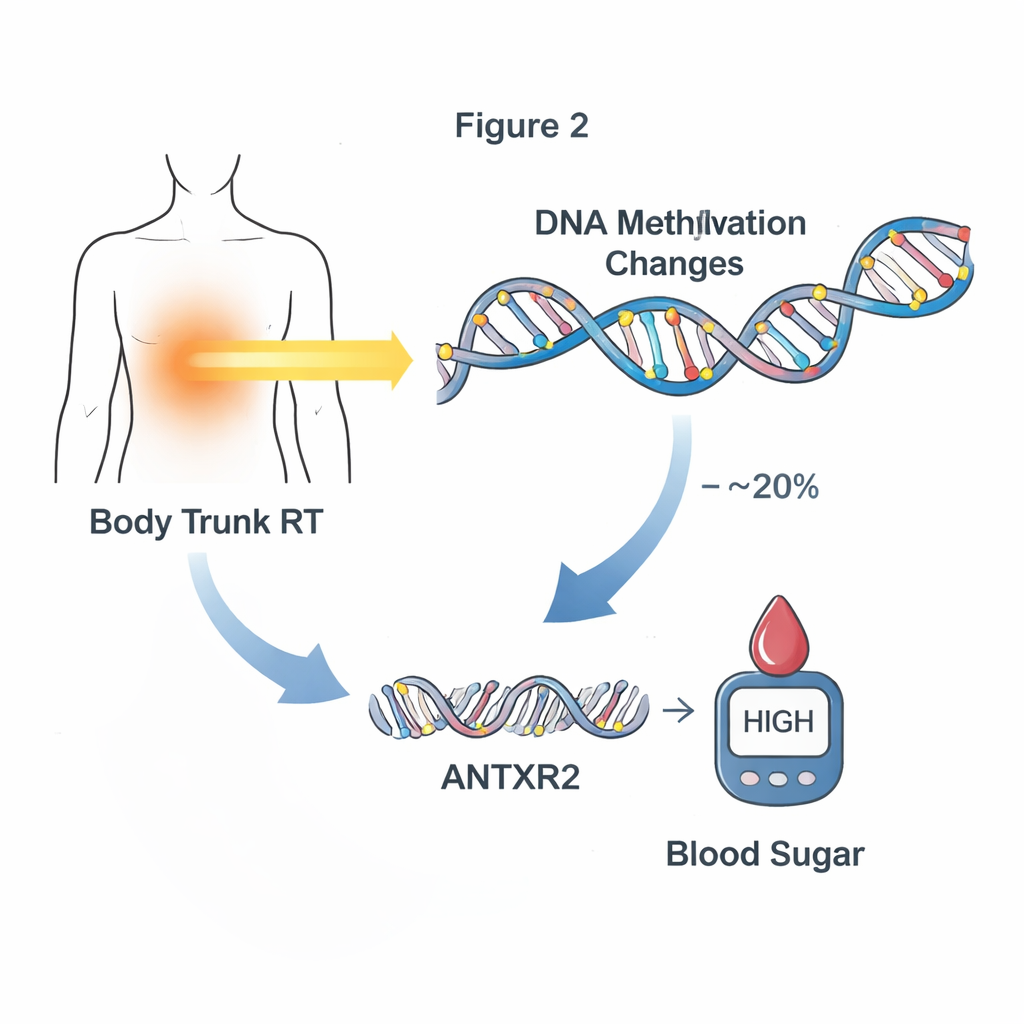
Från DNAs märken till genaktivitet
För att förstå hur dessa metyleringsmärken kan förändra biologin undersökte teamet genaktivitet i en delmängd av överlevare som hade både DNA‑ och RNA‑data från blodet. De fann dussintals metyleringsplatser där högre eller lägre metylering var kopplad till förändrad uttrycks nivå av närliggande gener. Bland dem fanns den viktiga mediatorplatsen nära ANTXR2, där metyleringsnivåerna starkt hängde ihop med hur mycket denna gen uttrycktes, särskilt hos överlevare som fått bålsstrålning. ANTXR2 hjälper till att reglera blodkärl och den omgivande vävnadsstrukturen — system som påverkar hur glukos och insulin rör sig i kroppen. Detta mönster tyder på en händelsekedja där strålning ändrar metylering, vilket förskjuter genaktivitet, vilket i sin tur kan skjuta kroppen mot onormala blodsockernivåer.
Vad detta betyder för överlevare och framtida vård
För icke‑specialister är huvudbudskapet att behandlingar mot barndomscancer inte bara skadar vävnader i stunden; de kan också lämna långvariga ”anteckningar” på DNA som formar hälsan i årtionden. I denna studie hjälpte några av dessa anteckningar — förändringar i DNA‑metylering — till att förklara varför vissa överlevare är mer benägna att utveckla fetma, förhöjda blodfettvärden eller glukosproblem kopplade till diabetes och hjärtsjukdom. Även om dessa kemiska märken bara utgör en del av förklaringen kan de så småningom fungera som blodbaserade biomarkörer för att identifiera de överlevare som löper högst risk och för att testa om livsstilsförändringar eller nya terapier kan skriva om delar av denna epigenetiska historia på ett säkert sätt. Arbetet för flyttar vården av överlevare ett steg närmare precisionsmedicin: att använda molekylära fotavtryck av tidigare behandling för att styra tidigare, mer skräddarsydd förebyggande insatser mot hjärt‑ och metabola sjukdomar.
Citering: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
Nyckelord: överlevare av barndomscancer, DNA-metylering, kardiometabol risk, strålbehandling, epigenetik