Clear Sky Science · sv
Ko-translationell bestämning av kvaternära strukturer i chaperonfabriker
Hurcellens ”monteringslinjer” håller stora maskiner i form
Inuti varje cell måste tusentals proteindelar haka i varandra och bilda komplexa molekylära maskiner, från motorerna som kopierar DNA till fabrikerna som bygger andra RNA-molekyler. Denna studie ställer en till synes enkel fråga med stora konsekvenser: hur bestämmer cellerna, i realtid, vilka hjälpproteiner som ska följa med varje ny del medan den byggs, och hur håller de denna process organiserad i cellens kaotiska vätska?
En allmän hjälpare för cellens megamaskiner
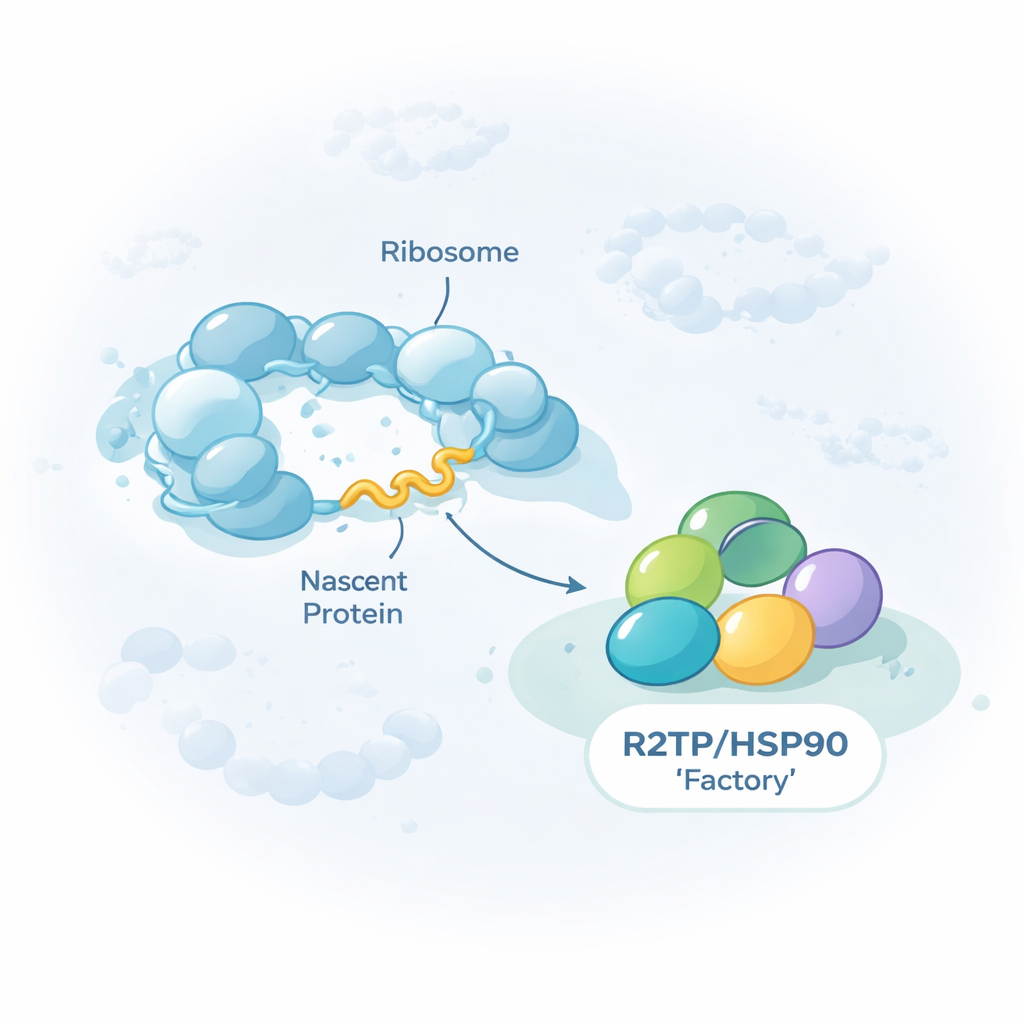
Arbetet fokuserar på en grupp hjälpproteiner, eller chaperoner, kända som HSP90/R2TP. Istället för att vika enstaka proteiner specialiserar sig denna chaperon på att montera jättelika flerpartskomplex, inklusive de tre nukleära RNA‑polymeraserna som transkriberar DNA till RNA, vissa RNA–proteinpartiklar och stora omstrukturerande maskiner som formar om DNA‑paketering. Författarna visar att R2TP inte bara möter dessa klientproteiner efter att de är färdiga. Istället fäster den ofta medan varje klient fortfarande tillverkas på ribosomerna, cellens proteinproducerande maskiner. Genom att dra ner R2TP från humana celler och sekvensera de RNA som följde med, fann de omkring 150 budbärar‑mRNA som kodar för proteiner som R2TP kommer i kontakt med under deras egen translation.
Hjälpare som åker med på växande proteinkedjor
För att testa om detta bindande verkligen sker under proteinsyntes använde teamet läkemedel som fryser eller stör translationen. När de använde ämnen som drar bort växande proteinkedjor från ribosomer försvann de flesta budbärar‑mRNA från R2TP:s grepp. Men när de använde ett läkemedel som helt enkelt pausar ribosomer och lämnar de nästlade kedjorna fästa, ökade R2TP‑bindningen. Konstruerade rapportör‑RNA bekräftade detta: om translationen artificiellt stoppades tidigt band chaperonen inte längre budskapet. Tillsammans pekar dessa resultat på en tydlig insatsregel: R2TP känner igen sina klienter huvudsakligen via den framväxande proteinkedjan som kommer ut ur ribosomen, snarare än via RNA‑sekvensen i sig.
Chaperonbyggda ”fabriker” som samlar specifika budskap
Med avancerad en‑molekylsbildgivning gjorde författarna en överraskande upptäckt. Istället för att se många olika klientbudskap slumpmässigt spridda iakttog de att vissa nyckelbudskap—särskilt de som kodar för stora subenheter av RNA‑polymeras II och en stor splitsningsfaktor kallad PRPF8—ofta samlades i ljusstarka fokalpunkter i cytoplasman. Dessa fokalpunkter var rika på R2TP och dess partner HSP90, liksom på ribosomala komponenter och de proteiner som hölls på att tillverkas, vilket visar att de är aktiva translationsställen. När translation eller den energikrävande ATPas‑aktiviteten hos R2TP eller HSP90 blockerades, löstes dessa fokalpunkter upp. Författarna kallar dessa strukturer ”R2TP‑fabriker”: specialiserade kondensat där utvalda budbärar‑mRNA och chaperoner koncentreras för att gynna snabb, skyddande kontakt mellan framväxande proteinkedjor och deras monteringshjälpare.
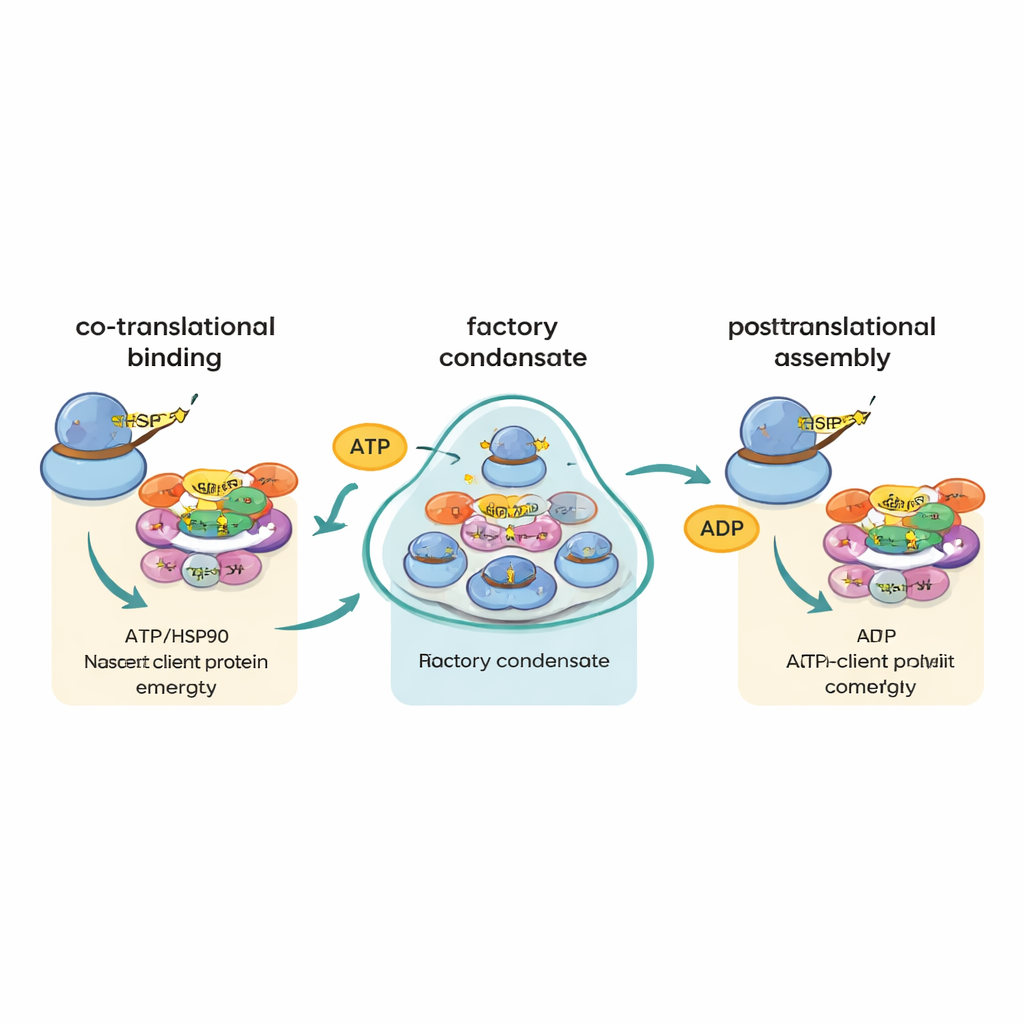
Dirigera delar utan att matcha deras ritningar
En tidigare idé var att budskap som kodar för olika delar av samma komplex kanske hittar varandra och översätts sida vid sida, så att deras proteinprodukter kan monteras omedelbart. Det nya arbetet avfärdar till stor del denna modell om en ”samexisterande ritning”. Även för proteinduetter som är kända för att förenas i samma maskin syntes deras budbärar‑mRNA sällan tillsammans. Istället stöder data en annan strategi som författarna kallar ”ko‑translationell chaperonkanalisering”, eller ”cha‑cha”. I detta upplägg, när varje stort eller monteringsbenäget protein börjar träda fram ur ribosomen, hakar R2TP och HSP90 på och bestämmer dess öde, och vägleder det genom nästa steg i monteringen. Själva fabrikerna för sammanför inte i första hand matchande budskap; snarare ökar de sannolikheten att sårbara nybildade proteiner snabbt möter rätt chaperon.
Varför denna dolda organisation betyder något för hälsa och sjukdom
Genom att avslöja att R2TP och HSP90 inte bara skyddar sköra proteindelar utan också formar var och hur de översätts, blottar denna studie ett oväntat lager av intracellulär organisation. Cha‑cha‑mekanismen hjälper till att förklara hur celler pålitligt bygger enorma molekylära komplex trots att budskapen för deras delar sällan delar samma adress. Den antyder också varför defekter i chaperoner eller deras energicykler kan destabilisera vitala maskiner som RNA‑polymeras och splitsningsfaktorer, med konsekvenser från utvecklingsstörningar till cancer. I grunden visar arbetet att celler förlitar sig på dynamiska chaperon ”fabriker” för att styra nygjorda delar in i rätt komplex, och därigenom hålla sitt inre maskineri både effektivt och ordnat.
Citering: Philippe, M., Salloum, S., Slimani, F. et al. Co-translational determination of quaternary structures in chaperone factories. Nat Commun 17, 1978 (2026). https://doi.org/10.1038/s41467-026-68687-8
Nyckelord: proteinchaperoner, ko-translationell montering, molekylära maskiner, RNA-polymeras, cellulär kvalitetskontroll