Clear Sky Science · sv
Iterativ upptäckt av potenta polymera antibiotika via flerstegs- och flervalsinlärning mot antimikrobiell resistens
Varför nya antibiotika spelar roll för alla
Läkemedelsresistenta infektioner ökar globalt och gör välkända sjukdomar svårare — och ibland omöjliga — att behandla. Denna studie beskriver ett nytt sätt att snabbt upptäcka en annan typ av antibiotikum: små syntetiska polymerer som både kan döda svåra bakterier och återigen göra gamla läkemedel, som penicillin, effektiva. Arbetet förenar avancerad artificiell intelligens med kemi och djurförsök för att söka i ett enormt kemiskt rum som vore omöjligt att utforska genom provning och fel ensam.
Jakt efter nya försvarare i ett trångt kemiskt universum
Traditionella antibiotika riktar sig ofta mot specifika bakterieproteiner, vilka bakterier så småningom kan undkomma. Polymererna i denna studie efterliknar däremot kroppens egna försvarspetider som fysiskt skadar bakteriers membran och är mindre benägna att möta resistens. Utmaningen är att det finns tiotusentals möjliga polymerstrukturer, och deras beteende beror på en fin balans mellan positiv laddning samt vatten- och fettälskande komponenter. Att manuellt testa tillräckligt många kandidater för att hitta säkra och kraftfulla varianter skulle ta år. Författarna byggde ett kombinatoriskt bibliotek på cirka 100 000 relaterade polymerer kallade poly(β-amino-estrar), var och en utformad för att självmontera till nanoskopiska partiklar som kan interagera starkt med bakteriers ytor.
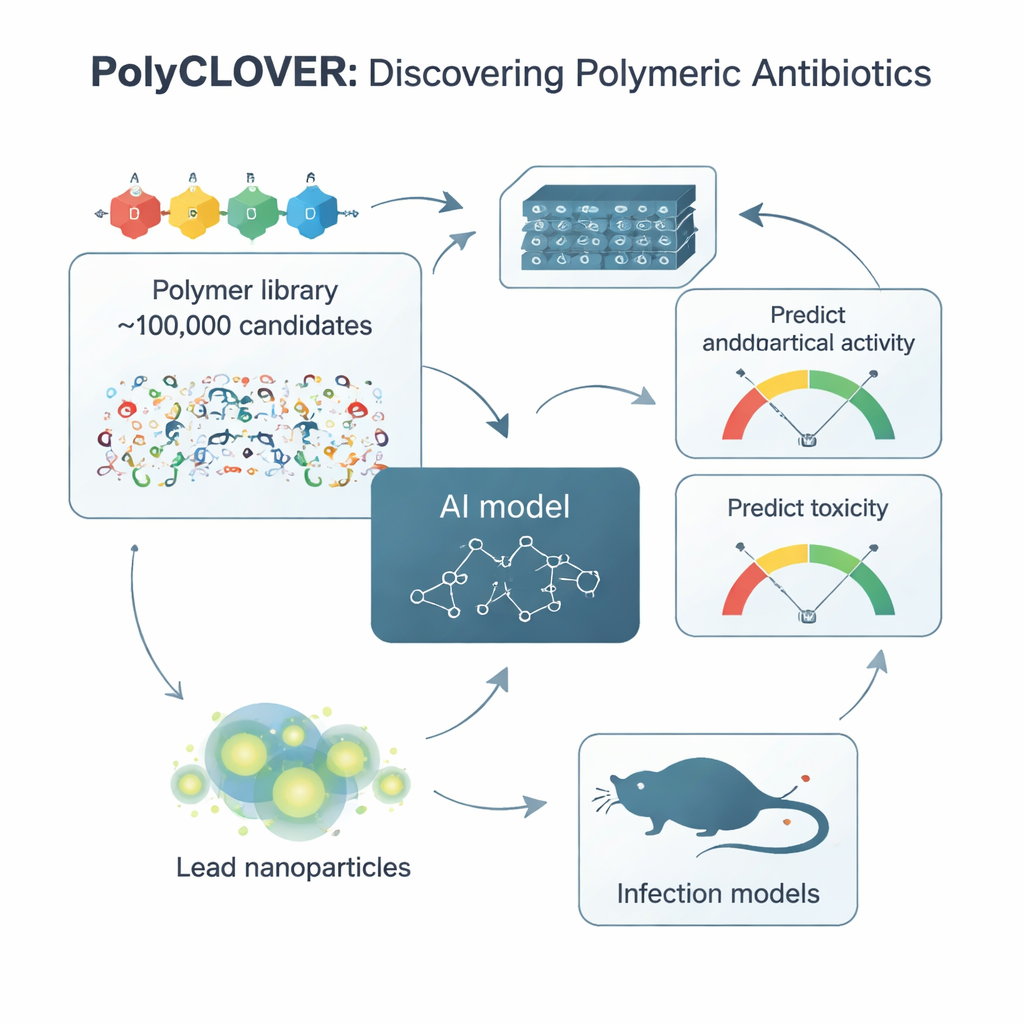
Att lära en AI att läsa polymerers “kroppsspråk”
För att navigera i detta bibliotek skapade teamet ett ramverk de kallar PolyCLOVER. I dess kärna finns ett grafbaserat neuralt nätverk som behandlar varje polymer som ett nätverk av sammankopplade atomer, vilket låter modellen urskilja subtila skillnader i struktur. Eftersom det fanns mycket få markerade exempel på vilka polymerer som var bra eller dåliga antibiotika använde forskarna en flerstegs självlärande strategi. Först tränades modellen på cirka en miljon omärkta polymerstrukturer för att fånga generella kemiska mönster. Därefter tränades den vidare på det omärkta biblioteket med 100 000 medlemmar, och slutligen finjusterades den på en liten uppsättning om 220 polymerer som hade syntetiserats och testats för både antibakteriell styrka och skada på röda blodkroppar. Denna stegvisa inlärning förbättrade dramatiskt modellens förmåga att förutsäga vilka nya polymerer som skulle vara både potenta och säkra.
Låta experiment och algoritmer lära av varandra
PolyCLOVER stannar inte vid ett enda predictionsvarv. Det körs i en loop där AI:n föreslår de mest lovande och mest informativa kandidaterna, kemister tillverkar och testar dem i höggenomströmning, och de nya resultaten matas tillbaka för att förfina modellen. Urvalssteget använder en ”övre konfidensgräns”-metod som balanserar exploatering (att favorisera polymerer som förväntas fungera väl) med utforskning (att pröva osäkra områden där modellen kan lära sig mest). Under cirka fyra iterativa rundor förbättrades de föreslagna polymererna stadigt: de blev mer potenta mot meticillinresistent Staphylococcus aureus (MRSA) samtidigt som de behöll acceptabel toxicitet mot röda blodkroppar. På bara 20 dagar experimenterande konvergerade systemet till en liten uppsättning stjärnpresterare.
Små självmonterande partiklar som slår hål på bakterier
De slutliga tre ledande polymererna, benämnda H1, H2 och H3, formade spontant positivt laddade nanopartiklar omkring 100 nanometer i diameter. I laboratorietester dödade de MRSA lika effektivt som ett standardantibiotikum, streptomycin, och gjorde det mycket snabbare — minskade bakteriemängder med flera storleksordningar inom minuter till timmar, även i proteinrik serum. Elektronmikroskopi och fluorescerande prober visade att dessa partiklar snabbt fäster vid bakterieytan och stör membranets integritet och elektriska potential, vilket gör att cellinnehållet läcker ut. Viktigt är att när MRSA exponerades för dessa polymerer under nästan en månad utvecklade bakterierna mycket liten resistens, i skarp kontrast till streptomycin, vars nödvändiga dos ökade dramatiskt över samma period.
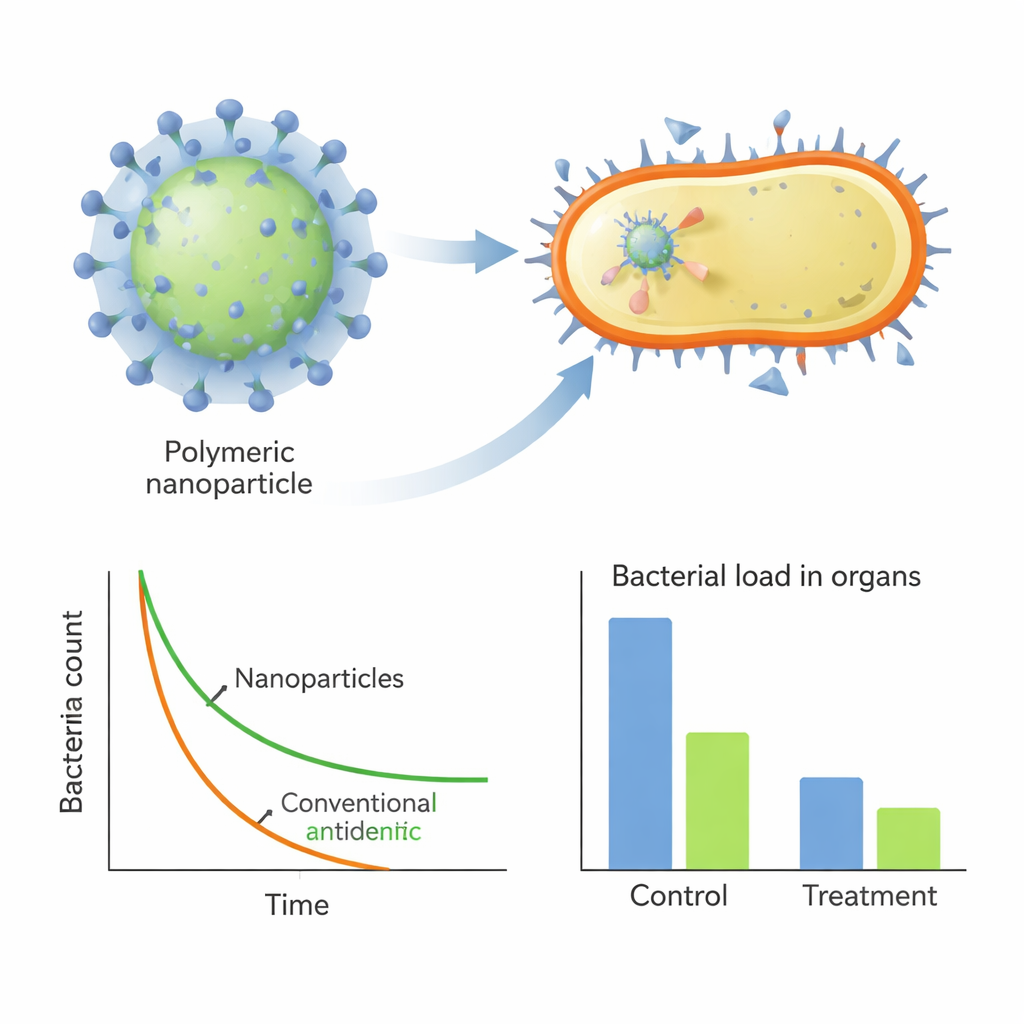
Återaktivera gamla antibiotika i djurinfektioner
Utöver att verka på egen hand fungerade nanopartiklarna även som kraftfulla hjälpmedel för traditionella läkemedel. När de kombinerades med penicillin G, mot vilket MRSA normalt är starkt resistent, bildade den bästa polymeren (H2) nanokompositer som fångade antibiotikumet inuti partikeln. Dessa kompositer visade stark synergi i laboratorietester och reducerade den penicillindos som krävdes för att stoppa MRSA avsevärt. I musmodeller för lunginfektion och en svår bukinfektion minskade behandling med de ledande polymererna — antingen ensamma eller i kombination med penicillin — kraftigt bakterielasten i organen, sänkte inflammatoriska signaler i blodet och begränsade vävnadsskador, allt utan uppenbar toxicitet.
En ny spelbok för smartare antibiotikaupptäckt
För icke-specialister är huvudpoängen att PolyCLOVER visar hur AI och automatiserade experiment kan samarbeta för att upptäcka helt nya typer av antibiotika mycket snabbare än tidigare. Istället för att enbart förlita sig på slump och långsam screening lär sig detta tillvägagångssätt av varje omgång resultat för att rikta in sig på polymerer som både attackerar läkemedelsresistenta bakterier och transporterar konventionella antibiotika dit mer effektivt. Ytterligare arbete krävs innan något av dessa material når kliniken, men studien erbjuder en lovande väg för att fylla på vår krympande arsenal mot resistenta infektioner och antyder en generell strategi för att designa många andra smarta biomaterial.
Citering: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
Nyckelord: antimikrobiell resistens, polymerva antibiotika, nanopartiklar, maskininlärning, läkemedelsresistenta bakterier