Clear Sky Science · sv
Strukturell grund för AP‑4:s dynamiska konformationer och dess bindning till ARF1
Hur celler sorterar och skickar sina laster
Varje cell är ett livligt lager, ständigt upptagen med att sortera och skicka tusentals protein”paket” till rätt destinationer. När detta leveranssystem fallerar i nervceller kan följderna bli allvarliga störningar i hjärnans funktion och rörelseförmåga. Denna studie avslöjar hur en nyckelmaskin för transporter, kallad AP‑4, ändrar form och samarbetar med reglerande proteinet ARF1 för att lasta cargo i små transportbubblor — och varför dess flexibilitet är så viktig för friska neuroner.
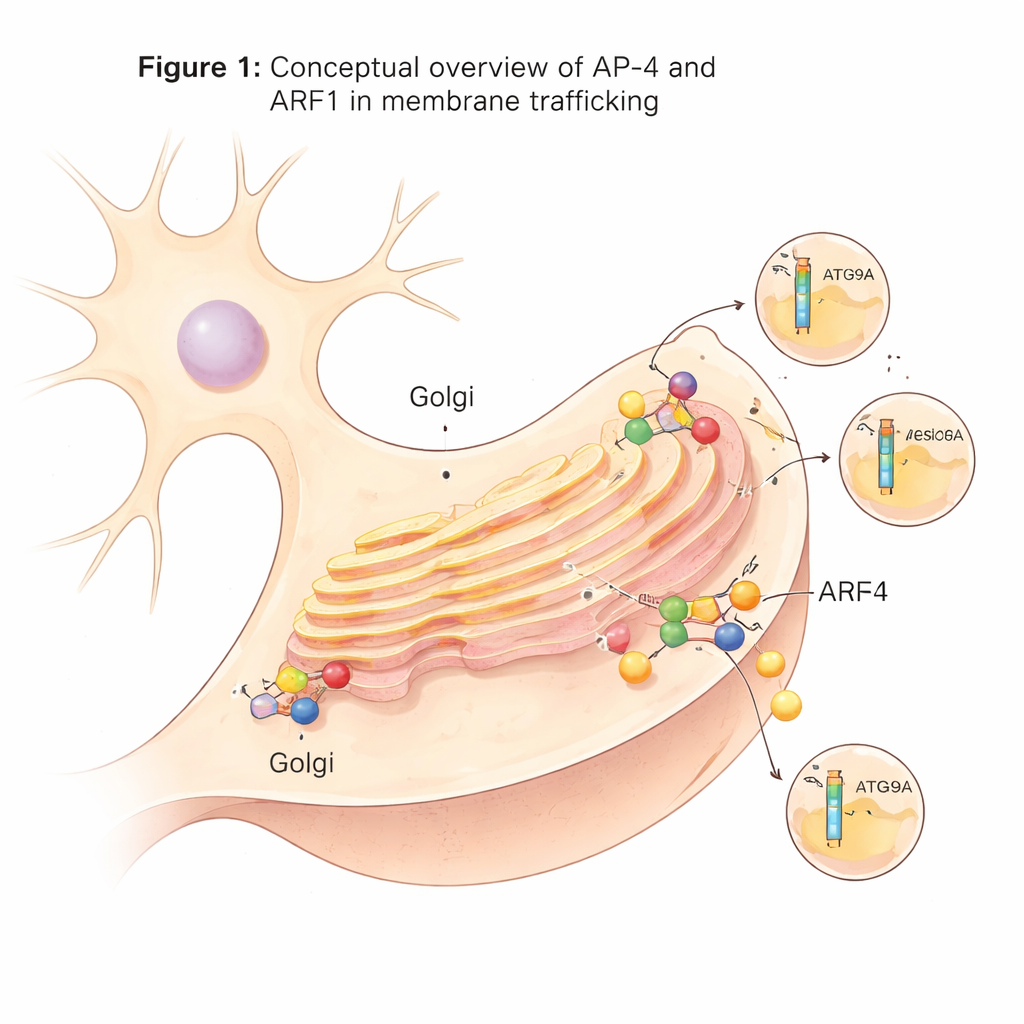
En specialiserad transportmaskin i nervceller
Inuti celler knoppas många transportvesiklar av från en central sorteringsstation känd som det trans‑Golgi‑nätverket. Dessa vesiklar förlitar sig på adaptorprotein‑komplex, eller AP‑komplex, som fungerar som lastningsstationer: de känner igen cargo‑proteiner och hjälper till att bilda beklädda vesiklar runt dem. AP‑4 är ett av dessa adaptrar och är ovanligt eftersom det, till skillnad från många andra, inte använder det vanliga scaffold‑proteinet klathrin. Trots att AP‑4 finns i många vävnader har det en särskilt viktig roll i neuroner. När AP‑4 saknas eller är defekt hos människor misslyckas viktiga cargo‑proteiner, såsom autofagi‑relaterade ATG9A och vissa glutamatreceptorer, att transporteras korrekt, vilket leder till ett allvarligt neurodevelopmentellt tillstånd känt som AP‑4‑bristsyndrom.
Ett formbytande komplex i vila
Författarna använde kryo‑elektronmikroskopi, en kraftfull bildmetod som kan visualisera stora proteinaggregat, för att bestämma den tredimensionella strukturen av AP‑4:s ”kärnkomplex” i lösning. AP‑4 byggs upp av fyra subenheter som tillsammans bildar en skålformad struktur. De upptäckte att AP‑4 inte sitter i en enda rigid form. Istället växlar det naturligt mellan en ”stängd” form, där en subenhet (den mediumsubenhetens C‑terminala domän) är inskjuten i skålens mitt, och en ”öppen” form där denna del svänger ut och blir mycket flexibel. Ytterligare single‑molecule fluorescensexperiment visade att denna subenhet faktiskt antar åtminstone tre positioner — stängd, delvis öppen och helt öppen — vilket visar att AP‑4 är inneboende dynamiskt redan innan det binder till membraner.
ARF1:s roll: rekryterare, inte huvudströmbrytare
Många närbesläktade adaptorcomplex skiftas från en inaktiv till en aktiv konformation genom bindning till små regulatoriska proteiner kallade ARF:er. För att undersöka hur detta fungerar för AP‑4 löste forskarna strukturer av AP‑4 bundet till ARF1, ett litet GTP‑bindande protein som förankrar vid membraner. De fann att ARF1 fäster huvudsakligen vid en av AP‑4:s stora subenheter nära dess N‑terminal, på ett sätt som liknar andra AP‑komplex. Överraskande nog utlöser inte ARF1‑bindning en dramatisk strukturell omställning i AP‑4. De stängda och öppna formerna samexisterar fortfarande, och komplexets övergripande arkitektur förblir i stort sett oförändrad. Biokemiska tester bekräftade att specifika kontaktpunkter mellan ARF1 och AP‑4 är avgörande för membranrekrytering, men ARF1 ensam låser inte AP‑4 i ett enda aktivt läge.
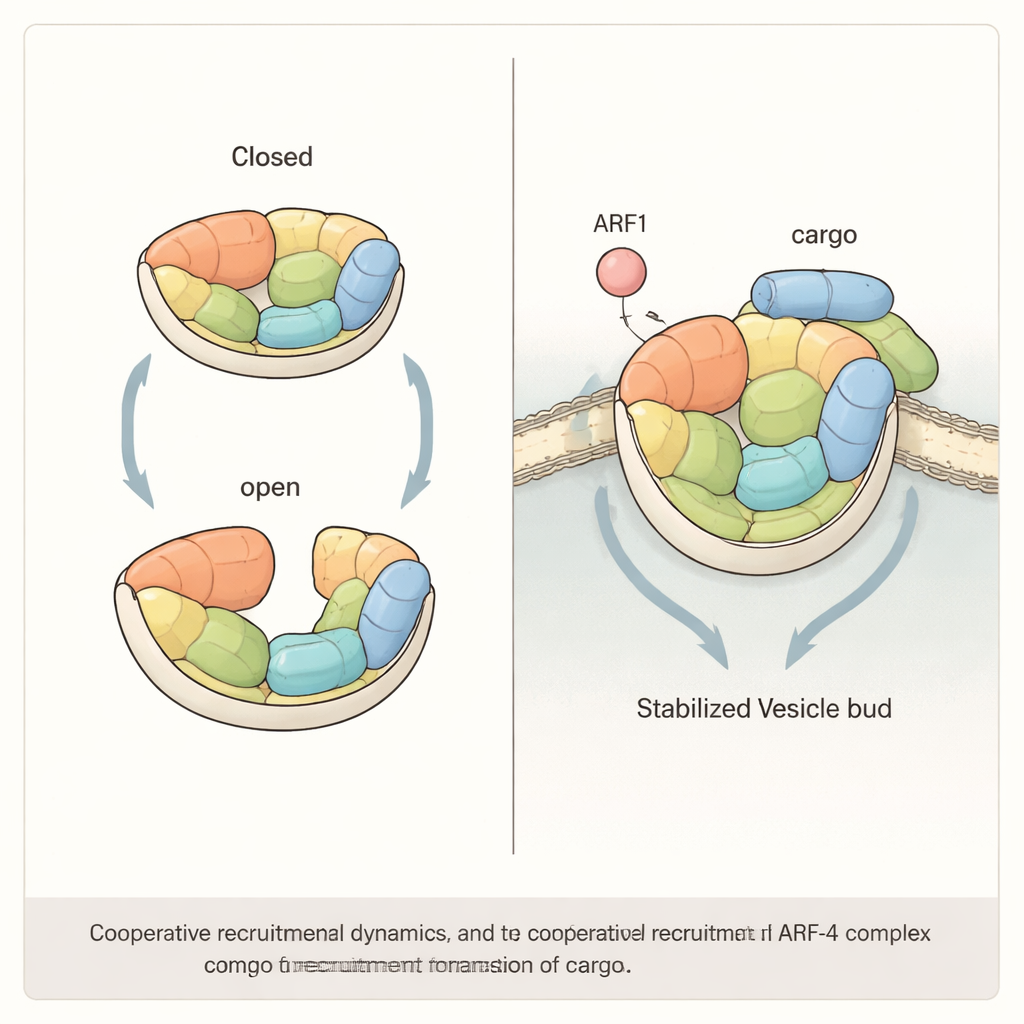
Samarbete mellan regulator och cargo
Studien visar vidare att effektiv rekrytering av AP‑4 till membraner sannolikt kräver samverkan mellan ARF1 och själva cargo‑proteinerna. Genom att rekonstituera systemet på artificiella pärlor och liposomer fann författarna att antingen ARF1 eller en kort svans från cargo‑proteinet ATG9A kan dra till sig AP‑4, men när båda är närvarande tillsammans rekryteras betydligt mer AP‑4 än vad som förväntas av summan av deras individuella effekter. När forskarna konstruerade mutationer som förstyvade AP‑4:s struktur — vilket minskade dess förmåga att växla mellan öppet och stängt läge — försvann denna synergistiska effekt. I humana celler som saknar en nyckel‑AP‑4‑subenhet räckte det inte att återinföra sådana ”styva” mutanta versioner av komplexet för att återställa normal transport av ATG9A från Golgi, vilket understryker att AP‑4:s flexibilitet inte bara är en kuriositet utan ett funktionellt krav.
Varför flexibilitet spelar roll för hjärnhälsa
Sammanfattningsvis framställer arbetet AP‑4 som en formbytande adaptor som antar flera konformationer i lösning och på membraner. Istället för att fungera som en av‑på‑knapp tjänar ARF1 som en membranbaserad rekryterare som samarbetar med cargo‑proteiner för att stabilisera AP‑4 i produktiva konfigurationer för vesikelformation. Att rubba denna balans — antingen genom att försvaga ARF1‑ eller cargo‑bindning eller genom att frysa AP‑4 i en enda form — försämrar export av cargo från Golgi och kan bidra till neurodevelopmentell sjukdom. Genom att avslöja den strukturella grunden för AP‑4:s dynamiska beteende erbjuder denna studie en ram för att förstå AP‑4‑relaterade störningar och antyder framtida strategier för att återställa korrekt transport i drabbade neuroner.
Citering: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
Nyckelord: membrantransport, AP‑4-adapterkomplex, ARF1, vesikelformation, neurodevelopmentell störning