Clear Sky Science · sv
ZNF683+ NK-celler styr keratosensitivitet vid avancerad HPSCC genom att omforma immunmikromiljön
Varför vissa kemoterapier fungerar bättre för vissa halscancer
Personer med avancerad hypofaryngeal cancer — en tumör dold djupt i svalget — står ofta inför tuff kemoterapi med osäkra resultat. Vissa tumörer försvinner, medan andra knappt påverkas. Denna studie ställer en enkel men avgörande fråga: vad skiljer de tumörer som svarar väl? Genom att granska immunceller en och en identifierar forskarna en särskild typ av ”väktarceller” som kan avgöra om standardkemoterapin lyckas eller misslyckas.
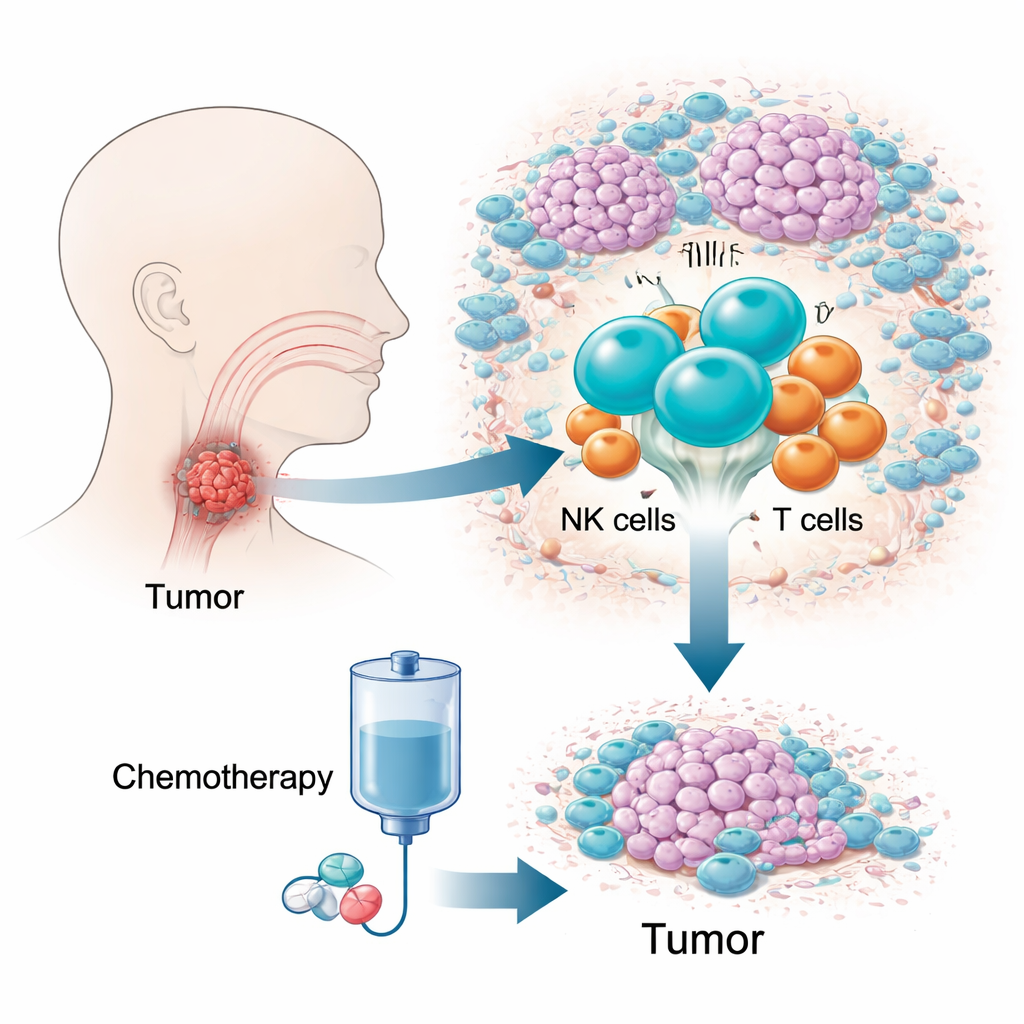
Utmaningen med en dold, svårbehandlad cancer
Hypopharyngeal squamous cell carcinoma är en av de dödligaste huvud- och halscancerformerna, delvis eftersom den växer i ett trångt, svårtillgängligt område och ger få tidiga symtom. Många patienter diagnostiseras sent, när behandlingsmöjligheterna är begränsade och femårsöverlevnaden är låg. En läkemedelskombination känd som TPF-kemoterapi används i stor utsträckning eftersom den kan kontrollera sjukdomen samtidigt som stämbanden bevaras. Ändå visar 10–20 procent av patienterna liten eller ingen respons, vilket innebär förlorad värdefull tid. Traditionella genetiska tester, som summerar signaler över miljontals celler, har haft svårt att förklara denna skillnad, vilket fick författarna att i stället fokusera på tumörens levande ekosystem av immunceller.
Läsa tumörens immunlandskap cell för cell
Forskarna följde 12 patienter över tid, samlade tumörprover före och efter två cykler av TPF-kemoterapi och profilerade mer än 150 000 immunceller med single-cell-upplösning. De undersökte även ytterligare 41 patienter för att bekräfta viktiga fynd med hjälp av bildteknik och flödescytometri. Genom att kartlägga varje cells genaktivitet och typ byggde de en detaljerad atlas av tumörens mikromiljö: T-celler, B-celler, makrofager, dendritiska celler, mastceller, neutrofiler och naturliga mördarceller (NK-celler). Bland alla dessa aktörer framträdde ett mönster. Före behandling hade tumörer som senare krympte betydligt fler NK-celler än de som motstod terapin, och ju högre andel NK-celler desto större blev den slutliga tumörkrympningen.
En speciell NK-cellssubgrupp förbereder T-celler för framgång
När teamet grävde djupare delade de in NK-cellerna i tre grupper baserat på molekylära egenskaper. Endast en av dessa, markerad av transkriptionsfaktorn ZNF683 och till största delen belägen i vävnaden runt tumörnästen, korrelerade starkt med god kemoterapirespons. Patienter vars tumörer innehöll fler av dessa ZNF683+ NK-celler vid baslinjen hade mycket större sannolikhet att dra nytta av TPF. I musförsök gjorde avlägsnande av NK-celler nästan helt bort fördelen av kemoterapi, vilket bekräftar att NK-aktivitet inte bara är en markör utan ett krav för effektiv behandling. Intressant nog agerade dessa NK-celler inte enbart som direkta cancermördare; deras genprogram var i högre grad berikade för att styra och aktivera T-celler.
Hur NK-celler ger grönt ljus åt potenta tumördödande T-celler
För att förstå vilka T-celler som betydde mest följde forskarna individuella T-cellreceptor-kloner före och efter behandling. De fann att hos dem som svarade ökade en specifik grupp CD8 ”effector memory”-T-celler, berikade för molekylen GZMK, dramatiskt efter kemoterapin. Dessa T-celler producerade höga nivåer av de toxiska cytokinernas TNF och interferon-gamma utan att uppvisa djup utmattning, vilket gjorde dem till kraftfulla, uthålliga mördare. Spatial avbildning visade att efter behandling klustrade dessa GZMK+ CD8 T-celler starkt i tumörer från respondenter men inte från icke-respondenter. I laboratorieförsök med samsådd av mänskliga celler drev direkt kontakt med ZNF683+ NK-celler tillväxten av denna GZMK+ CD8 T-cellssubtyp, en effekt som försvann när cellerna skiljdes åt av en barriär.
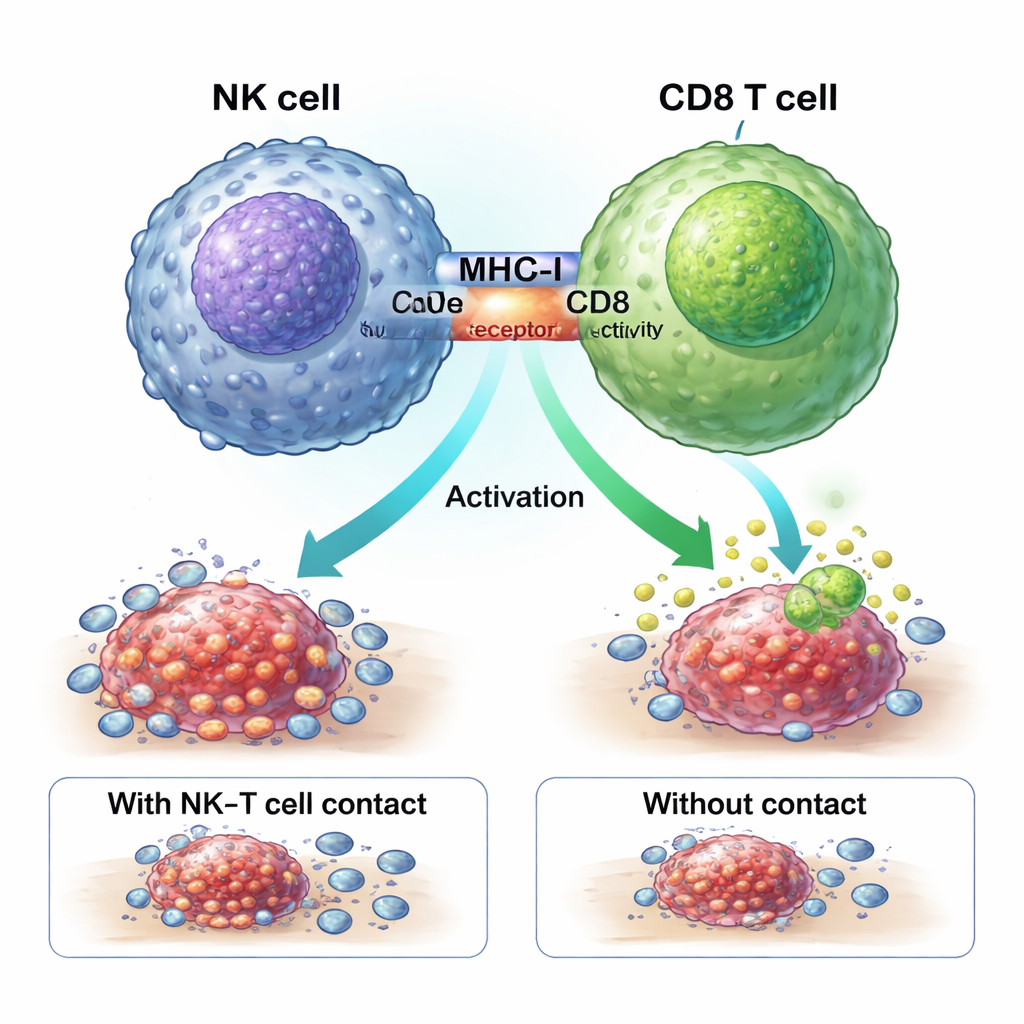
En fysisk handskakning som aktiverar tumörbekämpare
Studien visar att ZNF683+ NK-celler förbättrar kemoterapirespons genom en fysisk ”handskakning” med CD8 T-celler. Molekyler kallade MHC-I på NK-cellens yta engagerar CD8-receptorer på T-celler vid en nära kontaktzon, eller immunologisk synaps. Blockering av MHC-I förhindrade att NK-celler genererade de potenta GZMK+ CD8 T-cellerna. I särskilt konstruerade möss som saknade ZNF683 endast i NK-celler uttryckte dessa NK-celler mindre MHC-I och var mycket sämre på att aktivera CD8 T-celler, vilket förstärker idén att ZNF683 programmerar NK-celler att bli effektiva handledare för T-cellskämpar snarare än enkla bödlar.
Vad detta innebär för patienter
För icke-specialister är huvudbudskapet att inte alla immunceller i en tumör är likadana. Detta arbete identifierar en särskild NK-cellssubgrupp som en spejare som förbereder slagfältet innan kemoterapin börjar. Tumörer rika på dessa celler är redo att släppa loss vågor av starka CD8 T-celler när läkemedlen träffar, vilket leder till mycket bättre krympning. Att mäta förekomsten av denna NK–T-cellaxel före behandling skulle kunna hjälpa läkare att förutsäga vem som får nytta av TPF-kemoterapi och vem som kan behöva alternativa eller tilläggsbehandlingar. I framtiden kan behandlingar som förstärker eller efterliknar dessa ZNF683+ NK-celler förvandla resistenta hypofaryngeala cancerformer till sådana som är mycket känsligare för standardkemoterapi.
Citering: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
Nyckelord: hypofaryngeal cancer, chemotherapy resistance, natural killer cells, tumor immune microenvironment, CD8 T cells