Clear Sky Science · sv
Fotoninducerad selektiv N–N-bindningsbildning genom utnyttjande av nitrenfrisättning och -överföring
Lyser upp en ny väg för att föra ihop kväveatomer
Kväveatomer ligger i centrum för många läkemedel, växtskyddsmedel och avancerade material. Kemister är mycket skickliga på att koppla kväve till kol, men att direkt förena två kväveatomer är betydligt svårare. Denna studie presenterar en ljusdriven, metallfri metod för att föra ihop kväveatomer på ett kontrollerat sätt, vilket öppnar en enklare väg till ett brett spektrum användbara molekyler.
Varför det är svårt att koppla kväve till kväve
Många naturliga produkter och läkemedel innehåller par av kväveatomer bundna till varandra, ett mönster som kan finjustera hur en molekyl beter sig i kroppen eller i material. Befintliga sätt att bygga dessa N–N-enheter utgår vanligtvis från färdiga kväve–kväve-fragment, såsom hydraziner eller diazo-föreningar, och modifierar dem steg för steg. Att direkt skapa N–N-bindningen från enkla aminer är lockande men svårt: kväve är relativt elektronegativt, så två kväveatomer bildar inte naturligt en stabil, opoler bindning. Tidigare framgångar har i hög grad förlitat sig på övergångsmetallkatalysatorer och fungerar ofta endast för snäva familjer av molekyler, vilket begränsar deras användbarhet i upptäcktskemin.
Använda ljus för att tygla en reaktiv mellanprodukt
Författarna vände sig till nitren—mycket reaktiva, kortlivade kvävearter som i princip kan infogas i andra bindningar. Traditionell nitrenkemi kräver vanligtvis metallkatalysatorer och kan drabbas av sidoreaktioner eftersom nitren är så energirika. Gruppen undersökte om de kunde generera nitren med hjälp av ljus på ett mildare, mer kontrollerat sätt, utan några metaller, och sedan använda dem för att länka enkla aminer till produkter som innehåller N–N-enheter. Deras centrala insikt var att använda sulfiliminer, en familj av molekyler som är lätta att skräddarsy och som absorberar ultraviolett och närliggande synligt ljus. När de belyses kan dessa sulfiliminer klyvas så att ett nitrenfragment frigörs samtidigt som en ofarlig svavelhaltig biprodukt återbildas.
En bred, metallfri receptur för kvävepar
Efter systematisk testning identifierade forskarna en särskild sulfilimin som under 365 nanometers ljus i kloroform reagerar effektivt med många aminer och ger hydrazidprodukter—molekyler med en nybildad N–N-bindning intill en karbonylgrupp. De optimerade faktorer som sulfiliminstruktur, lösningsmedel och ljusintensitet för att gynna önskad produkt framför vanliga biprodukter som ureat. Under dessa milda förhållanden kopplade en mängd olika aminer, inklusive aromatiska och alifatiska typer samt cykliska varianter, framgångsrikt. De visade också att många olika sulfiliminer, med både aromatiska och alifatiska acylgrupper och sulfonylgrupper, deltar väl och ger flera dussin skilda N–N-innehållande produkter. Viktigt är att metoden kan tillämpas sent i en syntes för att modifiera komplexa, biologiskt aktiva molekyler såsom vanliga antiinflammatoriska läkemedel och chirala byggstenar, vilket visar dess praktiska användbarhet inom läkemedels- och materialkemi.
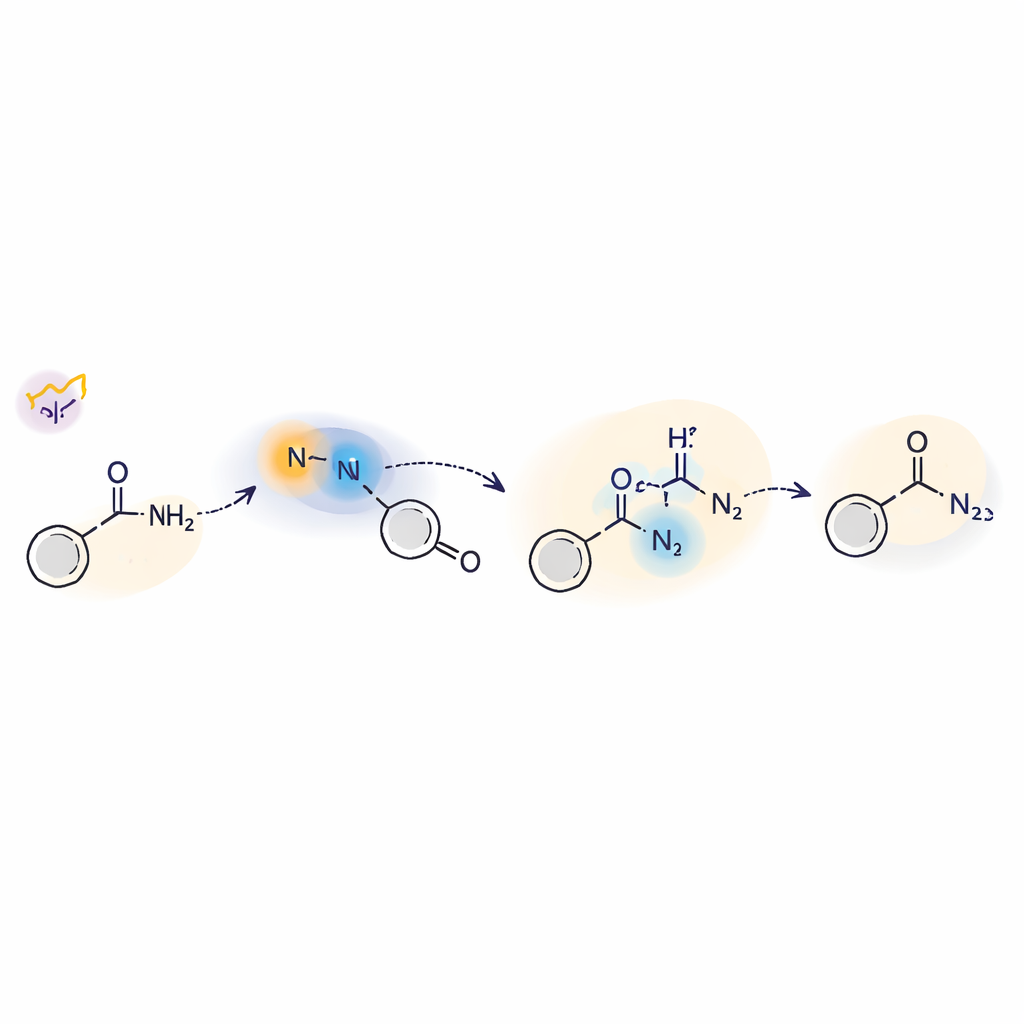
En titt under huven på det ljusdrivna steget
För att förstå hur denna ljustriggade kemi fungerar kombinerade teamet experiment och teori. De använde radikalfällor, isotopmärkning och elektronparamagnetisk resonans för att visa att fria nitrenintermediärer och kvävecentrerade radikaler uppträder under reaktionen. Tidsupplöst laserspektroskopi avslöjade två nyckelformer av nitrenen: ett kortlivat triplettillstånd och ett längre levande singlettillstånd. Singletformen reagerar direkt med aminer via en form av nukleofil attack, medan tripletformen kan delta i väteatomöverföringssteg. Beräkningskemi stödde en mekanism där ljus exciterar sulfiliminen, dess svavel–kvävebindning klyvs, och den resulterande nitrenen sedan engagerar aminen genom både singlet- och tripletvägar innan den slutligen omvandlas till den färdiga hydrazidstrukturen.
Vad detta betyder för framtida molekyler
Detta arbete visar att noggrant utformade sulfiliminer kan fungera som ”nitrenreservoarer” som frigör reaktiva kväveenheter på begäran under ljus, utan hjälp av metaller. Genom att utnyttja både nitreners singlet- och tripletpersonligheter samtidigt som deras koncentration hålls låg, uppnår metoden selektiv bildning av N–N-bindningar över ett brett spektrum byggstenar. För icke-specialister är slutsatsen att kemister nu har ett enklare, renare och mer flexibelt sätt att sy ihop kväveatomer, vilket kan påskynda skapandet av nya läkemedel, växtskyddsmedel och kväverika material.
Citering: Yu, M., Feng, J., Wang, X. et al. Photo-induced selective N-N bond construction via harnessing nitrene release and transfer. Nat Commun 17, 2084 (2026). https://doi.org/10.1038/s41467-026-68674-z
Nyckelord: nitrenkemi, fotoninducerade reaktioner, N–N-bindningsbildning, sulfiliminer, hydrazider