Clear Sky Science · sv
Reglering av AP1-adaptorsammansättning av den tvåhövade chaperonen MEA1
Varför denna dolda hjälpare i cellen är viktig
Inne i varje människocell transporterar tusentals små paket proteiner dit de behövs eller till cellens "återvinningscentral" för nedbrytning. Denna trafik håller våra celler friska och våra immunsvar under kontroll. Artikeln som sammanfattas här avslöjar ett tidigare mystiskt protein, kallat MEA1, som visar sig vara avgörande för att bygga en av de viktigaste sorteringsmaskinerna som lastar dessa paket. Att förstå hur MEA1 fungerar bidrar till att förklara hur celler kontrollerar viktiga laster, inklusive molekyler som slår på och av antivirala immunsvar.
Trafikstyrning vid cellens fraktnav
Stor del av cellens fraktaktivitet går via en struktur kallad Golgi, en stapel av tillplattade säckar som fungerar som ett centralt postkontor. Från Golgi kan last skickas ut för användning vid cellens yta eller omdirigeras till inre kompartment för nedbrytning. Ett proteinkomplex känt som AP1 sitter i centrum för denna väg. AP1 känner igen märkningar på lastproteiner, hjälper till att böja membranet och rekryterar ett yttre hölje av klathrin för att bilda små transportvesiklar. Utan korrekt sammansatt AP1 ansamlas viktiga laster på fel ställen och normala signalvägar, inklusive de som är kopplade till immunitet, kan störas. 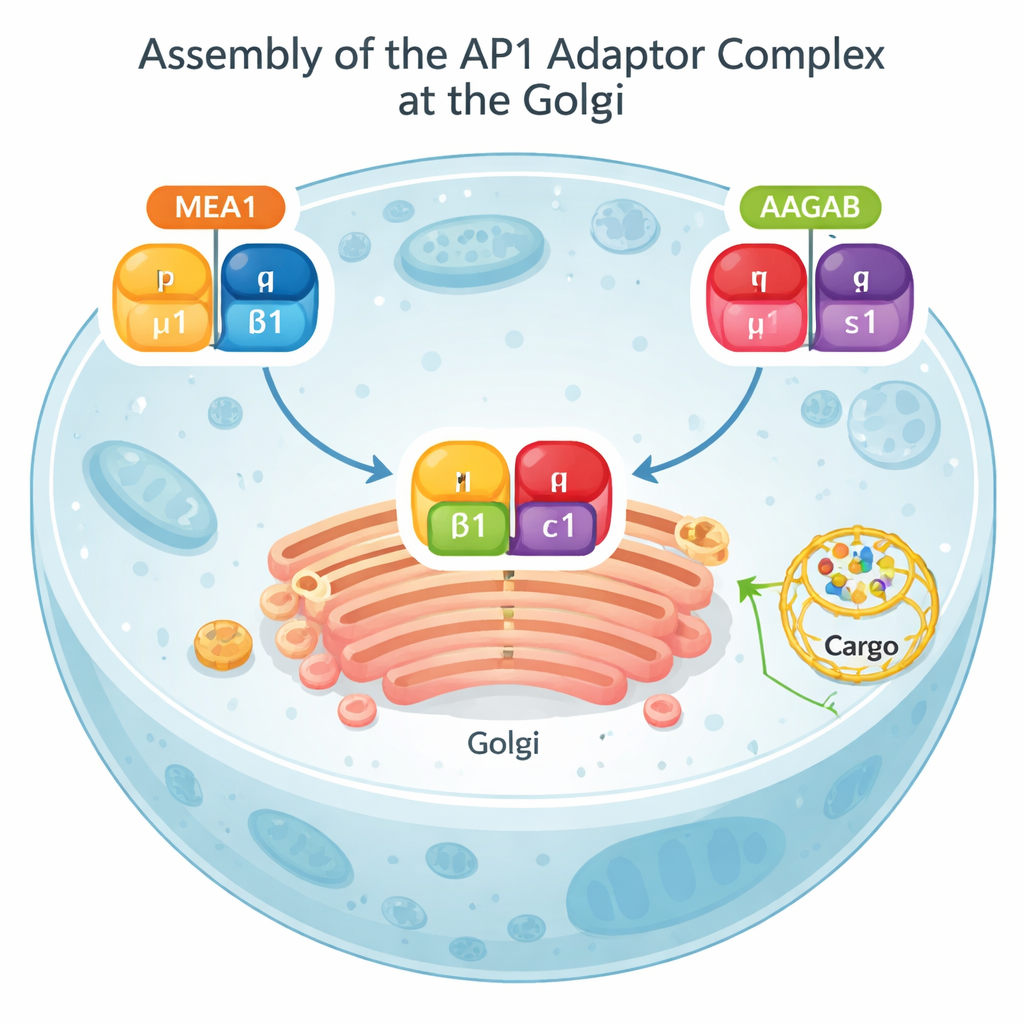
Att hitta en saknad monteringsarbetare
Författarna gav sig i kast med att identifiera proteiner som fysiskt associerar med AP1 och som kan hjälpa det att monteras. De sökte i en stor databas över protein–interaktioner, filtrerade bort kandidater som sannolikt inte samarbetade med AP1 och använde sedan ett artificiellt intelligens-verktyg, AlphaFold, för att förutsäga hur de återstående proteinerna kan kontakta AP1:s individuella delar. Denna sökning framhöll MEA1, ett litet och tidigare okaraktäriserat protein som finns i många vävnader. Uppföljande experiment i humana celler bekräftade att MEA1 binder två specifika AP1-subenheter, kända som μ1 och β1, både när de testades separat och i sina naturliga, omodifierade former.
MEA1 håller AP1 intakt och cellens laster i rörelse
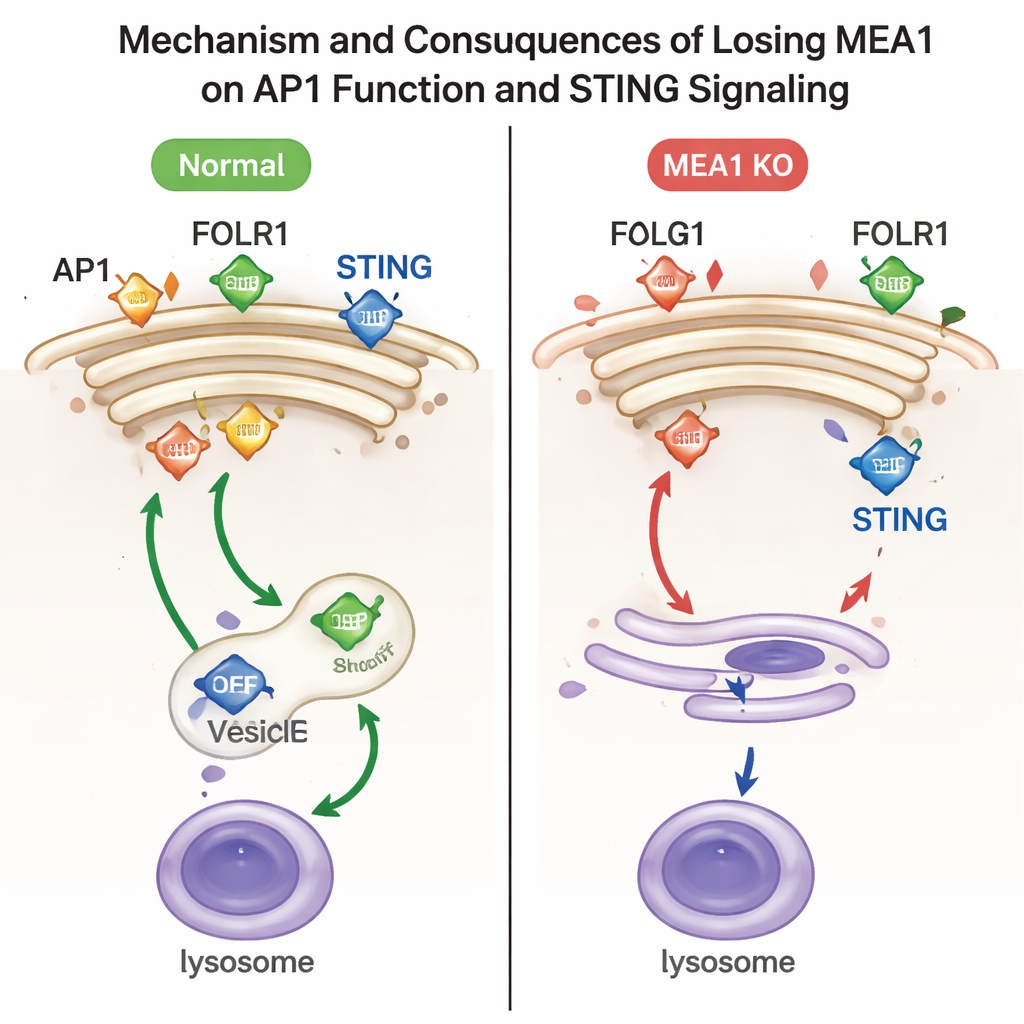
För att undersöka vad MEA1 faktiskt gör raderade forskarna MEA1-genen i humana cellinjer. När MEA1 saknades minskade alla fyra delarna av AP1 drastiskt, och typiska AP1-fläckar nära Golgi nästan försvann. Denna förlust hade tydliga funktionella konsekvenser. En AP1-last, folatreceptorn FOLR1, ansamlade sig vid cellytan istället för att skickas inåt, ett kännetecken för felaktig AP1-sortering. En annan last, immunsignalproteinet STING, packades inte längre effektivt i vesiklar på väg till lysosomerna, cellens återvinningscentraler. Som ett resultat var aktiverad STING och dess partnerkinas TBK1 kvar på höga nivåer, vilket indikerar att "avstängningsknappen" för denna antivirala väg inte fungerade som den skulle. Återinförande av MEA1 återställde AP1-nivåerna och rättade till dessa trafikfel.
En tvåhövdad chaperon och en kollisionsbaserad byggprocess
Biokemiska tester och AlphaFold-modeller visade att MEA1 beter sig som en "tvåhövdad" monteringschaperon: dess främre del greppar subenheten μ1, medan dess bakre del greppar β1. Mu1 och β1 är på egen hand instabila och tenderar att klumpa ihop sig eller förstöras; bundna till MEA1 blir de lösliga och redo att monteras. En annan känd chaperon, AAGAB, utför ett parallellt jobb för de återstående två AP1-subenheterna, γ och σ1. När MEA1–μ1–β1- och AAGAB–γ–σ1-komplex möts förenas deras subenheter till ett komplett, fyrdelat AP1-adaptor. Vid den tidpunkten släpper båda chaperonerna och återvänder till cellvätskan, medan det nybildade AP1 förflyttar sig till membran för att utföra sitt sorteringsarbete. Denna "dubbel-chaperon-kollision"-mekanism visar att AP1-assembly är noggrant orkestrerad snarare än överlämnad åt slumpen.
Vidare lärdomar om cellulär kvalitetskontroll
Bortom AP1 antyder studien en mer generell strategi som celler kan använda för att bygga många stora proteinkomplex. MEA1 kan också svagt bistå med en annan adaptor, AP2, och tillsammans med AAGAB och en tredje chaperon vid namn CCDC32 illustrerar det en bredare väg som författarna kallar "Chaperone-assisted Adaptor Protein Assembly". I detta upplägg stabiliserar specialiserade chaperoner sköra subenheter, för de rätta paren samman och blockerar tillfälligt lastbindande ytor tills komplexet är fullt bildat och säkert att använda.
Vad detta betyder för hälsa och sjukdom
För icke-specialister är huvudpoängen att MEA1 är en avgörande bakom-kulisserna-arbetare som hjälper till att montera AP1, en kärnsorteringsmaskin i våra celler. När MEA1 saknas faller AP1 sönder, trafikstockningar uppstår och viktiga regulatorer som STING stängs inte av på rätt sätt. Denna nya förståelse kan så småningom hjälpa till att förklara vissa immunrelaterade störningar eller andra sjukdomar kopplade till felaktig proteintrafik, och den visar en allmän princip för hur celler säkert bygger komplexa molekylära maskiner av instabila delar.
Citering: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
Nyckelord: proteintrafik, adaptorprotein AP1, molekylära chaperoner, STING-signalering, cellbiologi