Clear Sky Science · sv
Molekylär igenkänning av tyroglobulin av sortilin
Hur sköldkörtelceller avgör när de ska släppa hormon
Sköldkörtelhormoner hjälper till att ställa in vår metaboliska ”termostat”, och påverkar allt från hjärtfrekvens till kroppstemperatur. Dessa hormoner byggs upp och lagras i ett jätteprotein som kallas tyroglobulin. Denna studie avslöjar hur ett annat protein, sortilin, hjälper sköldkörtelceller att välja vilken form av tyroglobulin som ska tas in i cellen igen så att hormonet kan frisättas till blodet — ett beslut som i slutändan påverkar hur mycket sköldkörtelhormon våra kroppar utsätts för.
Ett lagringsprotein som väntar på att bearbetas
Tyroglobulin är ett massivt, Y-format protein som produceras och utsöndras av sköldkörtelceller till en geléliknande vätska kallad kolloid. Där fungerar det både som råmaterial och lager för sköldkörtelhormon: specifika byggstenar (aminosyror) inom tyroglobulin modifieras kemiskt med jod för att bli sköldkörtelhormon, fortfarande inbäddade i det större proteinet. För att faktiskt frigöra dessa hormoner måste tyroglobulin tas tillbaka in i cellen, klippas upp i återvinningskompartiment kallade lysosomer, och dess hormonfragment transporteras ut till blodet.
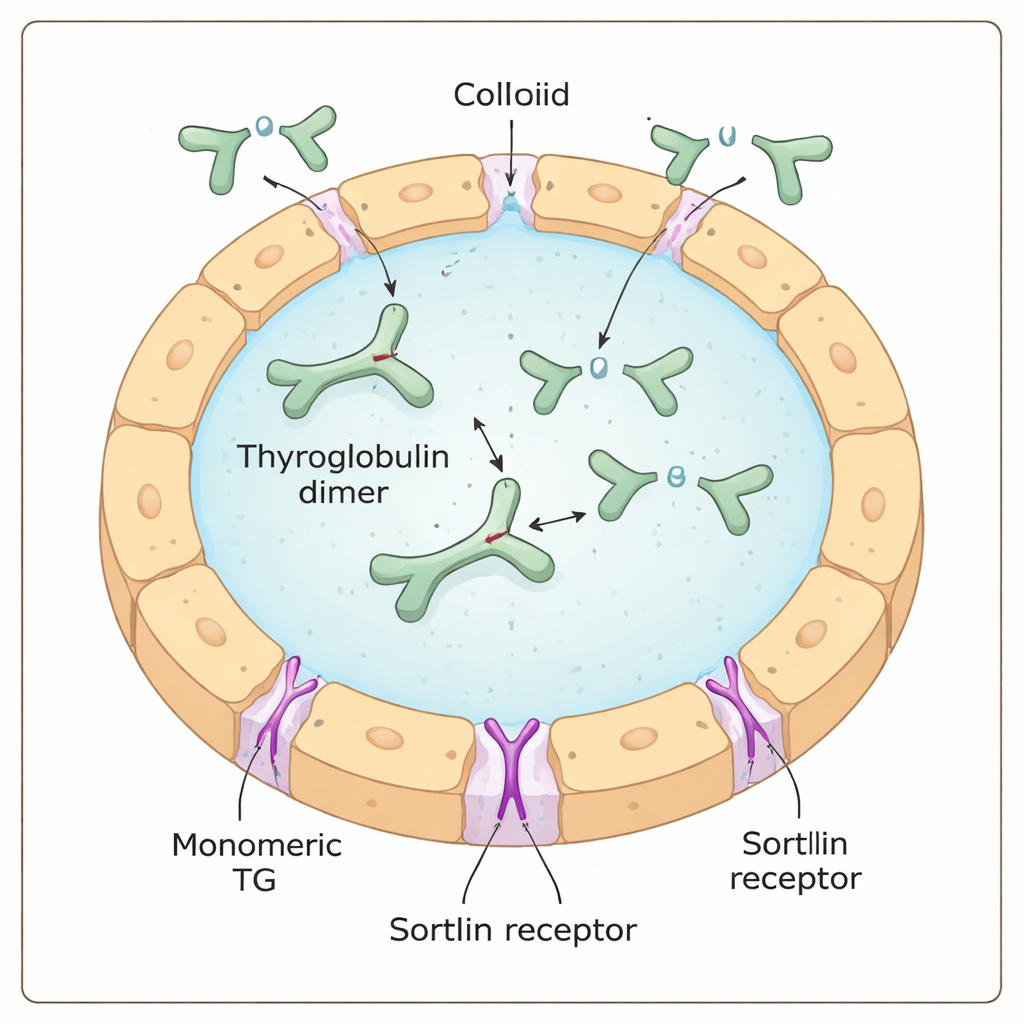
En cellulär grindvakt med dold preferens
Receptorn sortilin har föreslagits vara en av de ”grindvakter” som binder tyroglobulin vid cellytan och styr det inåt. Tidigare arbete antydde att sortilin föredrar starkt jodifierat tyroglobulin, vilket gav intryck av att receptorn kan mäta jodinnehåll direkt. Genom att kombinera biokemiska tester, massmätningar på enskilda molekyler och cellbaserade upptagsexperiment fann författarna istället att sortilin starkt favoriserar en enkel-enhetsform, eller monomer, av tyroglobulin framför dess vanligare parade, dimeriska form. Ju mer monomer i ett prov, desto effektivare bildades komplex med sortilin och togs upp av sköldkörtelcellerna, oberoende av hur mycket jod det bar.
Inzoomning på kontaktpunkten
För att förstå denna preferens på atomnivå vände sig teamet till högupplöst kryo-elektronmikroskopi och korsbindande masspektrometri. Dessa metoder visade att sortilin känner igen en kort, rörlig svans i C-terminalen (en ände) av monomeriskt tyroglobulin. Denna svans träs in i en central kavitet i sortilin, formad som en ti-bladig propeller, och dockar vid två små ”heta punkter” inuti. Slående nog är en del av området runt denna svans begravt i den dimeriska formen av tyroglobulin där sortilin inte kan nå det, vilket förklarar varför dimerer är dåliga partners. Data tyder på att extracellulär trimning eller uppluckring av tyroglobulin — genom naturlig proteinnedbrytning — hjälper till att omvandla dimerer till monomerer som sortilin kan fånga.
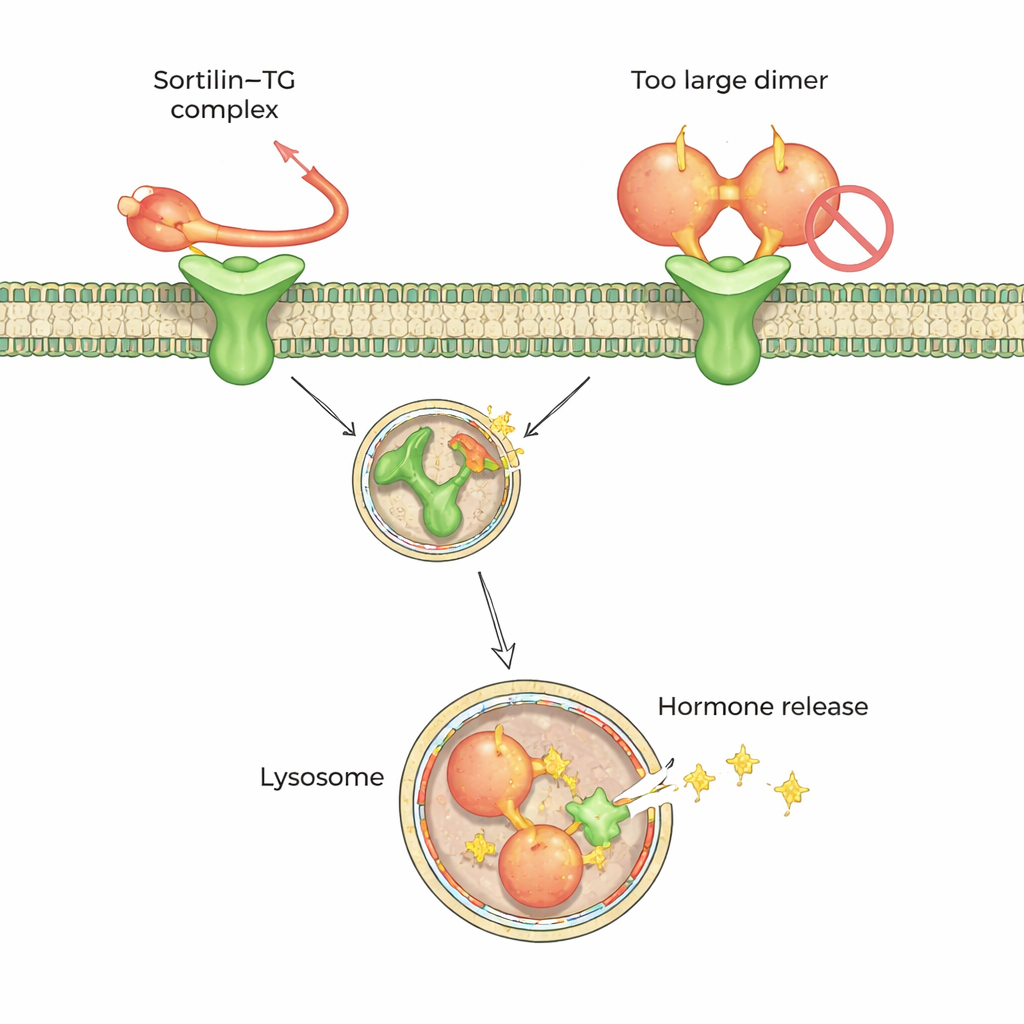
En delad dockningskod för många lastproteiner
Sortilin är inte bara ett sköldkörtelprotein; det hjälper till att transportera många olika molekyler i kroppen, inklusive faktorer kopplade till hjärtsjukdom och hjärnrelaterade störningar. Genom att kombinera deras strukturarbete med avancerade strukturprediktionsverktyg som AlphaFold och AlphaPulldown jämförde forskarna hur dussintals kända sortilinpartners potentiellt binder dess propellergrotta. De fann ett återkommande mönster: många laster presenterar ett ostrukturerat peptidsegment på ungefär tjugo aminosyror som passar in i samma ficka som tyroglobulins svans, ibland i samma riktning som en känd hjärnpeptid kallad neurotensin, och ibland i motsatt riktning. Trots omvänd orientering delar dessa peptider liknande egenskaper — en sur eller negativt laddad grupp i ena änden, en skrymmande aromatisk rest i den andra, och en flexibel, ofta prolinrik sektion däremellan.
Varför jod betyder mindre än form
Eftersom den centrala kontakten mellan sortilin och tyroglobulin är denna flexibla svans testade författarna om jodering av en tyrosin i svansen som bildar hormon skulle förändra bindningen. Det gjorde den inte: en syntetisk peptid som bar ett fullbildat sköldkörtelhormon uppträdde nästan identiskt med den omodifierade versionen. Modellering visade att den jodinerade ringen sticker ut i lösningen utan att skapa nya täta kontakter. Tillsammans med upptagsexperimenten stöder detta en reviderad bild: sortilin ”räknar” inte jodatomer på tyroglobulin. Istället märker det om proteinet har luckrats upp eller delvis degraderats så att dess monomeriska form och svans exponeras på ett sätt som passar.
Vad detta betyder för sköldkörtelhälsan
För en icke-specialist är huvudbudskapet att frisättning av sköldkörtelhormon styrs mindre av en inbyggd jodsensor och mer av en mekanisk kontroll av proteinets form och flexibilitet. Sortilin fungerar som en scanner vid cellytan, letande efter tyroglobulinmolekyler som har lossats eller trimmas till monomerer, för att sedan dra in dem för slutlig hormonfrisättning och jodåtervinning. Detta arbete klargör ett viktigt steg i sköldkörtelhormonbiologin och antyder att läkemedel som är utformade för att blockera sortilin — nu under utredning för andra sjukdomar — oavsiktligt kan förändra hanteringen av sköldkörtelhormon genom att störa detta igenkänningsteg.
Citering: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
Nyckelord: sköldkörtelhormon, tyroglobulin, sortilin, proteintrafik, endocytos