Clear Sky Science · sv
Bridge-helixen hos Cas12a är en allosterisk regulator av R-loopbildning och RuvC-aktivering
Varför detta är viktigt för genredigering
Många kraftfulla verktyg för genredigering, inklusive de som ligger bakom nya terapier och snabba diagnostiska tester, förlitar sig på CRISPR-proteiner som klipper DNA på valda platser. Om dessa molekylära saxar däremot klipper fel kan de orsaka skadliga bieffekter. Denna studie dissekerar en liten rörlig del inne i Cas12a-redigeraren, kallad bridge-helixen, och visar hur dess formförändringar fungerar som en intern säkerhetsbrytare som kopplar korrekt måligenkänning till DNAskärning. Att förstå denna brytare ger en vägkarta för att konstruera CRISPR-verktyg som är både precisa och säkrare för medicinska och bioteknologiska tillämpningar.
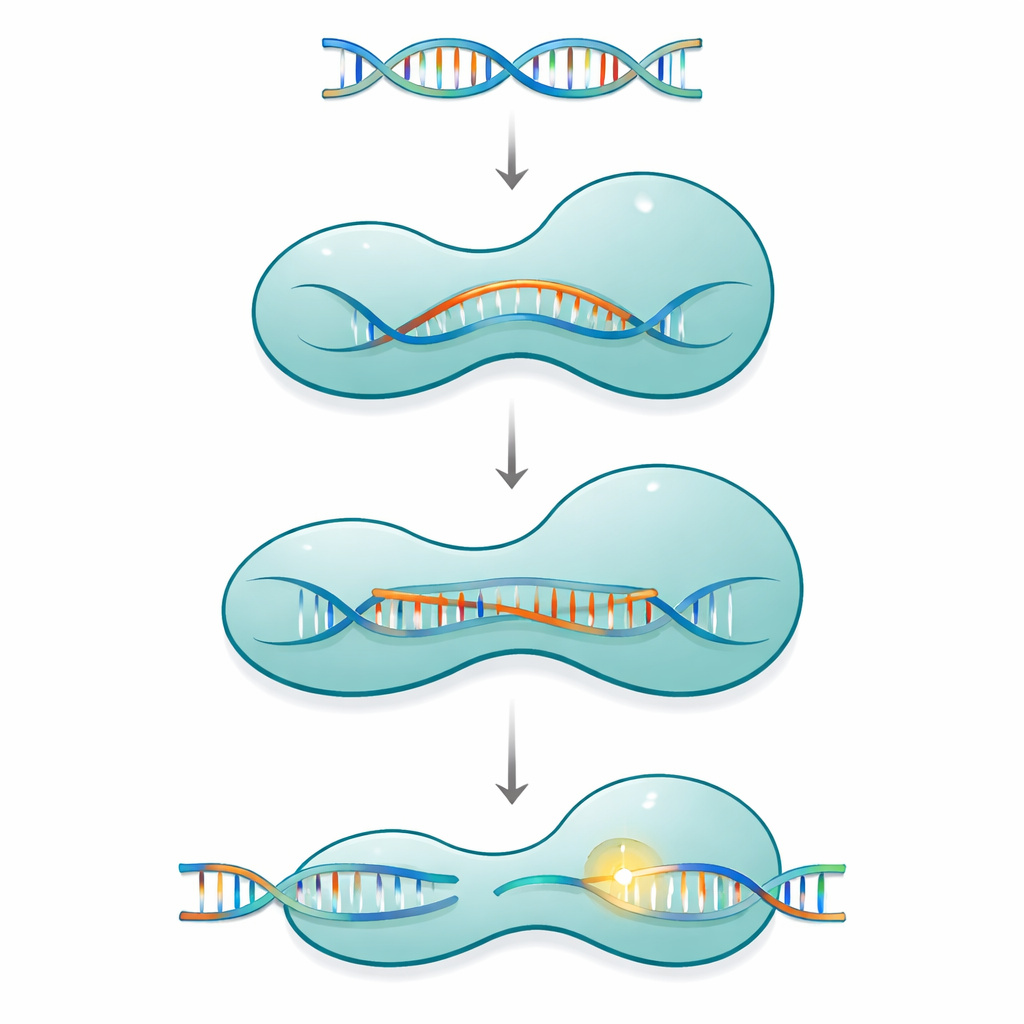
En molekylär klämma med rörliga delar
Cas12a tillhör en familj av enkla proteinbaserade CRISPR-system som använder ett kort guide-RNA för att hitta och klippa matchande DNA i virus eller i en cells genom. Proteinet är format som en tvåarmad klämma: en igenkänningssida som kontrollerar sekvensen, och en klyvsida som rymmer den kemiska maskineriet. Dessa två halvor är förbundna av ett smalt, positivt laddat segment kallat bridge-helix. När Cas12a binder sitt guide-RNA och därefter sitt DNA-mål, beter sig proteinet inte som ett stelt verktyg. Istället rör det sig genom en serie stora och små formförändringar som gradvis sluter sig runt en växande RNA–DNA-hybridstruktur känd som en R-loop, och klyvplatsen aktiveras först fullt ut när en tillräckligt lång sträcka av korrekt basparning har bildats.
Undersöka den inbyggda säkerhetsbrytaren
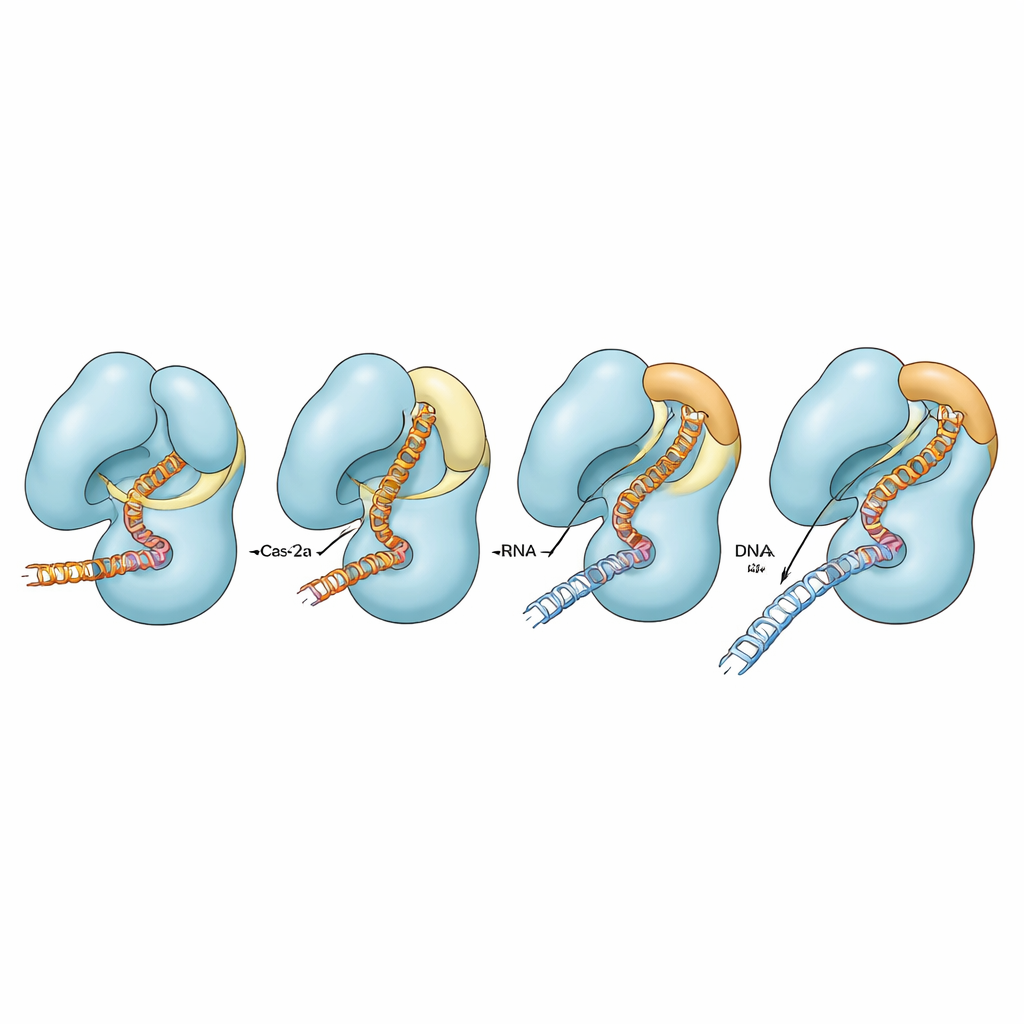
Forskarna fokuserade på en Cas12a från bakterien Francisella novicida och en tidigare konstruerad variant där två aminosyror i bridge-helixen ersatts med prolin, en förändring som är känd för att styva eller bryta helicer. Denna variant, kallad FnoCas12aKD2P, klipper DNA mer selektivt men långsammare än det naturliga proteinet. Med hjälp av kryo-elektronmikroskopi fångade de fem distinkta strukturella ögonblicksbilder av denna variant bunden till sitt guide-RNA och ett stycke mål-DNA. Dessa bilder visar proteinet i olika steg längs dess aktiveringsväg, från tidig initial DNA-igenkänning till senare tillstånd där en del av RNA–DNA-hybriden har bildats men full klyvberedskap ännu inte uppnåtts.
Hur formförändringar driver korrekt skärning
Jämförelser mellan varianten och tidigare bestämda strukturer av normal Cas12a avslöjade ett tydligt mönster. I det naturliga proteinet omvandlas ett segment av bridge-helixen från en lös slinga till en längre, rak helix som böjs mot den växande RNA–DNA-hybriden och kommer i nära kontakt med den. Samtidigt lossnar en intilliggande helix i klyvdomenänen, och en liten region kallad ”locket”, som normalt blockerar den aktiva ytan, växlar från slinga till helix och svänger upp. Tillsammans öppnar dessa koordinerade rörelser ett fack som tillåter en enkel DNA-sträng att gå in och bli klippt. I prolininnehållande varianten kan bridge-helixen inte fullfölja denna slinga-till-helix-övergång eller böja sig ordentligt. Som ett resultat förblir RNA–DNA-hybriden förvrängd och längre bort, locket förblir i ett slutet, slingliknande tillstånd, och komplexet når sällan en fullt pre-katalytisk konformation. Denna mekaniska flaskhals bromsar skärningen av korrekta mål och gör det svårare för mismatchat DNA att smita igenom de interna kontrollpunkterna.
Finjustera specificiteten genom att justera kontakter
För att pröva hur olika kontakter kring locket och bridge-helixen bidrar till aktiviteten ändrade författarna specifika laddade rester som förbinder dessa regioner. I normal Cas12a hade brutna kontakter endast måttliga effekter på att klyva perfekt matchande DNA, även om vissa villkor påverkade hur effektivt den andra DNA-strängen klövs när mismatch fanns. I den försvagade bridge-helixbakgrunden minskade däremot samma byten kraftigt eller nästan helt ut skärningen av båda strängarna, särskilt när guide och DNA inte matchade perfekt. Datorsimuleringar stödde dessa fynd och visade att endast när bridge-helixen kan anta sin fulla heliska form rör sig bron, den intilliggande helixen, locket och nukleinsyrorna i en starkt koordinerad rörelse. När helixen är skadad blir dessa rörelser delvis eller helt okopplade och enzymet har svårt att slutföra sin katalytiska cykel.
En konstruktionsguide för nästa generations CRISPR-verktyg
Sammanfattningsvis visar arbetet att bridge-helixen fungerar som en intern kontrollspak som knyter längd och kvalitet på RNA–DNA-hybriden till öppnandet av klyvfacket i Cas12a. Genom att tvinga proteinet att genomgå en specifik sekvens av formförändringar innan DNA klipps, upprätthåller denna mekanism naturligt diskriminering mot mismatch. Resultaten hjälper till att förklara varför riktade förändringar i denna lilla region kan ge Cas12a-varianter med minskat off-target-klipp och dämpad ”kollateral” DNA-aktivitet — egenskaper som är önskvärda för säkrare genomredigering och diagnostik. Mer generellt belyser studien hur subtila skift i korta helicer kan samordna långväga kommunikation i stora molekylmaskiner och ger allmänna principer för att konstruera högfidelitets nukleinsyra‑hanterande enzymer.
Citering: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
Nyckelord: CRISPR-Cas12a, noggrannhet vid genredigering, bridge-helix, R-loopbildning, allosterisk reglering