Clear Sky Science · sv
RoboA förstärker planariers stamcellsöde via FoxA och Anosmin1a
Hur maskar återbildar sina organ
Vissa plattmaskar kan återskapa nästan vilken saknad kroppsdel som helst, från deras matningsrör till hjärnan. Denna anmärkningsvärda förmåga bygger på adulta stamceller som kan bli många olika celltyper på begäran. Men med så mycket frihet, hur undviker dessa celler att bygga fel vävnad på fel plats — till exempel att göra magsäcksceller i huvudet istället för neuroner? Denna studie använder planariemattan för att utröna hur en liten uppsättning signaler håller högflexibla stamceller på rätt spår under regeneration.
Den regenererande masken och dess dolda potential
Planariearten Schmidtea mediterranea är en populär modell för att studera regeneration eftersom en stor population stamceller är spridd över hela kroppen. Ett nyckelorgan är svalget (pharynx), ett muskulärt matningsrör som sitter i mitten av masken och öppnar mot utsidan när djuret äter. Tidigare arbete visade att en gen kallad foxA är avgörande för att återskapa detta svalget efter skada, och att endast vissa stamceller nära svalget normalt aktiverar foxA. Den nya studien ställer en till synes enkel fråga: vad hindrar stamceller i andra regioner — särskilt i huvud och hjärna — från att också välja en svalgidentitet?
När vägledning saknas
Forskarna fokuserade på ett receptorprotein kallat RoboA, som finns i låga nivåer i många celttyper, inklusive stamceller. När de minskade RoboA-aktivitet med RNA-interferens växte djuren ofta extra, felplacerade svalgen efter att de blivit avkapade. Närmare granskning visade något mer subtilt: även i oskadade maskar orsakade sänkt RoboA att svalgliknande neuroner och muskler dök upp i hjärnregionen. Dessa ”ektopiska svalgneuroner” uppträdde som normala svalgceller vad gäller genuttryck, men var nu på fel plats. Viktigt är att kroppens övergripande plan och hjärnans arkitektur till största delen förblev intakta, vilket tyder på att RoboA inte omformade hela djuret utan i stället finslipade vad närliggande stamceller blev.
En trepartsventil för cellöde
För att förstå hur RoboA fungerar sökte teamet efter partners utanför cellen. Även om Robo-proteiner mest är kända för att binda en ligand kallad Slit, reproducerade inte Slit-nedslagning de felplacerade svalgcellerna. En stor RNAi-skärm av sekretoriska och membranbundna proteiner pekade istället ut Anosmin1a (Anos1a), ett sekretoriskt protein besläktat med en mänsklig faktor involverad i Kallmanns syndrom. Minskning av Anos1a gav liknande extra svalgneuroner, och kombinerade RoboA–Anos1a-nedslagningar uppträdde som om de verkade i samma bana. Samtidigt visade molekylär profilering att transkriptionsfaktorn FoxA sitter i beslutets mitt: när RoboA är närvarande håller det FoxA avstängt i huvudets stamceller; när RoboA-signalering tas bort slår FoxA på och dessa samma stamceller kan välja en svalgneuronsidentitet även medan de sitter i hjärnan.
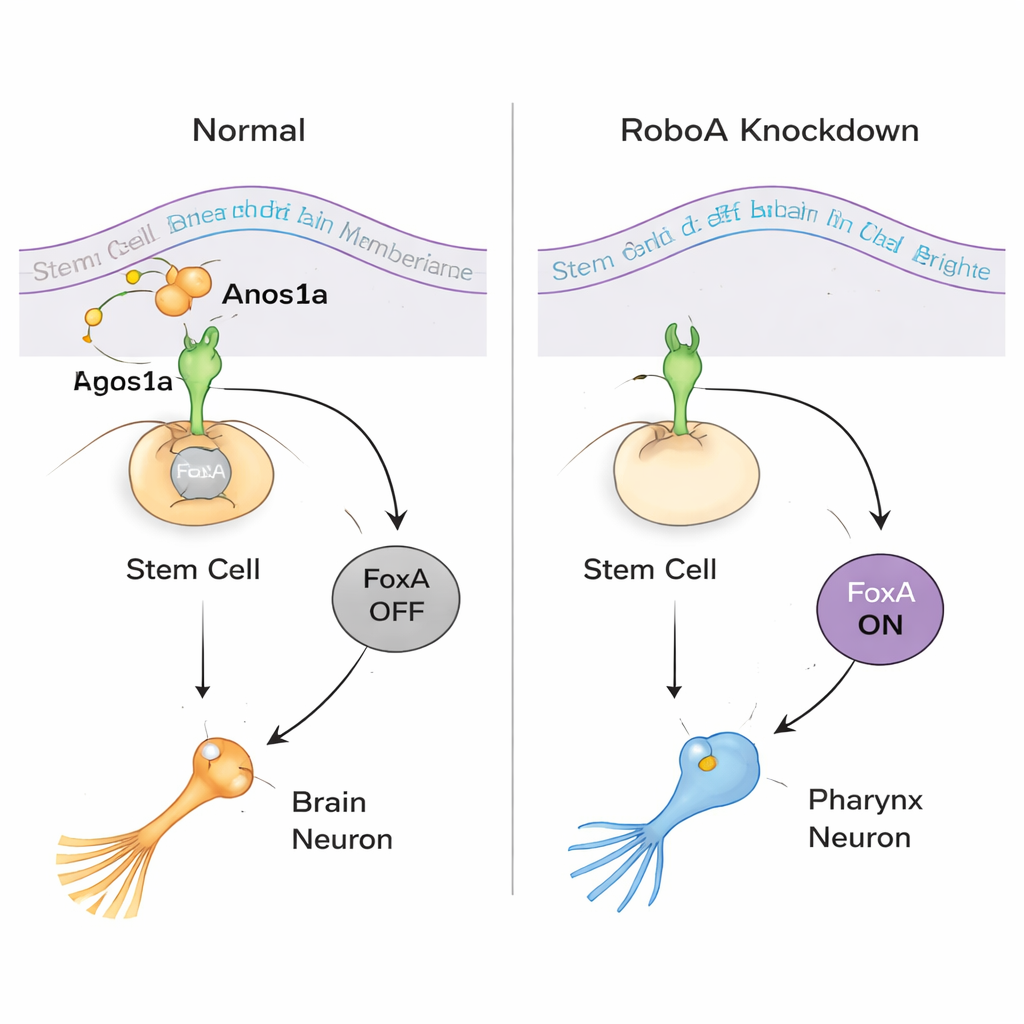
Att avslöja ett tvåvägsval i stamceller
Teamet frågade sedan om denna flexibilitet går åt båda håll. I normala djur förlitar sig stamceller runt svalget på FoxA för att bli svalgneuroner och epitelceller, medan svalgmuskler följer en annan bana. När FoxA slogs ner under längre perioder förlorade maskarna sina svalger helt och växte onormala utväxter i mitten av kroppen. Enkeltcells-RNA-sekvensering och marköranalys visade att dessa utväxter innehöll många celltyper som normalt är begränsade till huvudet, inklusive ögceller och hjärnspecifika neuroner. Med andra ord, när FoxA saknas där svalget borde bildas går lokala stamceller som standard mot en hjärnliknande identitet. Denna upptäckt visar att samma stamceller kan tryckas mot antingen ”svalg” eller ”hjärna” beroende på vilka signaler de mottar.
Finjustering av regeneration, inte omritning av kartan
Sammanfogar man all evidens föreslår författarna att planarieregeneration styrs i två lager. Breda ”positionskontroll”-signaler, såsom Wnt och andra mönstringsmolekyler, etablerar den grova kartan för huvud, bål och svans. Ovanpå detta fungerar lokala ”ödesförstärkande” gener som RoboA och Anos1a som säkerhetskontroller som blockerar olämpliga alternativ. I huvudet håller RoboA–Anos1a-signalering FoxA avstängt så att stamcellerna producerar hjärnneuroner i stället för svalgsceller; nära svalget tillåts FoxA att slå på och driva svalgsspecifika öden. Denna lagerindelade kontroll låter planariers stamceller förbli extraordinärt plastiska samtidigt som de ändå återskapar organ på rätt plats, och erbjuder en ritning för hur robust regeneration kan samexistera med strikt anatomisk ordning.
Citering: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
Nyckelord: planarieregeneration, stamcellsplasticitet, organmönstring, RoboA-signalering, FoxA transkriptionsfaktor