Clear Sky Science · sv
NeoPrecis: förbättrad prediktion av immunoterapisvar genom integration av kvalificerad immunogenicitet och klonalitetsmedvetna neoantigenlandskap
Varför vissa cancerformer svarar på immunterapi och andra inte
Immunterapi har förändrat cancerbehandlingen, men många patienter får fortfarande ingen nytta och vissa drabbas av allvarliga biverkningar. En central fråga är varför vissa tumörer upptäcks och förstörs av immunsystemet medan andra smiter förbi. Denna studie presenterar NeoPrecis, en beräkningsmetod som granskar de “flaggor” tumörer visar upp för immunsystemet — kallade neoantigener — och använder den informationen för att bättre förutsäga vilka patienter som sannolikt svarar på moderna immunterapier.
Nya flaggor på cancerceller
Cancerceller samlar på sig DNA‑mutationer som kan förändra de proteiner de producerar. Små fragment av dessa förändrade proteiner, kända som neoantigener, kan visas på cellens yta och uppfattas som främmande av T‑celler, immunsystemets lönnmördare. Under lång tid har läkare och forskare förlitat sig på grova mått såsom tumörmutationsbörda — det totala antalet mutationer — för att uppskatta hur sannolikt det är att en cancer svarar på checkpoint‑hämmare. Men detta är ett trubbigt verktyg: inte varje mutation skapar ett synligt eller attraktivt mål för T‑celler, och tumörer kan vara lapptäcken av många olika cellsubtyper. NeoPrecis är utvecklat för att gå längre än att bara räkna mutationer och i stället bedöma hur många av dem som verkligen utgör lovande mål över hela tumören.
Tittar på tre viktiga ingredienser samtidigt
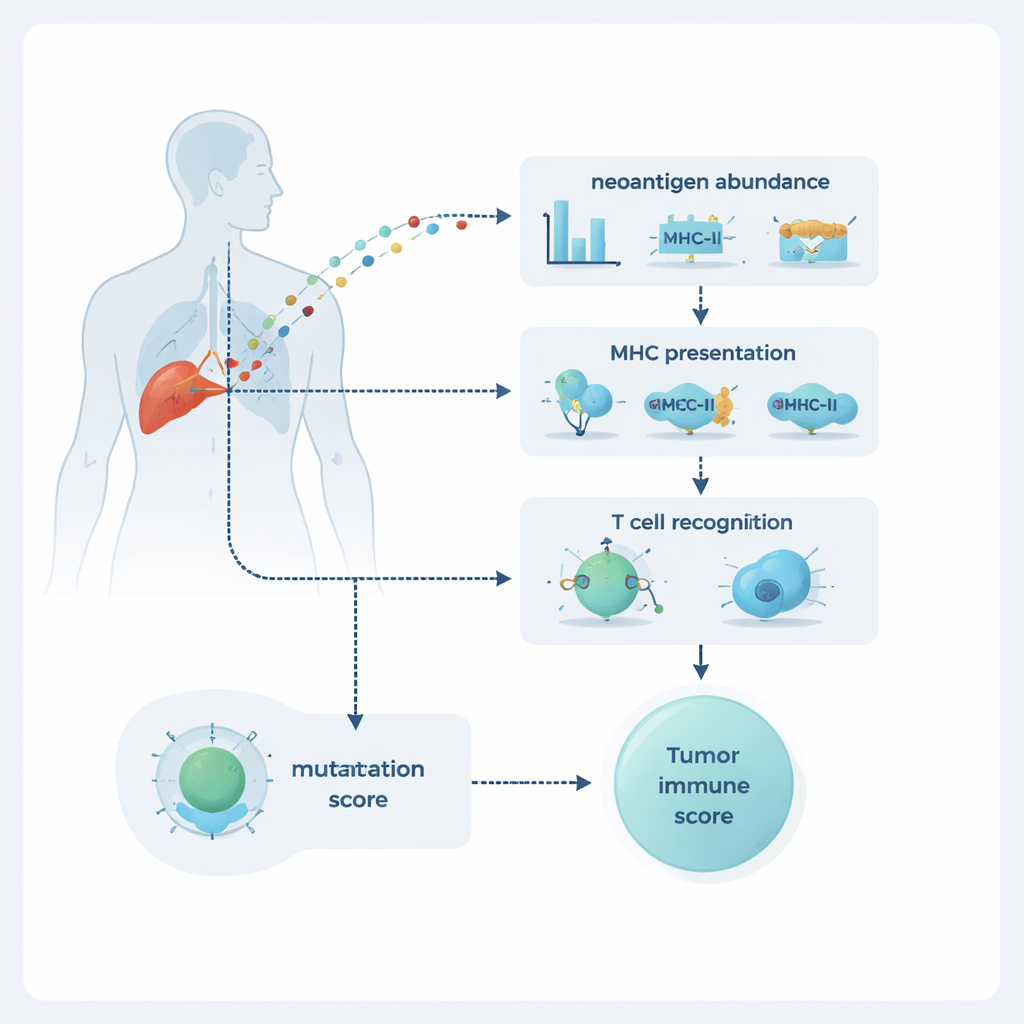
NeoPrecis utvärderar varje mutation längs tre dimensioner: hur riklig den är i tumören, om den sannolikt visas på cellytan, och hur sannolikt den uppmärksammas av T‑celler. Rikligheten uppskattas från DNA‑ och RNA‑sekvensering, vilka visar hur vanligt förekommande mutationen är och hur starkt den uttrycks. Visningen modelleras genom bindning till molekyler som kallas MHC klass I och klass II, som fungerar som anslagstavlor som visar proteinfragment för T‑celler. Den mest nya delen är T‑cellsigenkänningskomponenten, NeoPrecis‑Immuno. Denna modell lär sig från stora databaser med kända T‑cells–peptidinteraktioner för att uppskatta hur olika ett muterat fragment är från dess normala motsvarighet på ett sätt som spelar roll för T‑cellsigenkänning, samtidigt som den tar hänsyn till vilka specifika MHC‑varianter varje person bär.
Lära en dator vad T‑celler “ser”
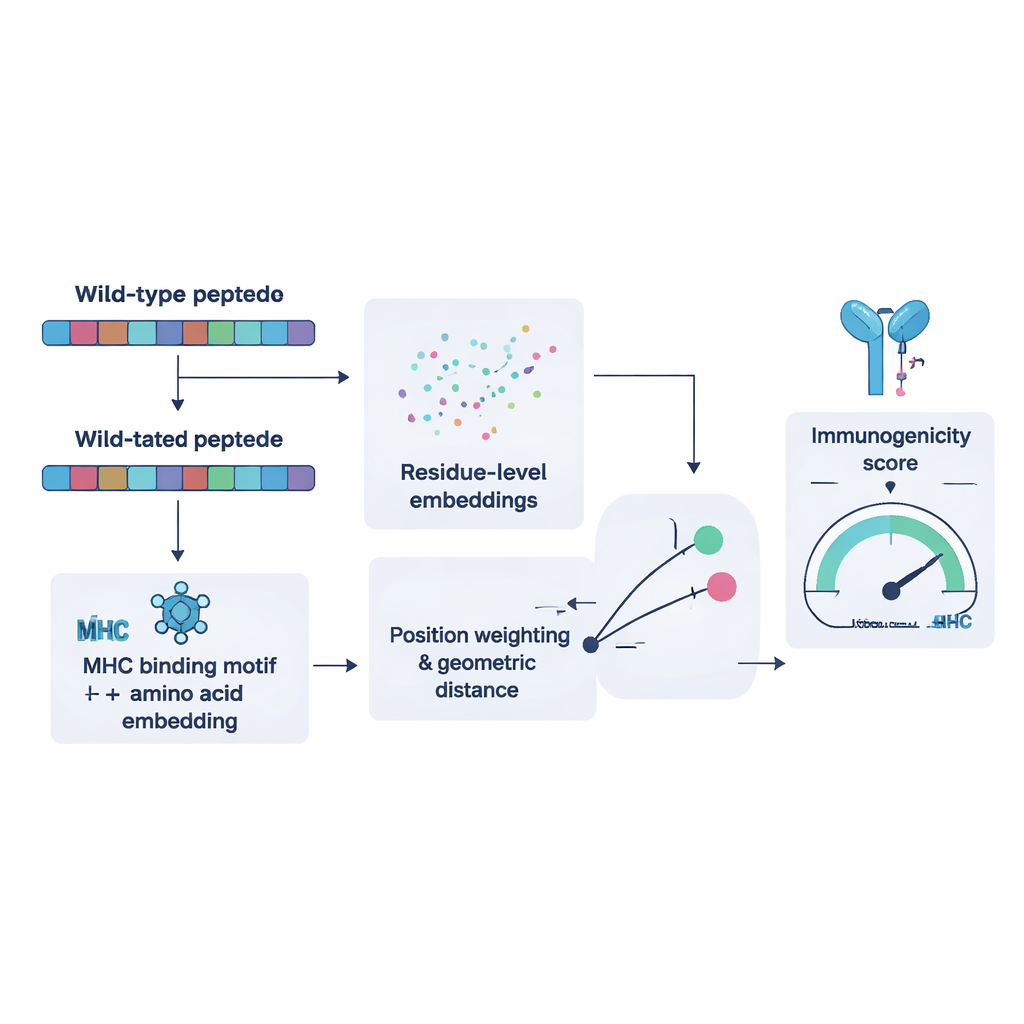
För att träna NeoPrecis‑Immuno samlade forskarna först tusentals exempel där samma T‑cell känner igen flera liknande peptider och andra den inte känner igen. De använde dessa för att lära modellen att mutanta fragment som liknar de normala i hög grad är mindre benägna att utlösa en immunattack, eftersom sådana självliknande mål vanligtvis filtreras bort under T‑cellsutvecklingen. Modellen representerar varje peptid som en punkt i ett matematisk rum format av både dess aminosyrasekvens och bindningspreferenserna hos en persons MHC‑molekyler. Den mäter sedan hur långt det muterade peptidet ligger från originalet. Större, motivinformella avstånd motsvarar högre sannolikhet att vara immunogent. När den testades mot befintliga verktyg på oberoende cancer‑dataset matchade eller överträffade NeoPrecis‑Immuno dem, särskilt vid arbete med MHC klass II, som presenterar för hjälpar‑T‑celler som stödjer och upprätthåller antitumörsvar.
Från enskilda mutationer till hela tumören
Enskilda mutationer är bara en del av berättelsen; hur de är fördelade inom tumören spelar också roll. Vissa mutationer är “klonala”, funna i nästan varje cancercell, medan andra är “subklonala”, förekommande endast i vissa nischer. NeoPrecis bygger ett “neoantigenlandskap” genom att summera sina immunogenicitetspoäng över mutationerna och lägga in information om vilka subkloner de tillhör och hur vanliga dessa subkloner är. Det ger tumörnivåpoäng som lyfter fram cancerformer rika på starka, vida delade neoantigener — särskilt de som kan presenteras på både MHC klass I och klass II och potentiellt utlösa koordinerade hjälpar‑ och mördande T‑cellsresponser. I patientgrupper med melanom och icke‑småcellig lungcancer behandlade med checkpoint‑hämmare separerade dessa NeoPrecis‑baserade poäng mer exakt respondrarna från icke‑respondrarna än standardmutationsräkningar, och var särskilt användbara i komplexa, heterogena lungtumörer.
Vad detta betyder för patienter
För patienter innebär NeoPrecis löftet om mer precis matchning av immunterapier till dem som mest sannolikt drar nytta, och en tydligare förståelse för varför vissa tumörer är motståndskraftiga mot behandling. Genom att fokusera på kvaliteten och fördelningen av neoantigener — inte bara deras kvantitet — hjälper ramen att förklara varför tumörer med liknande mutationsbörda kan bete sig mycket olika. I framtiden kan sådana detaljerade kartor över en tumörs immun‑synliga landskap vägleda inte bara användningen av checkpoint‑hämmare, utan även designen av personligt anpassade cancervacciner som prioriterar de mest potenta och brett delade målen inom varje persons cancer.
Citering: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
Nyckelord: cancerimmunoterapi, neoantigener, tumörheterogenitet, checkpoint‑hämmare, beräkningsonkologi