Clear Sky Science · sv
NR6A1 är avgörande för specificering, bildning och överlevnad av neurala crestceller
Hur tidiga cellval formar ansikte och kropp
Innan vi föds vandrar en särskild grupp celler, kallade neurala crestceller, genom embryot för att bygga upp ansikte, hjärta, nerver och mer. När dessa celler fungerar fel kan barn födas med allvarliga missbildningar. Denna studie avslöjar en tidigare underskattad molekylär brytare, ett protein kallat NR6A1, som hjälper till att bestämma när och var neurala crestceller bildas i däggdjursembryon, och vad som händer när den brytaren fallerar.
Embryots vandrande byggare
Neurala crestceller uppstår mycket tidigt i utvecklingen längs gränsen mellan det blivande hjärnan och ryggmärgen. Efter att ha lossnat från denna vävnad migrerar de långa sträckor för att skapa många olika strukturer — från ansiktets ben och brosk till delar av det perifera nervsystemet och pigmentceller i huden. Eftersom de bidrar till så många organ kan även små störningar i deras bildning orsaka vitt spridda tillstånd kallade neurocristopatier, inklusive kraniofaciala syndrom som Treacher Collins. Att förstå hur dessa celler först uppkommer är därför centralt för att förklara både normal utveckling och medfödda fel.
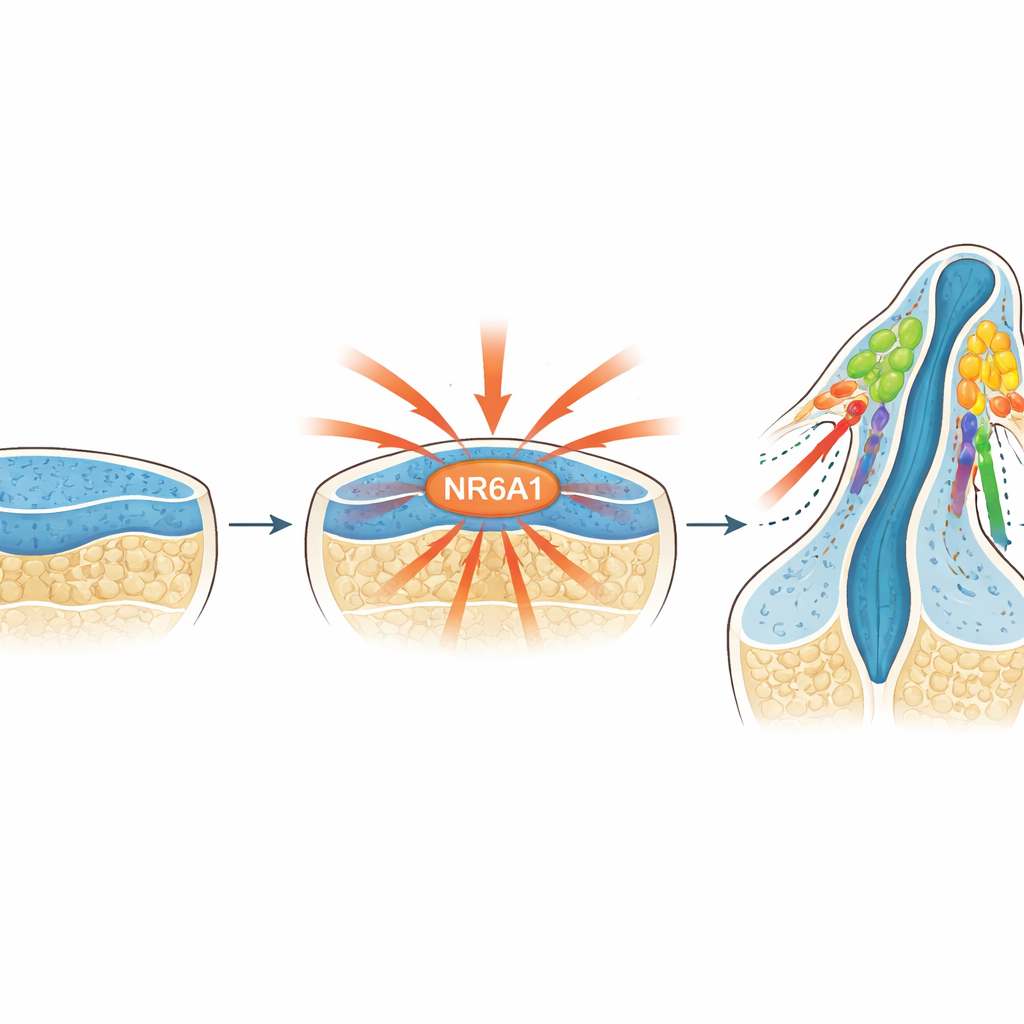
En nyupptäckt huvudbrytare
Forskarna fokuserade på NR6A1, medlem i nuclear receptor-familjen av proteiner som styr genaktivitet. Tidigare arbete antydde att NR6A1 kan vara involverat i huvud- och ansiktsdefekter, men dess roll i neurala crestceller var okänd. Genom att följa NR6A1 i musembryon från strax efter implantationen fann teamet att dess närvaro överensstämde noggrant med var och när neurala crestceller normalt föds: det uppträder i den tidiga neurala vävnaden, koncentreras längs den dorsala (bakre) sidan av den utvecklande hjärnan och ryggmärgen, och ses också i celler precis när de lämnar denna vävnad för att börja migrera.
Vad som händer när brytaren saknas
Möss som helt saknar NR6A1 dör tidigt i utvecklingen, så teamet undersökte embryon strax före denna tidpunkt. De observerade en kraftig brist på neurala crestceller, särskilt bakom den första bågen som ska bilda delar av käken och nacken, där migrerande neurala crestceller nästan helt saknades. Viktiga genprogram som normalt markerar neurala crestidentitet och möjliggör att celler kan lossna och röra sig var skarpt reducerade. Samtidigt förblev gener som håller celler i ett stamlikt, starkt proliferativt tillstånd påslagna, och många neurala crest-liknande celler som ändå bildades dog snart. Dessa fynd visar att utan NR6A1 misslyckas neurala stamceller med att övergå korrekt till migrerande neurala crestceller och inte kan överleva.
Stänga av stamhet och slå på rörelse
För att förstå hur NR6A1 utövar denna kontroll kombinerade författarna flera kraftfulla molekylära tekniker, inklusive enkelcells-RNA-sekvensering, kartläggning av kromatinåtkomlighet och riktade DNA–protein-bindningsanalyser i både mus- och mänskliga stamcellsderiverade neurala crestceller. De fann att NR6A1 fysiskt binder till specifika DNA-motiv nära gener som styr två motsatta program: ett som upprätthåller pluripotens (förmågan att bli många celltyper) och ett annat som driver neurala crestidentitet och cellrörelse. När NR6A1 är närvarande blir kromatinet kring stamhetsgener som Oct4 och Nanog mindre åtkomligt och dessa gener dämpas, medan regioner nära gener för neural crest och epitel-till-mesenkymövergång blir mer öppna och aktiva. Överuttryck av Oct4 under det kritiska fönstret för neurala crestbildning efterliknade förlusten av NR6A1, vilket ytterligare visar att stamhet måste tystas för att neurala crestceller ska kunna uppkomma.
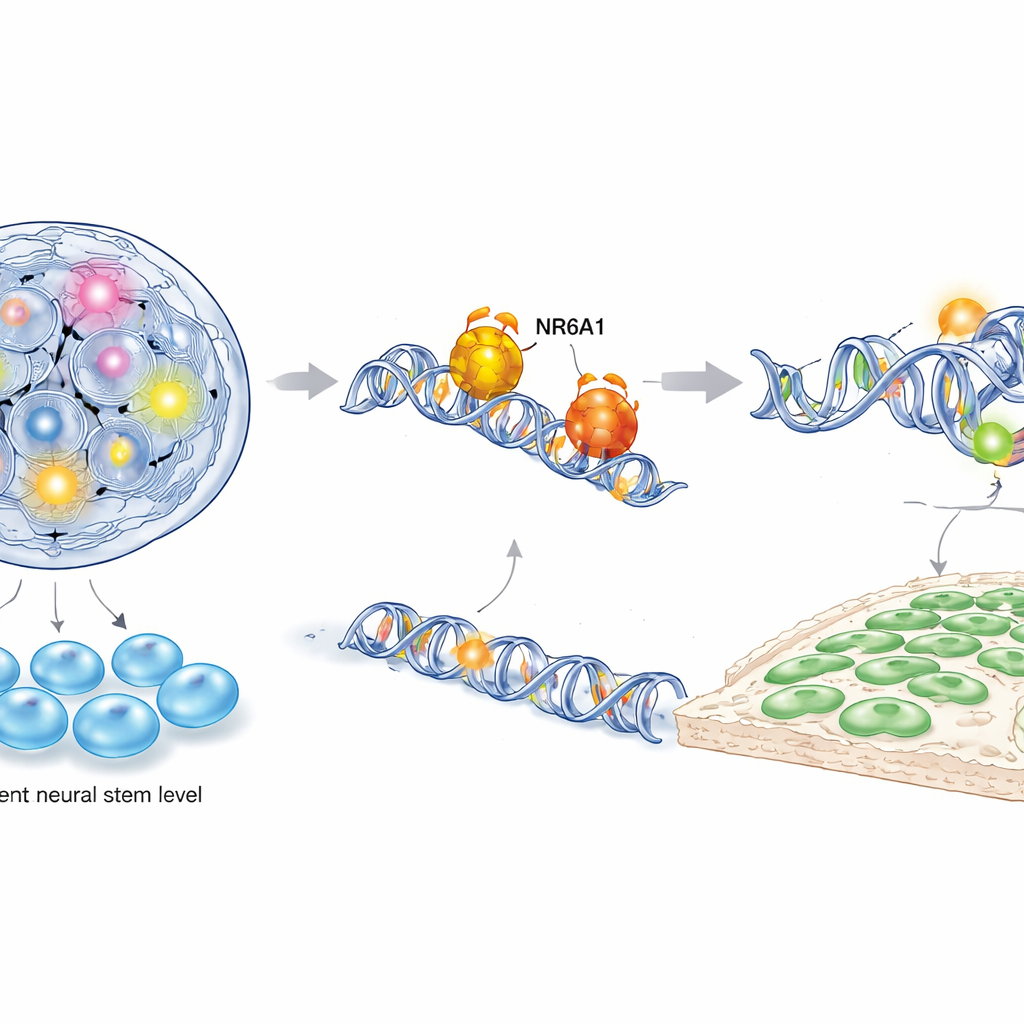
Omskriver tidtabellen för tidig utveckling
Studien reviderar också kalendern för när neurala crestceller börjar specificeras hos däggdjur. Genom att använda ett inducerbart genetiskt system för att ta bort NR6A1 vid olika tidpunkter visade teamet att radering av det vid mitten av gastrulation — ett stadium tidigare än man traditionellt trott — var tillräckligt för att blockera aktiveringen av neurala crestgener. I kontrast gav senare borttagning av NR6A1, även med en allmänt använd neural crest-specifik drivlinje, inga uppenbara defekter. Det betyder att viktiga beslut om neurala crestfate fattas innan dessa standardverktyg ens börjar verka, vilket förklarar varför några tidigare musstudier kan ha missat tidiga krav.
Varför detta spelar roll för medfödda fel och sjukdom
Sammantaget visar arbetet att NR6A1 är en central koordinator som hjälper neurala stamceller att «växa upp» till neurala crestceller genom att samtidigt stänga av pluripotensprogram och möjliggöra program för migration och överlevnad. Denna dubbla handling tycks börja under mitten av gastrulation, tidigare än tidigare erkänt hos däggdjur, och för samman musutveckling närmare andra ryggsträngsdjurs utveckling. Genom att klargöra när och hur denna brytare verkar ger studien en ram för att omtolka tidigare genetiska experiment, identifiera bättre verktyg för att studera neural crest-biologi och i slutändan förstå och potentiellt förebygga neurocristopatier som uppstår när detta tidiga utvecklingsbeslut går fel.
Citering: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
Nyckelord: neurala crestceller, NR6A1, embryonal utveckling, pluripotensväxling, neurocristopati