Clear Sky Science · sv
Ingenjörskonst med MmeFz2-ωRNA-systemet för effektiv genredigering via ett integrerat beräknings–experimentellt ramverk
Mindre gen-saxar för stora medicinska problem
Genredigering har redan förändrat hur forskare studerar sjukdomar, men att omvandla den till säker och praktisk medicin är fortfarande en stor utmaning. Ett stort hinder är att dagens mest kraftfulla DNA‑"saxar", som CRISPR‑Cas9, är fysiskt stora och svåra att packa in i de små leveransfordon som används hos patienter. Den här studien presenterar ett nytt, kompakt genredigeringsverktyg byggt från en relativt okänd enzymfamilj kallad Fanzor2 och visar hur artificiell intelligens snabbt kan omdesigna det till en stark kandidat för framtida genetiska terapier.
En ny klass av kompakta genredigerare
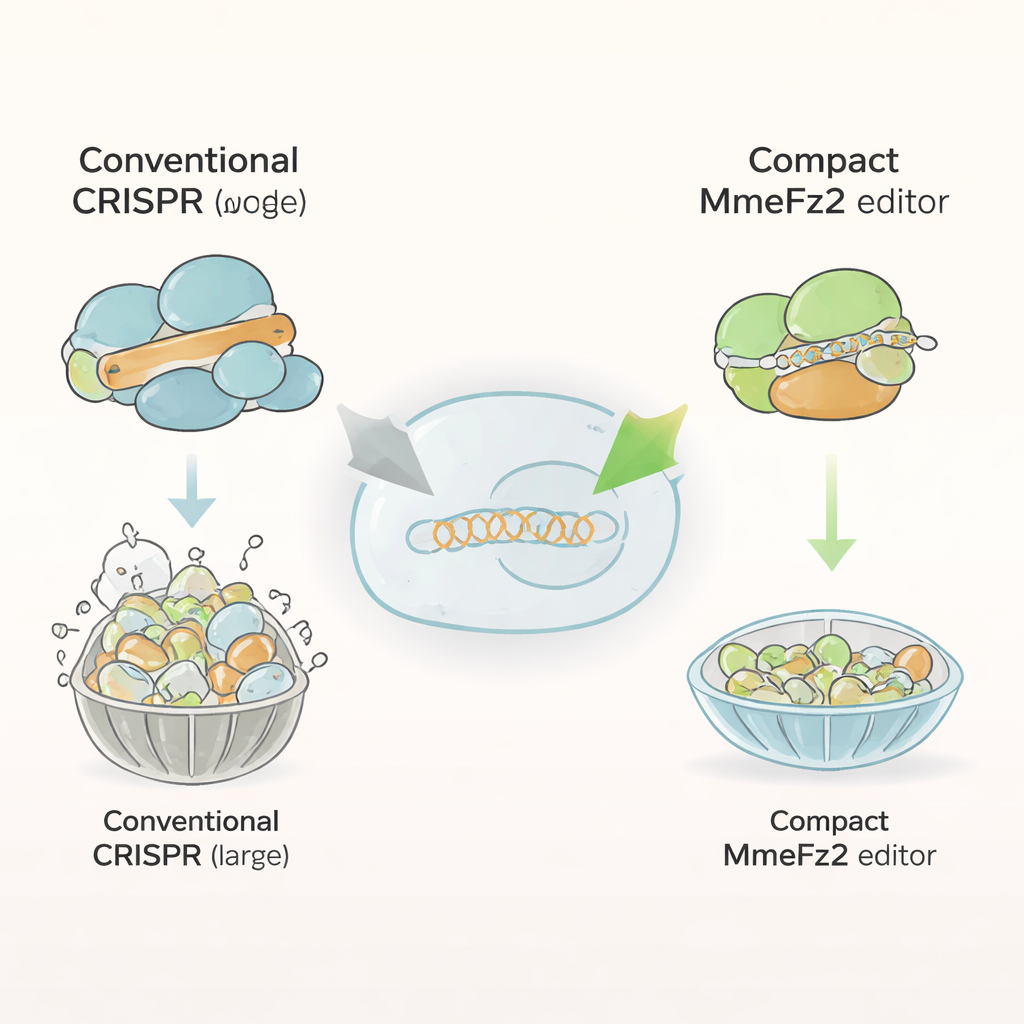
De flesta nutida genredigerare, såsom Cas9 och Cas12a, är klumpiga proteiner sammansatta av mer än tusen byggstenar. Denna storlek gör dem svåra att klämma in i adenoassocierade virus (AAV), den ledande leveransmetoden för genbehandlingar. I kontrast är Fanzor2‑proteiner mycket mindre och förekommer naturligt i eukaryoter, den livsgren som inkluderar djur och människor. Författarna koncentrerade sig på en medlem i denna familj, MmeFz2, som använder en kort RNA‑molekyl kallad ωRNA för att hitta och klippa specifika DNA‑sekvenser. På pappret såg MmeFz2 idealisk ut för terapi: kompakt och programmerbar. I praktiken var dess aktivitet i mänskliga celler dock usel, med redigeringar i mindre än en procent av målen. Teamet gav sig därför i kast med att förvandla detta svaga enzym till ett praktiskt verktyg.
Att använda AI för att omdesigna vägledarmolekylen
Det första målet var ωRNA, vägledaren som talar om för MmeFz2 var den ska klippa. Med AlphaFold3, ett toppmodernt program som förutsäger 3D‑strukturer för protein–RNA–DNA‑komplex, byggde forskarna en modell av MmeFz2 bundet till sin ωRNA och ett DNA‑mål. Denna virtuella struktur visade att delar av ωRNA var sladdriga, dåligt parade och knappt i kontakt med proteinet. Med denna information som vägledning ersatte teamet systematiskt instabila länkar i RNA:t och tog bort sekvenser av uridinbaser som kan störa transkription. De testade därefter dussintals varianter i mänskliga celler. Genom att stapla de bästa förändringarna och korta en onödig stamslinga skapade de en förkortad ωRNA som var 30 % mindre men ändå gav nära 20‑faldig ökning av redigeringseffektiviteten över många DNA‑mål.
Finputsning av proteinet med maskininlärning
Därefter förfinade teamet själva proteinet. De använde återigen AlphaFold3 för att kartlägga var MmeFz2 rörde vid RNA och DNA och designade över hundra enstaka aminosyreförändringar med sikte på att stärka dessa kontakter eller förbättra flexibiliteten. Efter screening av dessa i celler matade de prestationsdata till EVOLVEpro, ett maskininlärningssystem byggt på protein‑språkmodeller tränade på miljoner naturliga sekvenser. Detta verktyg lärde sig vilka egenskaper som tenderade att öka aktivitet och föreslog nya kombinationer av mutationer som förutspåddes fungera ännu bättre. Genom några rundor av denna beräknings–experimentella slinga kom forskarna fram till två optimerade enzymvarianter som, tillsammans med den förbättrade ωRNA, ökade redigeringsaktiviteten mer än 60‑falt jämfört med utgångssystemet.
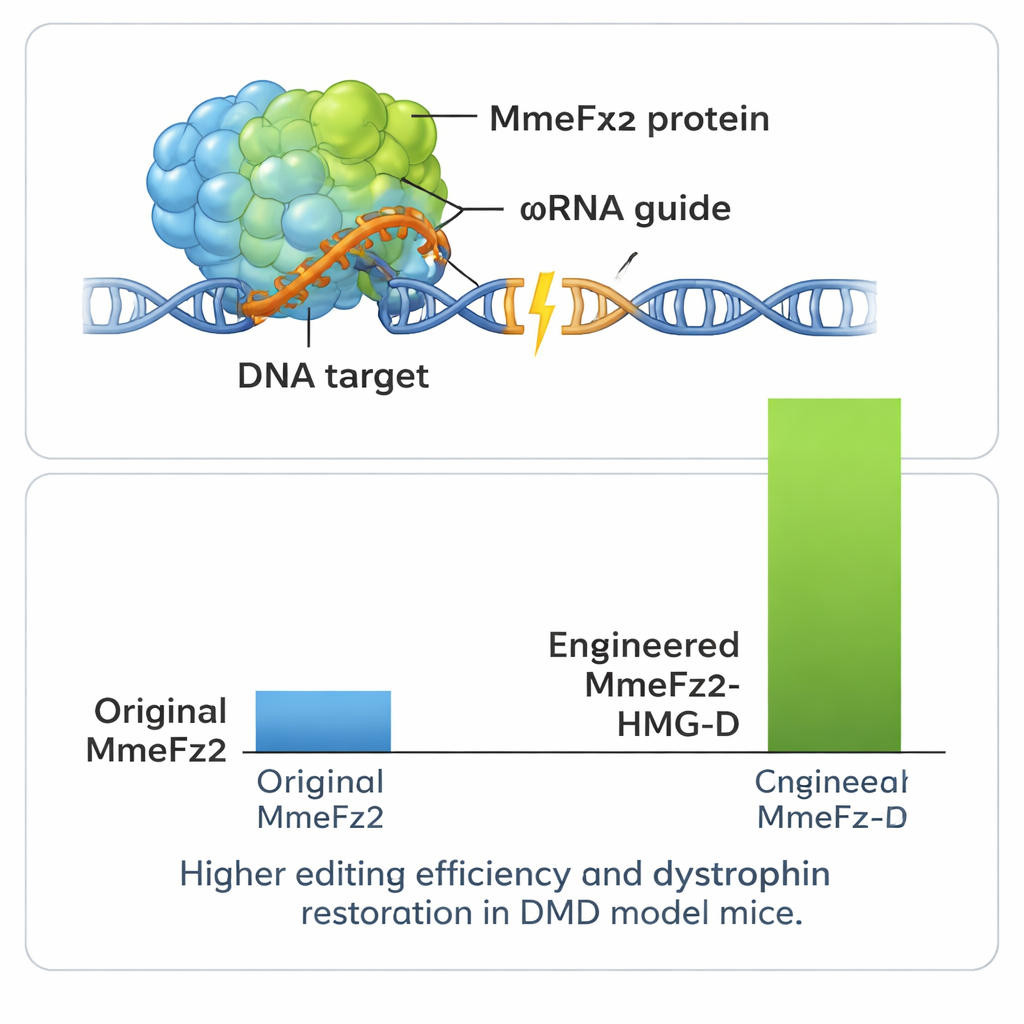
Ökad kraft och test i en sjukdomsmodell
För att pressa ännu mer prestanda ur systemet fäste författarna MmeFz2 vid små DNA‑bindande domäner som hjälper proteiner att fästa vid det genetiska materialet. En av dessa, kallad HMG‑D, visade sig särskilt effektiv när den sattes på änden av det konstruerade enzymet och gav redigeringsnivåer över 80 % vid vissa mål. Viktigt var att tester på förutsagda off‑target‑platser i genomet visade att denna ökade kraft inte innebar en stor förlust i precision. Eftersom hela genredigeraren — inklusive protein och guide‑RNA — är så kompakt, får den lätt plats i en enda AAV‑vektor, något som inte är möjligt för de flesta CRISPR‑system. Teamet utnyttjade denna fördel i en musmodell för Duchennes muskeldystrofi, en dödlig muskelnedbrytande sjukdom orsakad av fel i dystrofingenen. En engångsinjektion av AAV‑levererad redigerare i benmuskulaturen ledde till påvisbara korrigeringar i genens RNA och återställde dystrofinprotein i en betydande andel muskelceller.
Vad detta betyder för framtida gen‑terapier
För icke‑specialister är huvudbudskapet att författarna har förvandlat ett svagt, obskyrt genklippande enzym till en kompakt, högpresterande redigerare som kan levereras i ett enda viruspaket och kan reparera en allvarlig genetisk sjukdom i en realistisk djurmodell. Lika viktigt är hur de nådde dit: genom att tätt kombinera AI‑baserad strukturprognos och maskininlärning med fokuserade laboratorietester förbättrade de både proteinet och dess guide‑RNA långt effektivare än traditionella trial‑and‑error‑metoder. Denna integrerade strategi kan snabba upp skapandet av många nästa generations genredigerare och föra precisa och säkrare genterapier närmare patienter med muskeldystrofi och andra ärftliga tillstånd.
Citering: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
Nyckelord: genredigering, alternativ till CRISPR, Duchennes muskeldystrofi, virusbaserad genleverans, artificiell intelligens i biologi