Clear Sky Science · sv
Bedömning av proteins veckningsstabilitet med explicit hänsyn till veckade tillstånd
Varför proteinstabilitet spelar roll
Varje protein i din kropp är en liten molekylär maskin som måste vika sig till en noggrant bestämd tredimensionell form för att fungera korrekt. Om den vikningen är för skör kan proteinet fungera fel, klumpa ihop sig eller helt undanhållas produktion—problem som kopplats till sjukdomar och till misslyckanden vid framställning av proteinbaserade läkemedel och enzymer. Att mäta hur stabilt ett protein är i labbet är tidskrävande och komplicerat, så forskare söker datorbaserade metoder som pålitligt kan avgöra, utifrån sekvensen ensam, hur lätt ett protein veckas upp.
En ny syn på veckade och oveckade proteiner
De flesta moderna algoritmer fokuserar nästan uteslutande på proteinets veckade form. De börjar ofta från en AI‑predicerad struktur, såsom de från AlphaFold, och behandlar den enda strukturen som den huvudsakliga bestämningsfaktorn för stabilitet. Men stabilitet är egentligen energiskillnaden mellan två breda ensemble: det kompakta veckade tillståndet och de många sladdriga former som utgör det oveckade tillståndet. Författarna menar att att ignorera den oveckade sidan av denna balans är en viktig orsak till att befintliga verktyg har svårt att överensstämma med experimentella mätningar av veckningsfri energi, känd som ΔG.
En ny modell som lär sig båda tillstånden
Forskarna introducerar IFUM, ett djuplärande system utformat för att uppskatta ΔG samtidigt som det lär sig hur balansen mellan veckade och oveckade tillstånd ser ut för varje protein. I stället för att behandla det oveckade tillståndet som en vag bakgrund använder IFUM idéer från polymerfysik för att representera det som en "slumpmässig spole" och kodar både veckade och oveckade tillstånd som kartor över avstånd mellan aminosyrapar. Modellen tar in information från kraftfulla förtränade sekvens‑ och struktur‑nätverk, och predicerar sedan gemensamt den totala stabiliteten och en sannolikhetskarta som beskriver hur stor del av proteinpopulationen som är veckad respektive oveckad för varje residue‑par. Träning på en mycket stor datamängd av små, experimentellt karakteriserade proteiner och kända oordnade proteiner hjälper IFUM att känna igen både välstrukturerade och sladdriga sekvenser.
Bättre siffror och bredare mutationsomfång
När den testas på en noggrant kontrollerad datamängd av små proteiner predicerar IFUM experimentella ΔG‑värden med lägre fel och högre korrelation än tidigare AI‑baserade metoder som endast förlitar sig på den veckade strukturen eller på språkmodeller tränade på sekvenser. Avgörande är att modellen även hanterar en stor variation av sekvensförändringar. Den fångar noggrant effekterna av enkla och dubbla punktmutationer, liksom insertioner och deletioner som ändrar proteinets längd—situationer där många befintliga verktyg antingen misslyckas helt eller aldrig var avsedda att användas. En intern jämförelse visar att borttagning av det oveckade‑tillståndets mål gör prestandan avsevärt sämre, vilket understryker att explicit modellering av det oveckade ensemblen inte bara är ett konceptuellt tillskott utan centralt för förutsägelsens noggrannhet.
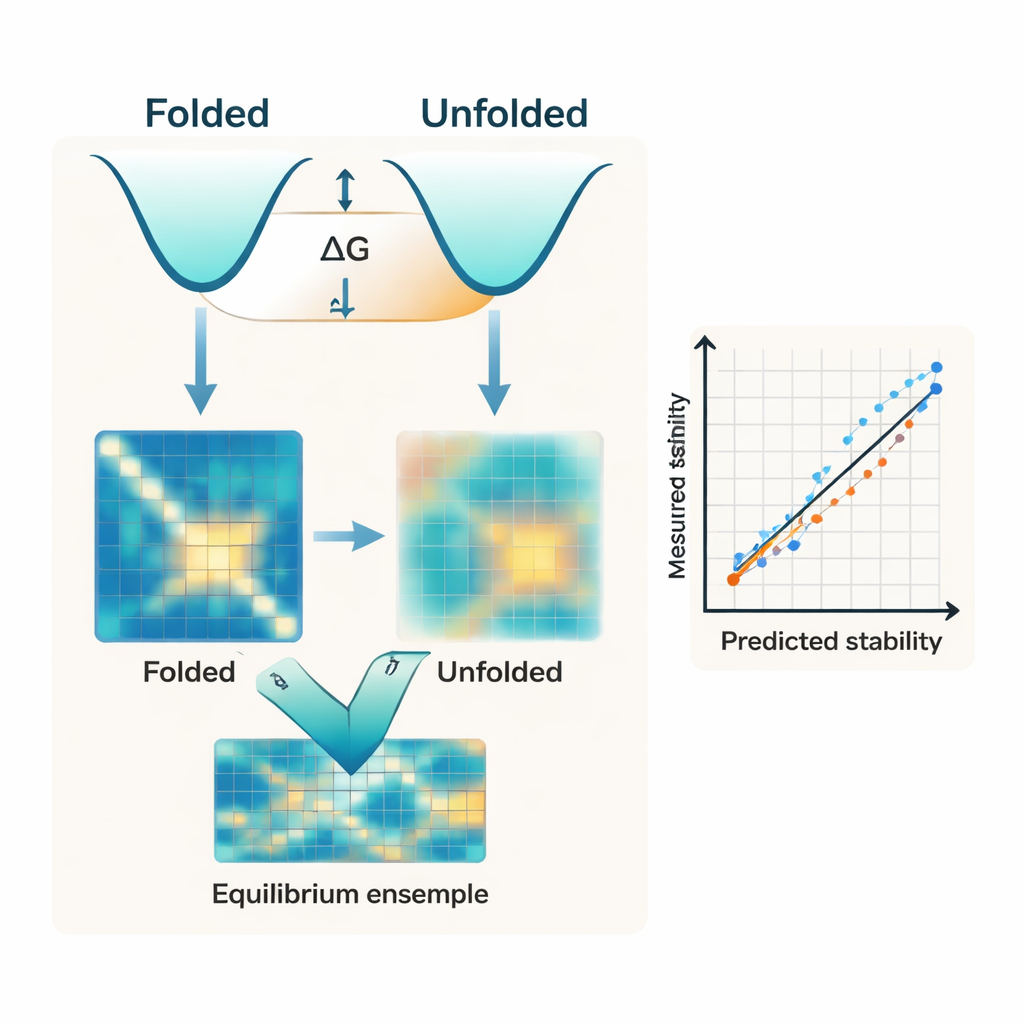
Från designbänk till verkliga tester
För att se om IFUM kan vägleda verklig proteinengineering tillämpar författarna den på tre utmanande designproblem: stabilisering av interferon‑lambda‑proteiner, omformning av immun‑signalproteinet IL‑10 och förbättring av ett sockermodifierande enzym kallat UGT76G1. I alla tre fallen följer IFUMs predicerade stabiliteter väl de uppmätta smälttemperaturerna, vilka rapporterar hur mycket värme ett protein tål innan det veckas upp. Modellen hjälper också till att sålla bland hundratals helt nya, dator‑designade proteiner för att välja dem som mest sannolikt veckas korrekt och förblir lösliga i celler, och överträffar vida använda förtroendescore från strukturprediktionsnätverk. Dessa resultat tyder på att IFUM kan användas som ett praktiskt "stabilitetsfilter" tillsammans med struktur‑baserade kontroller i moderna arbetsflöden för proteindesign.
Begränsningar och framtida riktningar
Liksom alla modeller har IFUM gränser. Den är huvudsakligen tränad på korta, enkelkedjiga, lösliga proteiner, och dess absoluta stabilitetssiffror blir mindre tillförlitliga för mycket större proteiner eller sådana med omfattande flexibla slingor eller membran‑spänningsregioner. Dess beskrivning av det oveckade tillståndet är fortfarande en förenklad statistisk modell snarare än en fullt realistisk bild av alla möjliga former. Ändå visar tillvägagångssättet att lära en AI att överväga både veckade och oveckade ensemblen ger mer pålitliga stabilitetsuppskattningar. För icke‑experter är huvudpoängen att IFUM för oss närmare möjligheten att med kvantitativt förtroende fråga en dator: "Håller denna proteindesign faktiskt ihop?", vilket potentiellt kan snabba upp utvecklingen av säkrare biologiska läkemedel och mer robusta industriella enzymer.
Citering: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
Nyckelord: proteinstabilitet, proteinveckning, djuplärande, proteindesign, mutationer