Clear Sky Science · sv
Metabolisk karaktärisering av tumör‑immuninteraktioner med multiplexad immunofluorescens avslöjar rumsliga mekanismer för immunterapisvar vid icke‑småcellig lungkarcinom (NSCLC)
Varför denna forskning är viktig
Immunterapi har revolutionerat behandlingen för vissa personer med avancerad lungcancer, men de flesta patienter ser fortfarande att deras cancer växer trots dessa kraftfulla läkemedel. Den här studien ställer en enkel men avgörande fråga: kan vi granska cancervävnaden mer i detalj — var olika celler befinner sig och hur mycket energi de använder — för att förutsäga vem som verkligen kommer att dra nytta av immunterapi? Genom att förvandla små biopsiprover till detaljerade kartor på cellnivå ämnar forskarna föra vården av lungcancer närmare ett verkligt personligt angreppssätt.
Att se in i lungtumörer som en stadsplan
Teamet undersökte vävnad från 55 personer med avancerad icke‑småcellig lungkarcinom (NSCLC) som behandlats med hämmande kontrollpunktsbehandlingar, en huvudklass av immunterapier. Före behandling färgades deras tumörprover med en panel om 44 markörer med multiplexad immunofluorescens, vilket möjliggjorde visualisering av många proteiner samtidigt. Ett djupinlärningssystem identifierade därefter nyckelcelltyper — såsom tumörceller, T‑celler, B‑celler, makrofager och fibroblaster — och klassificerade deras funktionella tillstånd (till exempel aktiverade, delande eller utmattade) samt deras metabola profil, det vill säga hur de producerade och använde energi. Istället för att bara räkna celler kartlade forskarna också var cellerna låg i förhållande till varandra och skapade område‑ eller grannskapsliknande regioner inom varje biopsi.
Energihungriga tumörer och deras immuna omgivning
Ett huvudfokus var metabolism — hur celler genererar bränsle för att växa eller bekämpa sjukdom. Forskarna definierade ”metaboliska grannskap” med olika nivåer och typer av energianvändning, från låg aktivitet till mycket aktiva zoner rika på oxidativ fosforylering och glykolys. De fann att både tumörceller och vissa immunceller, som makrofager, ofta uppvisade starka energi‑producerande vägar. Några av dessa mönster kopplades till patientutfall. Till exempel tenderade tumörer med hög aktivitet i vägar som hjälper dem att använda aminosyror och driva TCA‑cykeln att tillhöra patienter som recidiverade tidigt efter immunterapi. Däremot var vissa plasmaceller (antikroppsproducerande B‑celler) med aktiva energivägar i tumören vanligare hos patienter som klarade sig bättre, vilket antyder att inte alla energirika celler är skadliga — vissa kan stödja effektiv anti‑tumörimmunitet.
Goda och onda immunceller i tumörlandskapet
Bortom enkel mängd var även typ och beteende hos immunceller viktiga. Makrofager som bar det cytotoxiska molekylet granzyme B var starkt associerade med sämre progressionsfri överlevnad, särskilt när de återfanns i metaboliskt låga eller inaktiva grannskap. Dessa regioner kan representera näringsfattiga eller vilande områden där immunsvaret dämpas. Däremot verkade vissa arrangemang av regulatoriska T‑celler (Tregs) och fibroblaster vid gränsen mellan tumören och omgivande vävnad kopplade till bättre utfall, vilket möjligen speglar ett mönster där hämmande celler hålls vid kanterna i stället för att infiltrera djupt in i tumören. Kvoter mellan olika immunceller, såsom granulocyter till CD8‑T‑celler, korrelerade också med svar, och understryker att immunbalansen och positioneringen — inte bara totala antal — är viktiga.
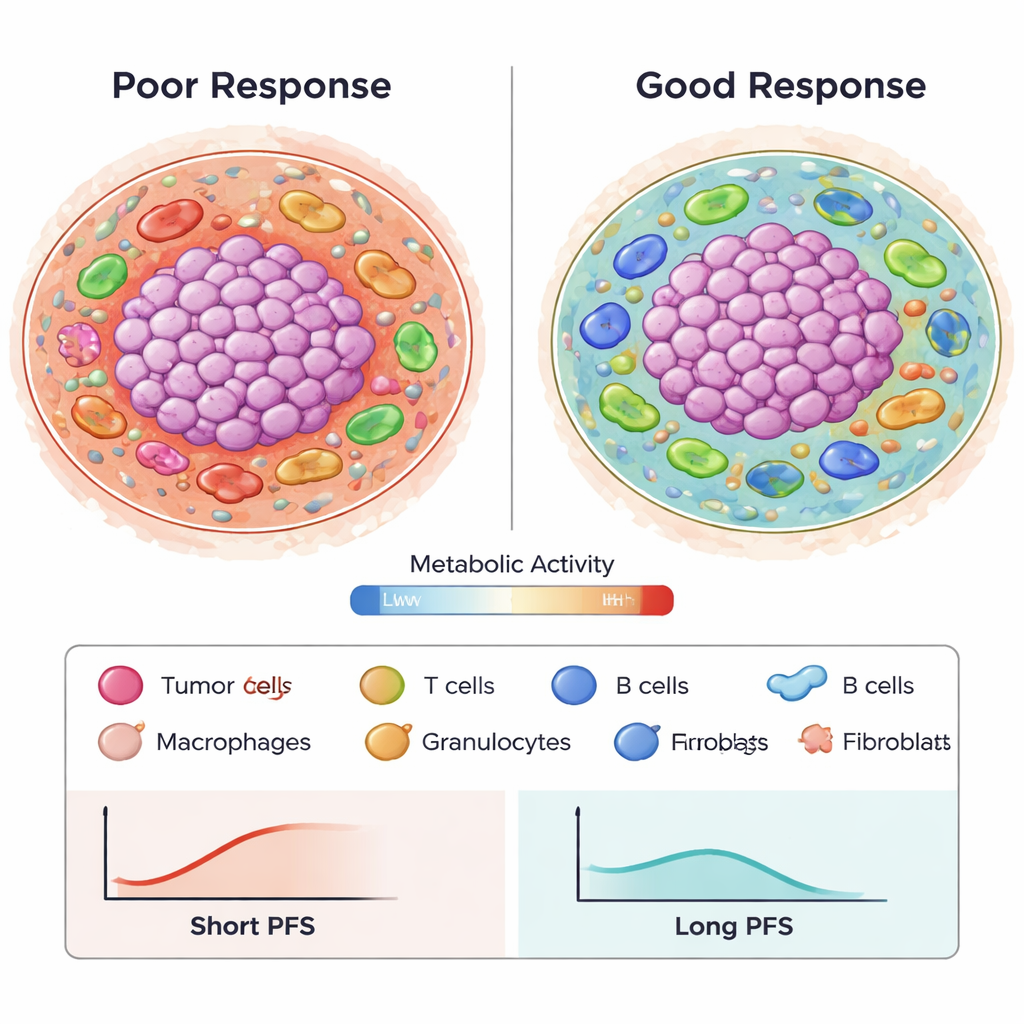
Från komplexa bilder till prediktiva mönster
För att tolka över en miljon konstruerade rumsliga funktioner som beskriver celltyper, avstånd och metabola tillstånd använde författarna en avancerad funktionsselektionmetod (Stabl) och överlevnadsmodelleringsverktyg. De identifierade 87 nyckelfunktioner, många av dem speglande hur metaboliskt aktiva tumörceller interagerar med makrofager och T‑celler, eller hur specifika immuncelltyper klustrar nära blodkärl och fibroblaster. Med dessa funktioner i Cox‑regressionsmodeller byggde de en prediktor som uppskattade progressionsfri överlevnad med en noggrannhet (AUC) runt 0,8 över 24 månader, vilket överträffade traditionella enskilda markörer som PD‑L1‑färgning eller tumörmutationsbörda i tidigare publicerade arbeten. Importantly, flera funktioner var reproducerbara över två oberoende patientkohorter, vilket tyder på att mönstren inte bara är slumpmässigt brus.
Vad detta betyder för patienter
För en lekmannapublik är huvudbudskapet att var celler befinner sig i en lungtumör och hur de försörjer sig med energi kan hjälpa förklara varför vissa patienter svarar bra på immunterapi medan andra inte gör det. Denna studie visar att rik rumslig och metabol information från en rutinbiopsi, kombinerad med artificiell intelligens och statistisk modellering, kan avslöja signaturer för troligen nytta eller resistens. Även om arbetet behöver valideras i större grupper och i helvävnadssektioner, visar det en väg mot framtida tester som skulle kunna säga till läkare, innan behandling påbörjas, vilka patienter som sannolikt får varaktig kontroll från immunterapi och vilka som kan behöva alternativa eller kombinerade strategier.
Citering: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
Nyckelord: immunoterapiresistens, icke‑småcellig lungcancer, tumörmikromiljö, rumslig biologi, cancermetabolism