Clear Sky Science · sv
G9a-medierad H3K9me2 styr regeneration av tarmepitel genom epigenetisk tystning av cellcykelrelaterade gener
Varför tarmens självreparation är viktig
Varje dag utsätts tarmens epitel för hårda påfrestningar: magsyra, matpartiklar och biljoner mikrober. Ändå överlever denna vävnad inte bara, den reparerar sig ständigt. När det reparationssystemet sviktar—efter strålbehandling, vid inflammatorisk tarmsjukdom eller under svåra infektioner—kan människor drabbas av smärta, blödningar och livshotande komplikationer. Denna studie avslöjar en dold ”brytare” inne i tarmceller som hjälper dem att avgöra när de ska sluta vila och börja återbygga, och ger ledtrådar till nya behandlingar som kan stärka tarmens naturliga reparationsstyrka.
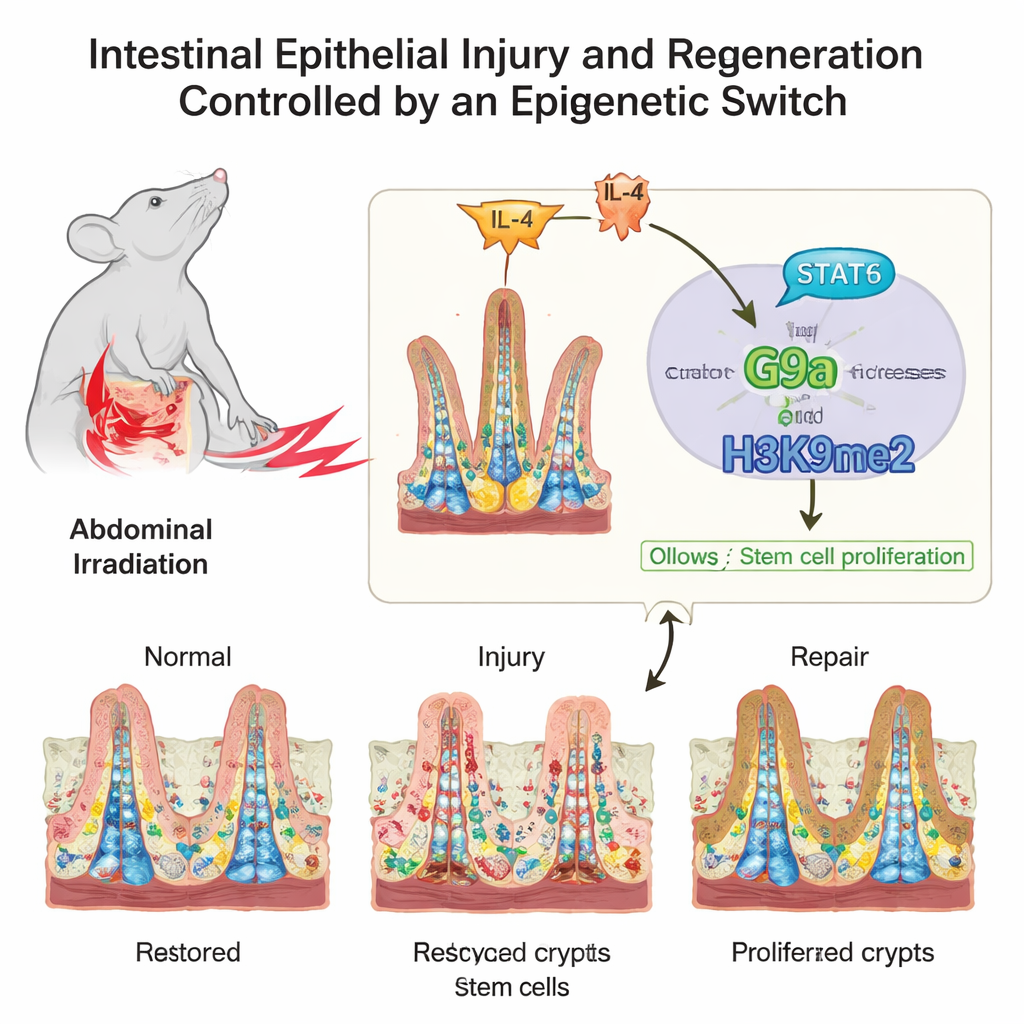
En känslig arkitektur under ständig påfrestning
Tarmens inre yta liknar under mikroskopet en luggmatta, med fingerlika villi som tar upp näring och fickor kallade kryptor där stamcellerna bor. Dessa stamceller och deras snabbdelande dotterceller måste hitta en balans mellan stadig förnyelse och akut reparation. Författarna fokuserade på hur kemiska markörer på DNA‑paketerande proteiner, så kallade histoner, påverkar denna balans. Dessa markörer ändrar inte generna själva, utan fungerar mer som dimmerbrytare som skruvar upp eller ner kluster av gener när tarmen går från normal funktion till skada och tillbaka till hälsa.
En epigenetisk markör som följer skada och läkning
Genom att använda möss som utsattes för strålning—en vanlig orsak till tarmsskada vid cancerbehandling—skannade forskarna många olika histonmarkörer i de stamcellsrika kryptorna. En markör, känd som H3K9me2, steg kraftigt när tarmen gick från skada till reparation. Dess skrivarenzym, ett protein kallat G9a, följde samma mönster. Teamet undersökte sedan mänskliga prover från patienter som fått bäckenstrålning samt från personer med Crohns sjukdom. I båda fallen korrelerade högre nivåer av H3K9me2 och G9a i tarmceller med bättre tecken på vävnadsreparation, vilket tyder på att detta system är bevarat mellan möss och människor.
När reparationsbrytaren är trasig
För att testa om denna markör bara är åskådare eller verkligen driver läkning, tog forskarna bort G9a specifikt från tarmepitelet hos möss eller blockerade dess aktivitet med ett läkemedel. I båda fallen sjönk nivåerna av H3K9me2. Efter strålning eller kemisk skada förlorade dessa möss mer vikt, hade kortare och mer skadade tarmar och visade färre regenererande kryptor och stamceller än normala djur. Även utan avsiktlig skada såg tarmepitelet hos G9a‑defekta möss förkortat ut: kryptorna var grundare, villi var kortare och antalet stamceller samt deras specialiserade avkommor minskade. Små ”mini‑tarmar” odlade från dessa celler i odlingsskålar växte också dåligt, vilket betonar att detta molekylära system är centralt för tarmens dagliga förnyelse.
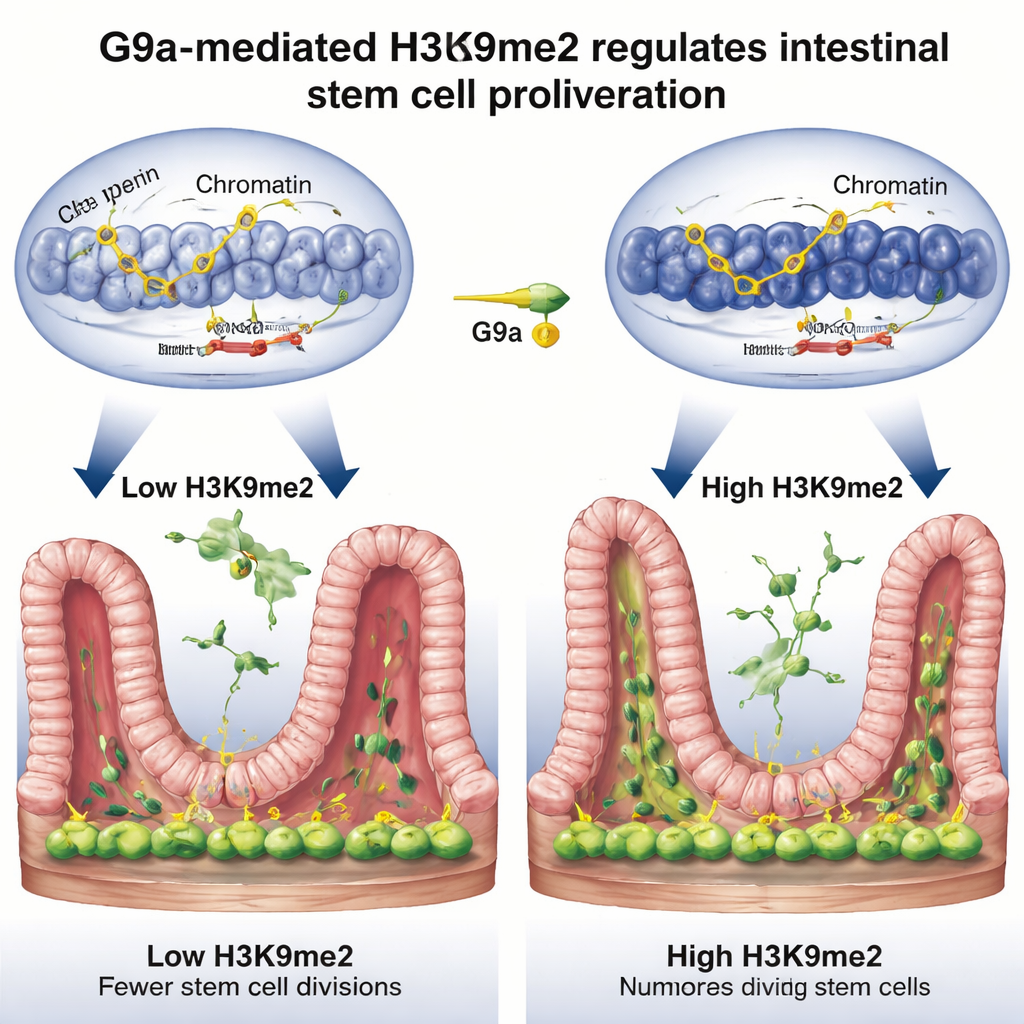
Släppa bromsen på celldelning
Vidaregrävande visade att teamet frågade vilka gener som kontrolleras av denna reparationsbrytare. Genom att kombinera tre kraftfulla genombredande metoder fann de att H3K9me2, satt dit av G9a, tenderar att sitta på DNA‑sträckor som normalt fungerar som bromsar på cellcykeln—gener som Rb1cc1, Rb1, Cdkn1a och Pten, vilka saktar ner eller stoppar celldelning. När G9a saknades försvann den kemiska markören från dessa regioner, det omgivande DNA:t öppnades upp och dessa bromsande gener aktiverades mer, vilket ledde till långsammare stamcellsproliferation. Under normal reparation efter skada ökade H3K9me2‑nivåerna vid dessa gener, deras aktivitet sjönk och stamcellerna kunde dela sig friare och återbygga epitelet. I korthet tystar G9a och H3K9me2 tillfälligt ”stopp‑signalerna” så att vävnaden kan växa tillbaka.
En signalväg från immuncues till reparation
Tarmen agerar inte ensam; den lyssnar kontinuerligt på signaler från immunsystemet. Forskarna spårade en sådan signal uppströms om G9a. Efter skada ökade nivåerna av immunsignalen IL‑4, vilket utlöste aktivering av ett protein kallat STAT6 inne i tarmcellerna. Aktiverat STAT6 band direkt till kontrollregionen för G9a‑genen och ökade dess produktion. Detta skapade en kommandokedja: IL‑4 aktiverar STAT6, STAT6 ökar G9a, och G9a sätter dit H3K9me2 för att tysta cellcykelns bromsgener, vilket gör det möjligt för stamceller att expandera och återställa det skadade epitelet.
Vad detta betyder för framtida behandlingar
För en icke‑specialist visar dessa fynd att tarmreparation inte bara styrs av gener, utan av reversibla kemiska markörer som finjusterar när gener används. IL‑4–STAT6–G9a–H3K9me2‑vägen fungerar som en intern kontrollpanel som tillfälligt lossar på bromsen för stamcellsdelning precis tillräckligt länge för att läka, och sedan kan återställas. I framtiden kan behandlingar som varsamt förstärker denna väg—såsom läkemedel eller genbaserade verktyg som höjer G9a‑nivåer vid rätt tid och plats—hjälpa patienter att återhämta sig snabbare efter strålningsskador, skov av inflammatorisk tarmsjukdom eller andra tillstånd som skadar tarmepitelet, samtidigt som risken för okontrollerad celltillväxt minimeras.
Citering: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
Nyckelord: tarmregenerering, epigenetik, stamceller, histonmetylering, inflammatorisk tarmsjukdom